
【題目】下圖是采用新能源儲能器件將CO2轉化為固體產物,實現CO2的固定和儲能靈活應用的裝置。儲能器件使用Li-CO2電池,組成為:釕電極/CO2飽和的LiClO4-DMSO電解液/鋰片。下列說法不正確的是

A. Li-CO2電池的電解液由LiClO4和DMSO溶于水得到
B. CO2的固定中,每轉移8 mol e-,生成6 mol氣體
C. 過程Ⅱ中化學能轉化為電能
D. 過程Ⅰ的釕電極的電極反應式為2Li2CO3+C-4e-═4Li++3CO2↑
科目:高中化學 來源: 題型:
【題目】下列關于能源和作為能源使用的物質的敘述中錯誤的是( )
A.化石能源物質內部蘊含著大量的能量
B.綠色植物進行光合作用時,將太陽能轉化為化學能“貯存”起來
C.物質的化學能可以在一定條件下轉化為熱能、電能,為人類所利用
D.吸熱反應沒有利用價值
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種釕(Ru)基配合物光敏染料敏化太陽能電池的原理及電池中發生的主要反應如圖所示。下列說法正確的是

A. 鍍鉑導電玻璃的作用是傳遞I-
B. 電池工作時,光能轉變為電能,X為電池的正極
C. 電池的電解質溶液中I-和I3-的濃度均不斷減小
D. 電解質溶液中發生反應2Ru3++3I-═2Ru2++I3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若測得鹽酸和氫氧化鈉溶液反應生成18g水時放出的熱量為Q,則下列各反應在溶液中生成18g水時,放出的熱量也為Q的是
①醋酸和氫氧化鈉溶液; ②氨水和鹽酸 ③氫氧化鉀溶液和硝酸
A.①②③B.①③C.②③D.③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積為2.0 L的密閉容器內,物質D在T ℃時發生反應,其反應物和生成物的物質的量隨時間t的變化關系如圖,下列敘述不正確的是

A. 從反應開始到第一次達到平衡時,A物質的平均反應速率為0.0667 mol/(L·min)
B. 該反應的化學方程式為2D(s) 2A(g)+B(g),該反應的平衡常數表達式為K=c(A)2·c(B)
C. 已知:反應的H>0,則第5分鐘時圖象呈現上述變化的原因可能是升高體系的溫度
D. 若在第7分鐘時增加D的物質的量,則表示A的物質的量變化正確的是a曲線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用0.100mol·L-1的NaOH溶液滴定20.00mL0.100mol·L-1的HA溶液,溶液的pH與所加NaOH溶液體積(V)的關系如圖所示。下列說法不正確的是
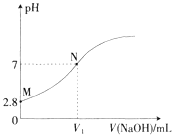
A. V1<20
B. Ka(HA)的數量級為10-5
C. M點溶液加少量水稀釋,![]() 增大
增大
D. N點后,隨著NaOH溶液的加入,溶液中水的電離程度逐漸增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物AX3和單質X2在一定條件下反應可生成化合物AX5。回答下列問題:
(1)已知AX3的熔點和沸點分別為-93.6 ℃和76 ℃,AX5的熔點為167 ℃。室溫時AX3與氣體X2反應生成1 mol AX5,放出熱量123.8 kJ。該反應的熱化學方程式為__________________________。
(2)反應AX3(g)+X2(g)![]() AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
AX5(g)在容積為10 L的密閉容器中進行。起始時AX3和X2均為0.2mol。反應在不同條件下進行,反應體系總壓強隨時間的變化如圖所示。
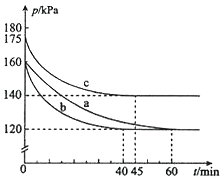
①實驗a從反應開始至達到平衡時的反應速率v(AX5)=________(保留兩位有效數字)。
②圖中3組實驗從反應開始至達到平衡時的反應速率v(AX5)由大到小的次序為___________ (填實驗序號);與實驗a相比,其他兩組改變的實驗條件及判斷依據是:
b____________________、c____________________。
③用p0表示開始時總壓強,p表示平衡時總壓強,α表示AX3的平衡轉化率,則α的表達式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)高鐵電池是一種新型可充電電池,與普通高能電池相比,該電池能長時間保持穩定的放電電壓。高鐵電池的總反應式為:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,原電池負極的電極反應式為 ______;放電時正極附近溶液的堿性____(填“增強”。“不變“或“減弱”)。
3Zn(OH)2+2Fe(OH)3+4KOH,原電池負極的電極反應式為 ______;放電時正極附近溶液的堿性____(填“增強”。“不變“或“減弱”)。
(2)三元鋰電池是以鎳鈷錳為正極材料的新型電池,鎳鈷錳材料可表示為Li1-nNixCoyMnzO2,x+y+z=1,通常簡寫為Li1-nMO2,Ni、Co、Mn三種元素分別顯+2、+3、+4價。其充電時總反應為:LiMO2+C6![]() Li1-nMO2+LinC6。
Li1-nMO2+LinC6。

①充放電電時,電解液的主要作用________________________________________。
②在Li1-nMO2材料中,若x︰y︰z=2︰3︰5,則n=______________。
③放電時,正極反應為:__________________________。
④充電時,當轉移0.2amol電子,負極材料減重_____________g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙酰乙酸乙酯是有機合成中非常重要的原料,實驗室制備乙酰乙酸乙酯的反應原理、裝置示意圖和有關數據如下所示:


實驗步驟:
(I)合成:向三頸燒瓶中加入9.8 mL無水乙酸乙酯,迅速加入0.1 g切細的金屬鈉。水浴加熱反應液,緩慢回流約2h至金屬鈉全部反應完。停止加熱,冷卻后向反應混合物中加入50%乙酸至反應液呈弱酸性。
(II)分離與提純:
①向反應混合物中加入等體積的飽和食鹽水,分離得到有機層。
②水層用5 mL無水乙酸乙酯萃取,分液。
③將①②所得有機層合并,洗滌、干燥、蒸餾得到乙酰乙酸乙酯粗產品。
④蒸餾粗產品得到乙酰乙酸乙酯3.9g。
(l)迅速加入金屬鈉的原因是_________(用化學方程式說明)。
(2)球形冷凝管中冷卻水從_____(填“上”或“下”)口進入,上方干燥管中盛有無水CaCl2,其作用是_______。
(3)實驗室制備乙酰乙酸乙酯時,通常在無水乙酸乙酯中加入微量的無水乙醇,其作用是_______。
(4)分離與提純操作①中使用的分離儀器是_______。加入飽和食鹽水的作用是_______。
(5)分離與提純操作③用飽和NaHCO3溶液洗滌的目的是______________。
(6)本實驗的產率為______%(結果保留兩位有效數字)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com