
【題目】下列敘述錯誤的是( )
A.帶相反電荷離子之間的相互作用稱為離子鍵
B.金屬元素與非金屬元素化合時,不一定形成離子鍵
C.某元素的原子最外層只有一個電子,它跟鹵素結合時所形成的化學鍵不一定是離子鍵
D.非金屬元素原子間不可能形成離子鍵
科目:高中化學 來源: 題型:
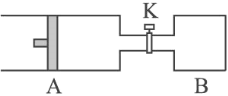
【題目】如圖所示向A中充入1 mol X 、1 mol Y,向B中充入2 mol X、2 mol Y,起始時,
V(A) = V(B) = a L。在相同溫度和有催化劑存在下,兩容器中各自發生下述反應:X(g)+Y(g)![]() 2Z(g)+W(g) ΔH<0。達到平衡時,V(A) = 1.1a L。(連通管中氣體體積不計)下列說法正確的是( )
2Z(g)+W(g) ΔH<0。達到平衡時,V(A) = 1.1a L。(連通管中氣體體積不計)下列說法正確的是( )
A. n(Z)B = 2n(Z)A
B. A容器中X的轉化率為20%
C. 若向A和B中均再加入1molX和1molY,X的體積分數均增大
D. 打開K保持溫度不變,又達到平衡時,A的體積為3.3a L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,有關說法不正確的是( )

A. 元素b的單質不能與酸性氧化物發生化學反應
B. a、b、d、f四種元素的離子半徑:f>d>a>b
C. 元素c的氧化物既能與酸反應又能與堿反應
D. a、c、e的最高價氧化物對應的水化物之間能夠相互反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時,pH = 2的CH3COOH和H2SO4溶液各1mL,分別加水稀釋到1000 mL,其溶液的pH與溶液體積(V)的關系如圖所示

(1)圖中a點的值為_________________
(2)若對上述硫酸再稀釋10000倍則溶液中n (H+) :n(SO42-)=_______
(3)在T℃時,醋酸的電離平衡常數K=1.0×10-5, Kw=1.0×10-13則下列反應CH3COO-+H2O![]() CH3COOH+OH- 的平衡常數K=_____________。
CH3COOH+OH- 的平衡常數K=_____________。
(4)在T℃時,取pH=2的硫酸溶液0.5VmL稀釋到2VmL ,與0.1mol/L的NaOH溶液0.15VmL混合后稀釋至10VmL,溶液的pH=___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過氧乙酸(CH3COOOH)是無色透明液體,易溶于水、易揮發,見光易分解,具有強氧化性的高效消毒劑,使用過氧乙酸消毒劑時通常先用水稀釋工業品過氧乙酸,然后用噴霧法對空氣與地面進行消毒.
(1)配制220mL0.05mol/L的過氧乙酸溶液,需使用的儀器有:燒杯、量筒、玻璃棒及__________________、____________________;
(2)配制過程中,可能引起濃度偏高的操作有__________________
A.容量瓶用蒸餾水洗滌后未干燥,含有少量蒸餾水
B.轉移溶液時,不慎有少量溶液灑在容量瓶外
C.定容時,俯視容量瓶刻度線進行定容
D.定容后,把容量瓶倒置搖勻后發現液面低于刻度線,補充幾滴水至刻度線
(3)過氧乙酸半小時內會完全分解成乙酸(CH3COOH)和一種常見的氣體單質,檢驗該氣體單質的實驗方法是_____________________________.
(4)如果生產過氧乙酸的原料CH3COONa中混有了SO42﹣,要想除掉SO42﹣請選擇下列試劑按照加入先后順序填空__________________________________________(試劑不必選完,填序號即可)
①鹽酸;②醋酸鋇溶液;③氯化鋇溶液;④醋酸;⑤碳酸鈉溶液;⑥NaHCO3溶液.
(5)制取過氧乙酸反應原理為:H2O2+CH3COOH![]() CH3COOOH(過氧乙酸)+H2O,現稱取5.0g用上述方法制取的過氧乙酸試樣(液體),稀釋至100mL備用.取上述稀釋后過氧乙酸試樣5.0mL,用0.01mol/L KMnO4溶液以除去其中的H2O2,隨即加入10% KI溶液10 mL,搖勻(化學反應方程式為CH3COOOH+2KI=CH3COOK+I2+KOH)再將0.05mol/L Na2S2O3標準溶液加入到上述混合溶液中(化學反應方程式為:I2+2Na2S2O3=2NaI+Na2S4O6),消耗Na2S2O3標準溶液的總體積為20mL.通過計算確定原試樣中過氧乙酸的質量分數為____________________.
CH3COOOH(過氧乙酸)+H2O,現稱取5.0g用上述方法制取的過氧乙酸試樣(液體),稀釋至100mL備用.取上述稀釋后過氧乙酸試樣5.0mL,用0.01mol/L KMnO4溶液以除去其中的H2O2,隨即加入10% KI溶液10 mL,搖勻(化學反應方程式為CH3COOOH+2KI=CH3COOK+I2+KOH)再將0.05mol/L Na2S2O3標準溶液加入到上述混合溶液中(化學反應方程式為:I2+2Na2S2O3=2NaI+Na2S4O6),消耗Na2S2O3標準溶液的總體積為20mL.通過計算確定原試樣中過氧乙酸的質量分數為____________________.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鑭系金屬元素鈰(Ce)常見有+3、+4兩種價態,鈰的合金耐高溫,可以用來制造噴氣推進器零件。請回答下列問題:
(1)霧霾中含有的污染物NO可以被含Ce4+的溶液吸收,生成NO2-、NO3- 物質的量之比為1:1,試寫出該反應的離子方程式:______________________。
(2)用電解的方法可將上述吸收液中的NO2- 轉化為穩定的無毒氣體,同時生成Ce4+,其原理如下圖所示。

①無毒氣體從電解槽的_______(填字母代號)口逸出。
②每生成1mol無毒氣體,同時可再生Ce4+ ______mol
(3)鈰元素在自然界中主要以氟碳鈰礦的形式存在,其主要化學成分為 CeFCO3。工業上利用氟碳鈰礦提取CeCl3的一種工藝流程如下圖所示
![]()

①焙燒過程中發生的主要反應的氧化劑和還原劑的物質的量之比為__________。
②向Ce(BF4)3中加入KCl溶液的目的是_________________________________。
③加熱CeCl3·6H2O和NH4Cl的固體混合物可得固體無水CeCl3,其中NH4Cl的作用是_________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度和壓強相同時,在體積相同的兩個密閉容器甲和乙,甲中充滿O2氣體,乙中充滿O2和O3的混合氣體,下列說法正確的是
A. 兩容器中氣體的質量相等 B. 兩容器中氣體的分子數目相等
C. 兩容器中氣體的氧原子數目相等 D. 兩容器中氣體的密度相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度和有催化劑條件下,恒容密閉容器中發生反應N2+3H2 2NH3,下列說法正確的是( )
t/min | 0 | 5 | 10 | 15 | 20 |
c(NH3)/(mol·L-1) | 0 | 1.00 | 1.60 | 1.80 | 1.80 |
A. 0~10min內,v(NH3)=0.16mol·L-1·min-1 B. 0~10min內,v(N2)=0.18mol·L-1·min-1
C. 0~10min內,v(N2)=0.16mol·L-1·min-1 D. 15~20min內,反應v(N2)正= v(N2)逆=0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求寫熱化學方程式:
(1)已知稀溶液中,1 mol H2SO4與NaOH溶液恰好完全反應時,放出114.6 kJ熱量,寫出表示H2SO4與NaOH反應的中和熱的熱化學方程式__________。
(2)已知在25℃、101kPa下,1 g乙醇在氧氣中充分燃燒生成二氧化碳和液態水釋放出29.7 kJ的熱量,試寫出乙醇燃燒熱的熱化學方程式_______________。
(3)標準狀況下,4.48L H2在足量O2中完全燃燒放出熱量Q kJ,寫出H2燃燒的熱化學方程式_________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com