
【題目】在給定的條件下,下列選項所示的物質間轉化均能一步實現的是
A.NaCl(aq) ![]() NaHCO3
NaHCO3![]() NaCO3
NaCO3
B.Al![]() NaAlO2
NaAlO2![]() AlCl3(aq)
AlCl3(aq) ![]() AlCl3(s)
AlCl3(s)
C.Fe![]() FeCl2
FeCl2![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3
D.H2SO4(aq) ![]() SO2
SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO3
(NH4)2SO3
 考前必練系列答案
考前必練系列答案科目:高中化學 來源: 題型:
【題目】PbCl2是一種重要的化工材料,常用作助溶劑、制備鉛黃等染料。工業生產中利用方鉛礦精礦(主要成分為PbS,含有FeS2等雜質)和軟錳礦(主要成分為MnO2)制備PbCl2的工藝流程如下圖所示。
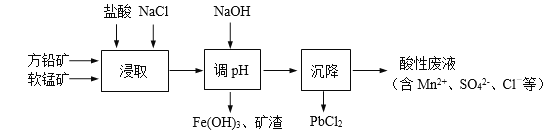
已知:i. PbCl2微溶于水
ii. PbCl2 (s) + 2Cl-(aq) ![]() PbCl42-(aq) ΔH > 0
PbCl42-(aq) ΔH > 0
(1)在浸取前礦石樣品要粉碎,目的是___________。
(2)浸取過程中MnO2與PbS發生如下反應,請將離子反應方程式配平:
__+__+PbS+__MnO2=PbCl2+______+_______+__
(3)由于PbCl2微溶于水,容易附著在方鉛礦表面形成“鈍化層”使反應速率大大降低,浸取劑中加入飽和NaCl溶液可有效避免這一現象,原因是_______________。
(4)調節pH的目的是_________________。
(5)調節pH過濾后的濾液進入沉降池,從濾液中獲得PbCl2(s)可以采取的措施有_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于可逆反應4NH3+5O2![]() 4NO+6H2O(g),下列敘述不正確的是 ( )
4NO+6H2O(g),下列敘述不正確的是 ( )
A.達到平衡時,4v(O2)正=5v(NO)逆
B.達到平衡狀態后,NH3 、O2 、NO 、H2O(g)的物質的量保持不變。
C.達到平衡狀態時,若增加容器體積,則反應速率增大
D.若單位時間生成xmolNO的同時,生成xmolNH3,則反應達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“筆、墨、紙、硯”在中國傳統文化中被稱為“文房四寶”,下列說法中錯誤的是( )
A | B | C | D |
|
|
|
|
用灼燒法可鑒別羊毫與尼龍毫的真偽 | 墨的主要成分是碳單質 | 紙的主要成分屬于合成材料 | 用石材制作硯臺的過程是物理變化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列七種有機物中:
A.CH4 B.CH2=CH2 C.![]()
D.CH3COOH E.淀粉 F.葡萄糖 G.蛋白質
(1)酸性比碳酸強的是______(填字母編號,下同).
(2)易發生銀鏡反應的是______.(3)具有正四面體結構的是______.
(4)通常用于檢驗碘單質的是______.(5)可用于合成聚乙烯塑料的是______.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知1-溴丙烷在不同條件下的反應及各物質轉化關系如圖所示:
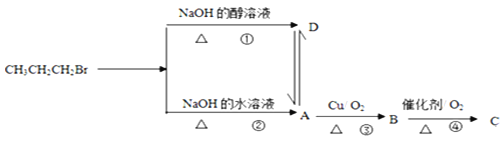
(1)D物質的結構簡式為_____________,試寫出反應②的化學反應方程式:________________。
(2)有機物A可以金屬鈉反應,試寫出該反應的化學方程式_______________________________。
(3)B物質中可能含有的官能團是_________________。檢驗該官能團常用以下哪種試劑________
A. 濃硫酸 B.NaOH溶液 C.無水硫酸銅 D.新制氫氧化銅懸濁液
該反應的原理是____________________________________________(用化學方程式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮化硅(Si3N4)是一種重要的結構陶瓷材料,可用作LED的基質材料,通過等離子法由SiH4(沸點-111.9℃)與氨氣反應制取的方程式如下:3SiH4+4NH3=Si3N4+12H2。設NA是阿伏加德羅常數的值,下列說法正確的是( )
A.常溫常壓下,1.8gSiH4所含質子的數目為3.2NA
B.標準狀況下,4.48LNH3和H2的混合氣體所含分子總數為0.2NA
C.NA個NH3分子溶于1L的水,所得溶液的物質的量濃度為1mol·L-1
D.當生成1molSi3N4時,轉移電子數目為6NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外興趣小組成員為研究金屬銅與強酸的反應 ,將6.4g銅粉分為兩等份,進行了如下實驗,請完成有關計算。
(1)取其中一份銅粉投入200mL氫離子濃度為 1molL-1 硫酸和硝酸混合液中,微熱使反應充分完成后,生成一氧化氮氣體448mL(標準狀況)。則反應前混合溶液中硫酸的物質的量濃度為_________(寫出計算過程)。
(2)用NaOH溶液吸收氮氧化物是防止NO2污染的一種方法。原理為2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O。取另一份銅粉溶于過量的硝酸溶液,假設硝酸的還原產物只有一氧化氮和二氧化氮,生成的混合氣體能被amol NaOH溶液完全吸收,試討論a的取值范圍:_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com