
【題目】計算題:常溫下,將20.0g 14%的NaCl溶液與30.0g 24%的NaCl溶液混合,混合后得到密度為1.17g/cm3的溶液.請計算(無解題過程不得分):
①混合后溶液中NaCl的質量分數;
②混合后溶液中NaCl的物質的量濃度;
③在1000g水中加多少 mol NaCl,才能使其濃度恰好與上述混合后溶液的濃度相等(結果保留一位小數).
【答案】解:①將20.0g14%的NaCl溶液跟30.0g24%的NaCl溶液混合,混合后溶液的質量為20g+30g=50g,令混合后NaCl的質量分數為ω,則:
50g×ω=20g×14%+30g×24%,解得ω=20%
答:混合后NaCl溶液的質量分數為20%.
②混合后溶液中NaCl的物質的量濃度為 ![]() mol/L=4mol/L,
mol/L=4mol/L,
答:混合后氯化鈉溶液的物質的量濃度為4mol/L.
③令需要氯化鈉的物質的量為n mol,NaCl的質量為n mol×58.5g/mol=58.5n g,則: ![]() =20%,
=20%,
解得n=4.3,
答:在1000g水中需要加入4.3 mol NaCl.
【解析】①根據m(溶質)=m(溶液)×ω計算溶質的質量,計算混合后溶液的質量,利用混合后溶質的質量等于原不同濃度溶液中氯化鈉的質量之和計算混合后溶質氫氧化質量分數;②根據c= ![]() 計算混合液的物質的量濃度;③令需要氯化鈉的物質的量為n mol,根據m=nM計算NaCl的質量,利用質量分數相等列方程計算.
計算混合液的物質的量濃度;③令需要氯化鈉的物質的量為n mol,根據m=nM計算NaCl的質量,利用質量分數相等列方程計算.


 名師金手指領銜課時系列答案
名師金手指領銜課時系列答案科目:高中化學 來源: 題型:
【題目】人造地球衛星用到的一種高能電池-銀鋅電池,它在放電時的電極反應為:Zn+2OH--2e-===ZnO+H2O,Ag2O+H2O+2e-===2Ag+2OH-。據此判斷,氧化銀是:
A.負極,被氧化B.負極,被還原
C.正極,被還原 D.正極,被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 總質量一定的油脂,無論以何種比例組合,完全水解后生成甘油的量不變
B. 用甘氨酸(![]() )和丙氨酸(
)和丙氨酸( )縮合最多可形成4種二肽
)縮合最多可形成4種二肽
C. 用碳酸鈉溶液不能區分乙醇、乙酸、苯和硝基苯四種有機物
D. 苯酚和苯甲醇互為同系物,均能使酸性高錳酸鉀溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A為淡黃色固體,T、R 為兩種常見的用途廣泛的金屬單質,D具有磁性的黑色晶體,C是無色無味的氣體,H是白色沉淀,且在潮濕空氣中迅速變為灰綠色,最終變為紅褐色固體。
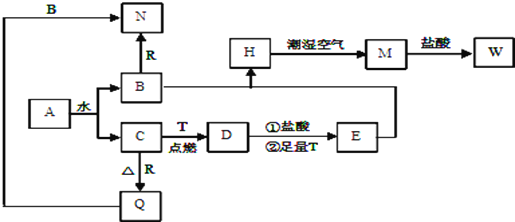
(1)寫出下列物質的化學式:D___________ R_________。寫出A的電子式 _______ 。
(2)按要求寫出下列反應方程式
H在潮濕空氣中變為M的化學方程式__________________________________________,
B與R反應的化學方程式 __________________________________________________ ,
Q與B反應的離子方程式____________________________________________________ 。
(3)向沸水中加入W飽和溶液,可制得一種紅褐色透明液體,該反應的離子方程式是__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法錯誤的是
A. 催化重整是獲得芳香烴的主要途徑之一
B. 重油的催化裂化主要是為提高輕質油的產量
C. “西氣東輸”工程中輸送的氣體主要成分為甲烷
D. 煤經氣化和液化等物理變化過程,可變為清潔能源
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com