
【題目】元素X、Y、Z、W、M、N原子序數依次增大,X與M、W與N分別同主族,且元素X、Y、Z、W分屬兩個短周期,它們四者原子序數之和為22,最外層電子數之和為16,在化合物YW2、Z2X4、X2W2中,相應分子內各原子最外層電子都滿足穩定結構,請回答下列問題:
(1)Y元素在周期表中的位置________周期________族,X、Y、Z、W、M的原子半徑由大到小的順序為____________________________________(用元素符號表示)。
(2)寫出YW2的電子式________;Z2X4結構式________________________________。
(3)X、Z、W形成的化合物,可用作化肥的鹽是________,該物質所含化學鍵的類型是________。
(4)均由X、W、M、N四種元素組成的兩種化合物相互反應,有刺激性氣味氣體放出,反應的離子方程式為____________________________________________________。
(5)火箭發動機曾經利用Z2X4作燃料X2W2作助燃劑,產物環保無污染,寫出二者反應的化學方程式________________________________________________________________________。
(6)寫出NW2通入硝酸鋇溶液中的離子方程式_____________________________________。
【答案】第二周期 第ⅣA族 Na>C>N>O>H ![]()
![]() NH4NO3 離子鍵、共價鍵 H++HSO3-===H2O+SO2↑ N2H4+2H2O2===N2+4H2O 3Ba2++3SO2+2NO3-+2H2O===3BaSO4↓+2NO+4H+
NH4NO3 離子鍵、共價鍵 H++HSO3-===H2O+SO2↑ N2H4+2H2O2===N2+4H2O 3Ba2++3SO2+2NO3-+2H2O===3BaSO4↓+2NO+4H+
【解析】
元素X、Y、Z、W、M、N原子序數依次增大,W與N同主族,結合原子序數可知,W處于第二周期、N處于第三周期,且元素X、Y、Z、W分屬兩個短周期,則X只能為H元素,Y、Z處于第二周期,X、Y、Z、W四原子序數之和為22,最外層電子數之和為16,故Y、Z、W原子序數之和為21,最外層電子數之和為15,可推知Y為C元素、Z為N元素、W為O元素,則N為S元素;X與M同主族,M原子序數大于O,故M為Na,化合物C2H2、N2H4、H2O2中,相應分子內各原子最外層電子都滿足穩定結構,據此解答。
根據分析可知X、Y、Z、W、M、N元素分別是H、C、N、O、Na、S。
(1)Y元素是C,其在周期表中的位置是第二周期第ⅣA族;由于同一周期的元素隨原子序數的增大,已知半徑逐漸減小,不同周期的元素,已知核外電子層數越多,已知半徑越大,所以X、Y、Z、W、M的原子半徑由大到小的順序是Na>C>N>O>H;故答案為:第二周期,第ⅣA族;Na>C>N>O>H。
(2)二氧化碳分子中碳原子與氧原子之間形成2對共用電子對,所以CO2的電子式為![]() ;在N2H4中兩個N原子形成一對共用電子對,每個N原子再與2個H原子形成2對共用電子對,所以N2H4結構式是
;在N2H4中兩個N原子形成一對共用電子對,每個N原子再與2個H原子形成2對共用電子對,所以N2H4結構式是![]() ;故答案為:
;故答案為:![]() ;
;![]() 。
。
(3)由H、N、O形成的化合物,可用作化肥的鹽是NH4NO3,NH4NO3中既含離子鍵又含共價鍵,故答案為:NH4NO3;離子鍵、共價鍵。
(4)均含X、W、M、N四種元素的兩種化合物分別是NaHSO4、NaHSO3,二者會發生復分解反應產生有刺激性氣味,且能使品紅溶液褪色的氣體SO2,該反應的離子方程式為H++HSO3-=H2O+SO2↑;故答案為:H++HSO3-=H2O+SO2↑。
(5)火箭發動機曾經利用Z2X4作燃料X2W2作助燃劑,產物環保無污染是H2O、N2,根據氧化還原反應中的電子守恒和原子守恒可得二者反應的方程式是N2H4+2H2O2==N2+4H2O,故答案為:N2H4+2H2O2==N2+4H2O。
(6)NW2是SO2,溶于水發生反應產生H2SO3,反應方程式是SO2+H2O=H2SO3,使溶液顯酸性,在酸性條件下NO3-表現氧化性,將H2SO3氧化為H2SO4,H2SO4電離產生的SO42-與溶液中的Ba2+發生復分解反應形成BaSO4沉淀,則NW2通入硝酸鋇溶液中的離子方程式是3Ba2++3SO2+2NO3-+2H2O===3BaSO4↓+2NO+4H+,故答案為:3Ba2++3SO2+2NO3-+2H2O===3BaSO4↓+2NO+4H+。


 寒假學與練系列答案
寒假學與練系列答案科目:高中化學 來源: 題型:
【題目】短周期元素Q、R、T、W在元素周期表中的位置如圖所示,其中T所處的.周期數與主族序數相等。
![]()
請回答下列問題:
(1)W在周期表中的位置是____________________________________,Q、R、T三種元素原子半徑由大到小的順序為____________________________________________________________________。(用元素符號表示),QO2的電子式為________________________,R的最高價氧化物的化學式____________________________。
(2)T單質與NaOH 溶液反應的離子方程式為____________________________________________________________________ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】人造地球衛星上使用的一種高能電池(銀鋅蓄電池),其電池的電極反應式為:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。據此判斷鋅是( )
A. 負極,被氧化B. 正極,被還原
C. 負極,被還原D. 正極,被氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某有機物A的紅外光譜和核磁共振氫譜如下圖所示,下列說法中錯誤的是
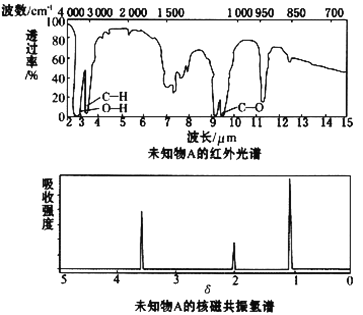
A. 由紅外光譜可知,該有機物中至少含有三種不同的化學鍵
B. 由核磁共振氫譜可知,該有機物分子中有三種不同的氫原子且個數比為1:2:3
C. 僅由其核磁共振氫譜可知其分子中的氫原子總數
D. 若A的化學式為C2H6O,則其結構簡式為CH3CH2OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B、C、D四種短周期元素, 它們的原子序數由A到D依次增大, 已知A和B原子有相同的電子層數, 且A的L層電子數是K層電子數的兩倍, C在空氣中燃燒時呈現黃色火焰, C的單質在加熱下與B的單質充分反應, 可以得到與D單質顏色相同的淡黃色固態化合物, 試根據以上敘述回答:
(1)元素名稱: A ______ B _____ C _____ D ______
(2)D元素位于周期表中___________周期____________族
(3)寫出AB2與C2B2反應的化學方程式:________________________________________。
(4)電子式表示化合物 C2D 的形成過程:________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗中,對應的現象以及結論都正確且兩者具有因果關系的是
選項 | 實驗 | 現象 | 結論 |
A | 將紅色紙條放入到新制氯水中 | 紙條褪色 | 氯氣有漂白性 |
B | 將硫酸酸化的H2O2溶液滴入到Fe(NO3)2溶液中 | 溶液變黃色 | H2O2氧化性比Fe3+強 |
C | 用坩堝鉗夾住一小塊用砂紙仔細打磨過的鋁箔在酒精燈上加熱 | 鋁熔化且滴落下來 | 鋁的熔點較低 |
D | 將NaI溶液加入到AgCl懸濁液中 | 產生黃色沉淀 | Ksp(AgCl)>Ksp(AgI) |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化合物CH3﹣CH=CH﹣C≡C﹣CF3分子結構的敘述中正確的是( )
A.6個碳原子有可能都在一條直線上
B.有5個碳原子可能在一條直線上
C.6個碳原子一定都在同一平面上
D.6個碳原子不可能在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各微粒半徑依次增大的是( )
A. Ca2+、K+、Mg2+、Al3+
B. F-、Cl-、Br-、I-
C. Si、Al、Mg、Na
D. Ca2+、K+、Cl-、S2-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟利昂是飽和碳氫化臺物的鹵族衍生物的總稱,其破壞臭氧層的化學反應機理如下(以F-12 (二氯二氟甲烷)為例):
CF2Cl2![]() CF2Cl+Cl Cl+O3→ClO+O2
CF2Cl+Cl Cl+O3→ClO+O2
ClO+ClO→ClOOCl(過氧化氯) ClOOCl![]() 2Cl+O2
2Cl+O2
下列說法中不正確的是
A. 紫外線可以增大CF2Cl2的分解速率 B. ClO +ClO![]() ClOOC1的反應中有非極性鍵的形成
ClOOC1的反應中有非極性鍵的形成
C. CF2Cl2是臭氧破壞反應的催化劑 D. 臭氧屢破壞的關鍵因素有:氟利昂,太陽光
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com