
【題目】實驗室用乙酸和正丁醇制備乙酸正丁酯,有關物質的相關數據如下:
化合物 | 密度/gcm-3 | 沸點/℃ | 溶解度/100g水 |
正丁醇 | 0.810 | 118.0 | 9 |
冰醋酸 | 1.049 | 118.1 | 互溶 |
乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
I.乙酸正丁酯粗產品的制備
在干燥的A中,裝入沸石,加入11.5mL正丁醇和9.4mL冰酷酸,再加3~4滴濃硫酸,然后安裝分水器(作用:實驗過程中不斷分離除去反應生成的水)。溫度計及回流冷凝管,熱冷凝回流反應。
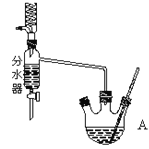
(1)實驗過程中可能產生多種有機副產物。寫出其中兩種的結構簡式:_________。
(2)實驗中為了提高乙酸正丁酯的產率,采取的措施是:_________。
II.乙酸正丁酯粗產品的制備
(3)將乙酸正丁酯粗產品用如下的操作進行精制:①水洗,②蒸餾,③用無水MgSO4干燥,④用10%碳酸鈉洗滌,正確的操作步驟是_________。
a ①②③④ b ③①④② c ①④①③② d ④①③②③
(4)將酯層采用下圖所示裝置蒸餾,圖中儀器B的名稱___________。冷卻水從______口進入(填字母),蒸餾收集乙酸正丁酯產品時,應將溫度控制在_________左右。
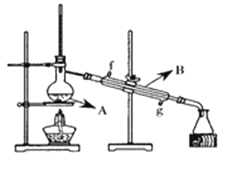
III.計算產率
(5)測量分水器內由乙酸與正丁醇反應生成的水體積為1.8mL,假設在制取乙酸正丁酯過程中反應物和生成物沒有損失,且忽略副反應,計算乙酸正丁酯的產率______。
【答案】CH3CH2CH2CH2OCH2CH2CH2CH3、CH2=CHCH2CH3 用分水器及時移走反應生成的水,減少生成物的濃度,使用過量醋酸,提高正丁醇的轉化率 c 冷凝管 g 126.1℃ 79.4%
【解析】
I.(1)正丁醇在濃硫酸的作用下發生分子內或分子間的脫水反應等副反應,分別生成1丁烯或丁醚等,其結構簡式為CH2=CHCH2CH3、CH3CH2CH2CH2OCH2CH2CH2CH3,故答案為:CH3CH2CH2CH2OCH2CH2CH2CH3、CH2=CHCH2CH3;
(2)實驗中要提高乙酸正丁酯的產率,即使酯化反應平衡向右移動,采取的措施可以是是增大另一種反應物乙酸的濃度(用量)、減小生成物的濃度,通過乙酸乙酯的制取可以知道,由于乙酸乙酯的沸點低于水,我們采取將乙酸乙酯蒸出的措施,但本題中乙酸正丁酯的沸點比水的高,因此采用分水器及時移走反應生成的水的措施,故答案為:用分水器及時移走反應生成的水,減少生成物的濃度,使用過量醋酸,提高正丁醇的轉化率;
Ⅱ.(3)乙酸正丁酯粗產品中含有的雜質:乙酸、正丁醇、水、丁醚等,分析題目給出的四種操作:①水洗②蒸餾③用無水MgSO4干燥④用10%碳酸鈉溶液洗滌,結合操作的難易、順序和必要性,如干燥要放在水洗或10%碳酸鈉洗滌之后,蒸餾操作復雜,一般放在最后,可知正確的操作步驟是①④①③②,即C選項正確,故答案為:c;
(4)圖中儀器B的作用為冷卻蒸餾得到的餾分,名稱是直形冷凝管,冷凝管的冷卻水應“下進上出”,由題干的表格信息可知,乙酸正丁酯的沸點為126.1℃,因此蒸餾收集乙酸正丁酯產品時,應將溫度控制在126.1℃,故答案為:(直形)冷凝管;g;126.1℃;
Ⅲ.根據反應的化學方程式可知,水的產率就是乙酸正丁酯的產率,根據公式![]() 可得,11.5mL正丁醇的質量為
可得,11.5mL正丁醇的質量為![]() ,物質的量為
,物質的量為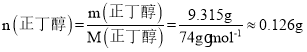 ,則完全反應生成水的物質的量為0.126mol,質量為0.126mol×18g/mol=2.268g,而實際生成水1.8g,則
,則完全反應生成水的物質的量為0.126mol,質量為0.126mol×18g/mol=2.268g,而實際生成水1.8g,則![]() ,故答案為:79.4%。
,故答案為:79.4%。


 探究與鞏固河南科學技術出版社系列答案
探究與鞏固河南科學技術出版社系列答案科目:高中化學 來源: 題型:
【題目】在給定條件下,下列選項所示的物質間轉化均能實現的是
A. NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s) ![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是用鐵鉚釘固定兩個銅質零件的示意圖,若該零件置于潮濕空氣中,下列說法正確的是
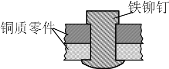
A.發生電化學腐蝕,銅為負極,銅極產生H2
B.銅易被腐蝕,銅極上發生還原反應,吸收O2
C.鐵易被腐蝕,鐵發生氧化反應,Fe-2e-=Fe2+
D.發生化學腐蝕:Fe + Cu2+ = Cu + Fe2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】W、X、Y、Z四種短周期元素,它們在周期表中位置如圖所示,下列說法正確的是![]()
![]()
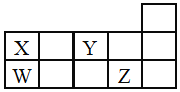
A.四種元素中原子半徑最大為W,Y元素通常沒有最高正價
B.酸性:![]()
C.![]() 、
、![]() 中所含化學鍵類型相同,熔點都很高
中所含化學鍵類型相同,熔點都很高
D.W、X形成的單質都是重要的半導體材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物M由兩種元素組成,某研究小組按如圖流程探究其組成:
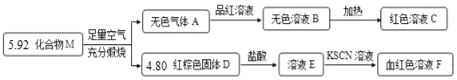
請回答:
(1)在制作印刷電路板的過程中常利用銅與溶液E的反應,反應的化學方程式為_____。
(2)將氣體A通入溶液E中,溶液由黃色變成淺綠色,且酸性明顯增強.寫出該反應的離子方程式_____。
(3)化合物M的化學式為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用![]() 表示阿伏加德羅常數的值。下列敘述正確的是
表示阿伏加德羅常數的值。下列敘述正確的是![]()
![]()
A.1mol的碳烯![]() :
:![]() 含電子數為6
含電子數為6![]()
B.一定溫度下,15g甲醛和乙酸的混合物含O原子數為![]()
![]()
C.常溫常壓下,![]() g乙醇中含有
g乙醇中含有![]() 鍵的個數為
鍵的個數為![]()
![]()
D.標準狀況下,![]() L庚烷完全燃燒后生成的
L庚烷完全燃燒后生成的![]() 分子數為
分子數為![]()
![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分析下列氧化還原反應:
Cu+4HNO3(濃)===Cu(NO3)2+2NO2↑+2H2O。
(1)該反應的還原劑是________,還原產物是________。
(2)該反應中氧化劑與氧化產物的物質的量之比是________。
(3)當有2 mol HNO3參加反應時,被氧化的物質是________ g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈉是一種應用廣泛的金屬,鈉及其化合物在生產生活中應用廣泛。某校化學課外小組為了鑒別碳酸鈉和碳酸氫鈉兩種白色固體,用不同的方法做了以下實驗,如圖所示。
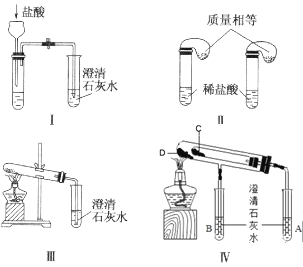
(1)只根據圖中裝置Ⅰ、Ⅱ所示實驗,能夠達到實驗目的的是__(填裝置序號)。
(2)圖Ⅲ、Ⅳ所示實驗均能鑒別這兩種物質,其反應的化學方程式__、__;Ⅳ中現象為___;與實驗Ⅲ相比,實驗Ⅳ的優點___。
(3)若用實驗Ⅳ驗證碳酸鈉和碳酸氫鈉的穩定性,則試管C中裝入的固體是__(填化學式)。
(4)將適量鈉投入下列溶液中,既能產生大量氣體又能生成沉淀的是__(填寫字母)
A.稀硫酸 B.氯化鈉溶液 C.氯化鎂溶液 D.硫酸銅溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組擬合成染料X和醫藥中間體Y。
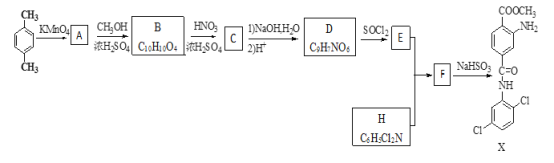
已知:①![]() ②
②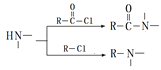 ③
③![]() ④
④![]() 。
。
(1)下列說法正確的是_________。
A.化合物A能與能與NaHCO3反應產生氣體 B.X的分子式是C15H14Cl2O3N2
C.化合物C能發生取代、還原、加成反應 D.A→B,B→C的反應類型均為取代反應
(2)化合物D的結構簡式是_________。
(3)寫出E+H→F 的化學反應方程式__________________。
(4)寫出化合物B(C10H10O4)同時符合下列條件的兩種同分異構體的結構簡式______________。
①與NaHCO3溶液反應,0.1mol該同分異構體能產生4.48L(標準狀況下)CO2氣體;②苯環上的一氯代物只有兩種且苯環上的取代基不超過三個;③核磁共振氫譜有五種不同化學環境的氫,且峰面積比為1:2:2:2:3。
(5)設計以乙烯為原料合成制備Y(![]() )的合成路線________________(用流程圖表示,無機試劑任選)。
)的合成路線________________(用流程圖表示,無機試劑任選)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com