
【題目】下列溶液一定呈堿性的是( )
A.pH=8的溶液B.含有OH-離子的溶液
C.c(OH-)>c(H+)的溶液D.NaCl溶液
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】已知元素X、Y、Z、W、R為前四周期元素,且原子序數依次增大。X基態原子核外有三個未成對電子,Z、W分別是短周期中電負性最大和最小的元素;R2+離子的3d軌道中有三對成對電子。請回答下列問題:
(1)R基態原子的電子排布式為__________,元素X、Y、Z的第一電離能由大到小的順序為(用元素符號表示)___________________。
(2)化合物XZ3的空間構型為______,R2+與NH3形成的配離子中,提供孤對電子的是_____。
(3)Z的氫化物由固體變為氣態所需克服的微粒間的作用力是________。
(4)Z、W、R形成某種化合物的晶胞結構如右圖所示,其化學式為___________。

(5)XY2-能被酸性KMnO4溶液氧化,其中MnO4-被還原為Mn2+,反應的離子方程式是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Na、Mg、Al為第三周期原子序數遞增的元素,則下列說法正確的是( )
A. 金屬活潑性:Na<Mg<Al B. 堿性:NaOH>Al(OH)3>Mg(OH)2
C. 原子半徑:Na<Mg<Al D. 與水反應的劇烈程度:Na>Mg>Al
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳跟濃硫酸共熱產生的氣體X和銅跟濃硝酸反應產生的氣體Y同時通入盛有足量氯化鋇溶液的洗氣瓶中(如圖裝置),下列有關說法正確的是( ) 
A.在Z導管出來的氣體中一定有二氧化碳
B.洗氣瓶中產生的沉淀是碳酸鋇
C.洗氣瓶中產生的沉淀是亞硫酸鋇和碳酸鋇
D.在Z導管的出口處會有無色氣體出現
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中,合成氨的反應N2+3H2![]() 2NH3,現將2mol N2和2mol H2通入該容器中反應,20s后生成0.8 mol的NH3,則H2的轉換率是多少( )
2NH3,現將2mol N2和2mol H2通入該容器中反應,20s后生成0.8 mol的NH3,則H2的轉換率是多少( )
A. 70% B. 60% C. 50% D. 40%
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應能用 H+ + HCO3- = H2O + CO2↑的離子方程式表示的反應是( )
A. 碳酸氫鈉溶液和稀硫酸的反應 B. 碳酸氫鈉溶液和醋酸溶液的反應
C. 碳酸氫鉀溶液和醋酸溶液的反應 D. 碳酸氫鋇溶液與稀硫酸的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在2L的密閉容器中X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示
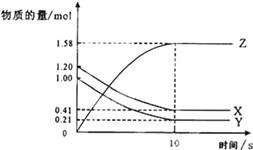
(1)該反應的化學方程式為____________________________________
(2)用Z表示的化學反應速率為_________________________
(3)在密閉容器中,下列條件的改變引起該反應的反應速率的變化是什么(填“加快”“不變”或“減慢”)。
A.縮小容器體積使壓強增大:________。
B.體積不變充入Z氣體使壓強增大:________。
C.體積不變充入氬氣使壓強增大:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能獲得預期目的是( ) 
A.實驗①燒杯中出現白色膠狀沉淀,證明非金屬性:N>C>Si
B.實驗②燒杯中出現白色渾濁,說明鎂與鹽酸反應是放熱反應
C.實驗③a、b分別滴加2滴FeCl3溶液、CuSO4溶液,驗證不同催化劑對反應速率的影響
D.實驗④利用置換反應,證明金屬單質還原性強弱,判斷金屬性強弱
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com