
ĪŠŅ}─┐Ī┐ĻPė┌═¼Ęų«Éśŗ¾wĄ─öó╩÷š²┤_Ą─╩Ū
A. ŽÓī”Ęųūė┘|┴┐ŽÓ═¼Č°ĮYśŗ▓╗═¼Ą─╗»║Ž╬’╗źĘQ×ķ═¼Ęų«Éśŗ¾w
B. ╗»īW╩ĮŽÓ═¼Č°ĮYśŗ▓╗═¼Ą─╗»║Ž╬’╗źĘQ×ķ═¼Ęų«Éśŗ¾w
C. ═¼Ęų«Éśŗ¾wų«ķgė╔ė┌ĘųūėĮM│╔ŽÓ═¼Ż¼╦∙ęį╦³éāĄ─ąį┘|ŽÓ═¼
D. ų╗ėą╔┘öĄĄ─ėąÖC╬’ų«ķg┤µį┌═¼Ęų«Éśŗ¼FŽ¾

| ─Ļ╝ē | Ė▀ųąšn│╠ | ─Ļ╝ē | │§ųąšn│╠ |
| Ė▀ę╗ | Ė▀ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ | │§ę╗ | │§ę╗├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀Č■ | Ė▀Č■├Ō┘Mšn│╠═Ų╦]ŻĪ | │§Č■ | │§Č■├Ō┘Mšn│╠═Ų╦]ŻĪ |
| Ė▀╚² | Ė▀╚²├Ō┘Mšn│╠═Ų╦]ŻĪ | │§╚² | │§╚²├Ō┘Mšn│╠═Ų╦]ŻĪ |
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐─│╗»īWąĪĮM×ķ┴╦蹊┐═ŌĮńŚl╝■ī”╗»īWĘ┤æ¬╦┘┬╩Ą─ė░ĒæŻ¼▀Mąą┴╦╚ńŽ┬īŹ“ׯ║
ĪŠīŹ“×įŁ└ĒĪ┐![]() __________
__________
ĪŠīŹ“×ā╚╚▌╝░ėøõøĪ┐
īŹ“׊Ä╠¢ | ╩ę£žŽ┬Ż¼įć╣▄ųą╦∙╝ėįćä®╝░Ųõė├┴┐/mL | ╩ę£žŽ┬╚▄ę║Ņü╔½═╩ų┴¤o╔½╦∙ąĶĢrķg/min | |||
|
|
|
ŽĪ┴“╦ß | ||
1 | 3.0 | 2.0 | 1.0 | 2.0 | 4.0 |
2 | 2.0 | 3.0 | 1.0 | 2.0 | 5.2 |
3 | 1.0 | 4.0 | 1.0 | 2.0 | 6.4 |
šł╗ž┤Ż║
Ż©1Ż®Ė∙ō■╔Ž▒ĒųąĄ─īŹ“×öĄō■Ż¼┐╔ęįĄ├ĄĮĄ─ĮYšō╩Ū___________ĪŻ
Ż©2Ż®└¹ė├īŹ“×1ųąöĄō■ėŗ╦ŃŻ¼ė├![]() Ą─ØŌČ╚ūā╗»▒Ē╩ŠĄ─ŲĮŠ∙Ę┤æ¬╦┘┬╩×ķŻ║
Ą─ØŌČ╚ūā╗»▒Ē╩ŠĄ─ŲĮŠ∙Ę┤æ¬╦┘┬╩×ķŻ║ ![]() _____________
_____________
Ż©3Ż®įōąĪĮM═¼īWĖ∙ō■Įø“×└LųŲ┴╦![]() ļSĢrķgūā╗»┌ģä▌Ą─╩ŠęŌłDŻ¼╚ńłD1╦∙╩ŠĪŻĄ½ėą═¼īW▓ķķåęčėąĄ─īŹ“×┘Y┴Ž░l¼FŻ¼įōīŹ“×▀^│╠ųą
ļSĢrķgūā╗»┌ģä▌Ą─╩ŠęŌłDŻ¼╚ńłD1╦∙╩ŠĪŻĄ½ėą═¼īW▓ķķåęčėąĄ─īŹ“×┘Y┴Ž░l¼FŻ¼įōīŹ“×▀^│╠ųą![]() ļSĢrķgūā╗»Ą─┌ģä▌æ¬╚ńłD2╦∙╩ŠĪŻįōąĪĮM═¼īWĖ∙ō■łD2╦∙╩Šą┼Žó╠ß│÷┴╦ą┬Ą─╝┘įOŻ¼▓ó└^└m▀MąąīŹ“×╠ĮŠ┐ĪŻ
ļSĢrķgūā╗»Ą─┌ģä▌æ¬╚ńłD2╦∙╩ŠĪŻįōąĪĮM═¼īWĖ∙ō■łD2╦∙╩Šą┼Žó╠ß│÷┴╦ą┬Ą─╝┘įOŻ¼▓ó└^└m▀MąąīŹ“×╠ĮŠ┐ĪŻ
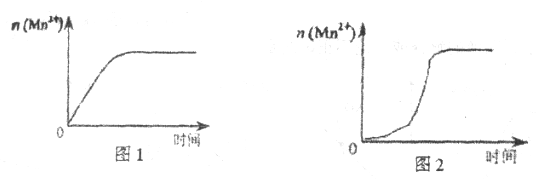
ó┘įōąĪĮM═¼īW╠ß│÷Ą─╝┘įO╩Ū____________ĪŻ
ó┌šł─ŃÄ═ų·įōąĪĮM═¼īW═Ļ│╔īŹ“×ĘĮ░ĖŻ¼▓ó╠Ņīæ▒Ēųą┐š░ūĪŻ
īŹ“׊Ä╠¢ | ╩ę£žŽ┬Ż¼įć╣▄ųą╦∙╝ėįćä®╝░Ųõė├┴┐/mL | į┘Ž“įć╣▄ųą╝ė╚ļ╔┘┴┐╣╠¾w | ╩ę£žŽ┬╚▄ę║Ņü╔½═╩ų┴¤o╔½╦∙ąĶĢrķg/min | |||
|
|
|
ŽĪ┴“╦ß | |||
4 | 3Ż«0 | 2Ż«0 | 1Ż«0 | 2Ż«0 | ____ | t |
ó█╚¶įōąĪĮM═¼īW╠ß│÷Ą─╝┘įO│╔┴óŻ¼æ¬ė^▓ņĄĮĄ─¼FŽ¾╩Ū______________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐Ę┤æ¬Ż║xA(ÜŌ)+yB(ÜŌ)![]() zC(ÜŌ)Ż¼▀_ĄĮŲĮ║ŌĢr£yĄ├AÜŌ¾wĄ─ØŌČ╚×ķ0.5 molŻ«L-1Ż¼«öį┌║Ń£žŽ┬īóįō╚▌Ų„¾wĘeöU┤¾ę╗▒ČŻ¼į┘┤╬▀_ĄĮŲĮ║ŌŻ¼£yĄ├AÜŌ¾wĄ─ØŌČ╚×ķ0.3 molŻ«L-1Ż¼ätŽ┬┴ąöó╩÷š²┤_Ą─╩Ū
zC(ÜŌ)Ż¼▀_ĄĮŲĮ║ŌĢr£yĄ├AÜŌ¾wĄ─ØŌČ╚×ķ0.5 molŻ«L-1Ż¼«öį┌║Ń£žŽ┬īóįō╚▌Ų„¾wĘeöU┤¾ę╗▒ČŻ¼į┘┤╬▀_ĄĮŲĮ║ŌŻ¼£yĄ├AÜŌ¾wĄ─ØŌČ╚×ķ0.3 molŻ«L-1Ż¼ätŽ┬┴ąöó╩÷š²┤_Ą─╩Ū
A. x+y<z B. ŲĮ║ŌŽ“ėęęŲäė
C. BĄ─▐D╗»┬╩╔²Ė▀ D. CĄ─¾wĘeĘųöĄĮĄĄ═
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐HR╩Ūę╗į¬╦ßĪŻ╩ę£žĢrŻ¼ė├0.250 moĪżL-1NaOH ╚▄ę║Ą╬Č©25.0 mLHR╚▄ę║ĢrŻ¼╚▄ę║Ą─pH ūā╗»Ūķør╚ńłD╦∙╩ŠĪŻŲõųąŻ¼b ³c▒Ē╩Šā╔ĘN╬’┘|ŪĪ║├═Ļ╚½Ę┤æ¬ĪŻŽ┬┴ąöó╩÷š²┤_Ą─╩Ū

A. HR Ą─ļŖļx│ŻöĄKa=5Ī┴10-6
B. łDųąX<7
C. a ³c╚▄ę║ųą┴ŻūėØŌČ╚┤¾ąĪĻPŽĄ╩ŪŻ║c(Na+)>c(R-)>c(HR)>c(H+)>c(OH-)
D. b ³c╚▄ę║ųą┴ŻūėØŌČ╚┤¾ąĪĻPŽĄ╩ŪŻ║c(Na+)>c(OH-)>c(R-)>c(H+)
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ė¹ė├║¼ėą╔┘┴┐┬╚╗»Ō}Ą─┬╚╗»Ōc╣╠¾wŻ¼┼õųŲ100 mL a molĪżLŻŁ1Ą─┬╚╗»Ōc╚▄ę║Ż¼įOėŗ┴╦Ž┬├µĄ─▓┘ū„ĘĮ░ĖĪŻĖ∙ō■ĘĮ░Ė▓┘ū„▓Į¾E╗ž┤Ž┬┴ąå¢Ņ}Ż║

(1)ĘQ┴┐┤ų¹}śėŲĘm gŻ¼į┌═ą▒P╠ņŲĮū¾▒P╔ŽĘ┼________Ż¼ėę▒P╔ŽĘ┼_______ĪŻ
(2)š¶░l▓┘ū„Ģræ¬īóę║¾wĘ┼į┌________ųą╝ė¤ßŻ¼Ą╚╝ė¤ßų┴________Ģr╝┤═Żų╣╝ė¤ßĪŻ
(3)į┌śėŲĘĄ─╚▄ę║ųą╝ė╚ļ▀^┴┐Ą─Na2CO3╚▄ę║Ż¼ū„ė├╩Ū_________________________________Ż¼
Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į╩Ū______________________________________________________ĪŻ
(4)į┌×Vę║ųą╝ė╚ļ¹}╦ߥ─ū„ė├╩Ū____________________________________Ż¼
Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į╩Ū____________________________________________ĪŻ
(5)┼õųŲ100 mL a molĪżLŻŁ1Ą─NaCl╚▄ę║ĢrŻ¼æ¬Å─W g╣╠¾wųąĘQ╚ĪNaClĄ─┘|┴┐×ķ________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐┐╔ė├╚ńłD╦∙╩ŠĄ─čbų├ųŲ╚Ī╔┘┴┐ęę╦ßę꧟(ŠŲŠ½¤¶Ą╚į┌łDųąŠ∙ęč┬į╚ź)ĪŻšł╗ž┤Ž┬┴ąå¢Ņ}:
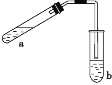
(1)įć╣▄aųąąĶę¬╝ė╚ļØŌ┴“╦ßĪó▒∙┤ū╦ß║═ęę┤╝Ė„2 mL,╝ė╚ļĄ─▓┘ū„Ēśą“╩Ū ĪŻ
(2)×ķĘ└ų╣aųąĄ─ę║¾wį┌īŹ“×Ģr░l╔·▒®Ęą,į┌╝ė¤ßŪ░æ¬▓╔╚ĪĄ─┤ļ╩®╩Ū ĪŻ
(3)īæ│÷īŹ“×ųą╝ė¤ßįć╣▄Ą──┐Ą─:ó┘ ;ó┌ ĪŻ
(4)įć╣▄bųą╩óėą’¢║═Na2CO3╚▄ę║,Ųõū„ė├╩Ū ĪŻ
(5)Ę┤æ¬ĮY╩°║¾,š±╩Äįć╣▄b,ņoų├,ė^▓ņĄĮĄ─¼FŽ¾╩Ū ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
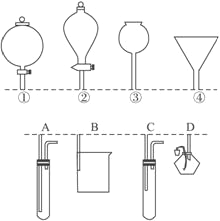
ĪŠŅ}─┐Ī┐╚ńŽ┬łD╦∙╩ŠŻ¼ó┘ó┌ó█ó▄Ęųäe╩ŪÄūĘN│ŻęŖ┬®ČĘĄ─╔Ž▓┐Ż¼AĪóBĪóCĪóD╩ŪīŹļHæ¬ė├▓┘ū„Ż©Ęųę║ĪóųŲÜŌĪóŽ“╚▌Ų„ųą╝ėę║¾wįć䮥╚Ż®ĢrŻ¼Ė„ĘN┬®ČĘĄ─Ž┬▓┐▓Õ╚ļ╚▌Ų„ųąĄ─╩ŠęŌłDŻ©łDųą┬®ČĘ╝░╚▌Ų„ųąĄ─╦ÄŲĘŠ∙ęč┬į╚źŻ¼ĶF╝▄┼_ĪóĶFŖAę▓ęč┬į╚źŻ®ĪŻšłĖ∙ō■īŹļH╩╣ė├▓┘ū„Ģr╔Ž╩÷┬®ČĘĄ─╩╣ė├ĘČć·║═╦³éāĄ─ą╬ĀŅŻ¼ųĖ│÷AĪóBĪóCĪóDĘųäe┼có┘ó┌ó█ó▄ųą──ę╗ĘNūŅ×ķŲź┼õŻ║A┼c_____________Ż¼B┼c______________Ż¼C┼c_______________Ż¼D┼c_______________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐│Ż£žŽ┬Ż¼īó 20.0 g ┘|┴┐ĘųöĄ×ķ 14.0%Ą─ KNO3╚▄ę║┼c 30.0 g ┘|┴┐ĘųöĄ×ķ 24.0%Ą─ KNO3╚▄ę║╗ņ║ŽŻ¼Ą├ĄĮĄ─├▄Č╚×ķ1.15 g/cm3Ą─╗ņ║Ž╚▄ę║ĪŻėŗ╦ŃŻ║
Ż©1Ż®╗ņ║Ž║¾╚▄ę║Ą─┘|┴┐ĘųöĄ_________ĪŻ
Ż©2Ż®╗ņ║Ž║¾╚▄ę║Ą─╬’┘|Ą─┴┐ØŌČ╚_______ĪŻ
Ż©3Ż®į┌1000g╦«ųąąĶ╚▄ĮŌ______molKNO3▓┼─▄╩╣ŲõØŌČ╚ŪĪ║├┼c╔Ž╩÷╗ņ║Ž║¾╚▄ę║Ą─ØŌČ╚ŽÓĄ╚Ż┐
Ż©4Ż®ś╦ørŽ┬44.8LHCl╚▄ė┌╦«┼õ│╔500mL╚▄ę║ĪŻėŗ╦ŃŻ║
ó┘HClĄ─╬’┘|Ą─┴┐____________________Ż╗
ó┌╦∙Ą├╚▄ę║ųą╚▄┘|Ą─╬’┘|Ą─┴┐ØŌČ╚____________________ĪŻ
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
┐Ų─┐Ż║Ė▀ųą╗»īW üĒį┤Ż║ Ņ}ą═Ż║
ĪŠŅ}─┐Ī┐ĻPė┌╣Ķ╦ßŌcęįŽ┬šfĘ©▓╗š²┤_Ą─╩Ū(ĪĪĪĪ)
A. ╣Ķ╦ßŌc┼c¹}╦ßĘ┤æ¬Ą─ļxūėĘĮ│╠╩ĮŻ║SiO32Ī¬Ż½2HŻ½=H2SiO3Ī²
B. ╣Ķ╦ßŌc╚▄ę║╦ūĘQĪ░┼▌╗©ēAĪ▒Ż¼Ųõ╚▄ę║’@ēAąįŻ¼Ą╬╝ėĘė╠¬’@╝t╔½
C. Na2CO3Ż½SiO2 ![]() Na2SiO3Ż½CO2Ī³Ż¼šf├„╣Ķ╦ß╦ßąį▒╚╠╝╦ßÅŖ
Na2SiO3Ż½CO2Ī³Ż¼šf├„╣Ķ╦ß╦ßąį▒╚╠╝╦ßÅŖ
D. ╦«▓Ż┴¦Š├ų├į┌┐šÜŌųąūā┘|Ż¼ę“×ķ┼c┐šÜŌųąĄ─CO2░l╔·Ę┤æ¬
▓ķ┐┤┤░Ė║═ĮŌ╬÷>>
ć°ļHīWąŻā×▀x - ŠÜ┴Ģāį┴ą▒Ē - įćŅ}┴ą▒Ē
║■▒▒╩Ī╗ź┬ōŠW▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ŲĮ┼_ | ŠW╔Žėą║”ą┼Žó┼eł¾īŻģ^ | ļŖą┼įp“_┼eł¾īŻģ^ | ╔µÜv╩Ę╠ō¤oų„┴xėą║”ą┼Žó┼eł¾īŻģ^ | ╔µŲ¾ŪųÖÓ┼eł¾īŻģ^
▀`Ę©║═▓╗┴╝ą┼Žó┼eł¾ļŖįÆŻ║027-86699610 ┼eł¾Ó]ŽõŻ║58377363@163.com