
【題目】原子、元素、核素、同位素等都屬于重要的化學基本概念。下列八種化學符號:![]() H、
H、![]() H、
H、![]() C、
C、![]() Li、
Li、![]() Na、
Na、![]() N、
N、![]() Li、
Li、![]() Mg
Mg
(1)涉及的核素共有__種;
(2)互為同位素的是__、__;
(3)質量數相等,但不能互稱為同位素的是__;
(4)中子數相等,但質子數不相等的是__。
(5)氫的三種同位素是__,它們與氯的同位素35Cl、37Cl相互結合為氯化氫,可得氯化氫分子的種數為__。
【答案】8 ![]() Li和
Li和![]() Li
Li ![]() H和
H和![]() H
H ![]() C和
C和![]() N
N ![]() Na和
Na和![]() Mg 1H、2H、3H 6
Mg 1H、2H、3H 6
【解析】
(1)核素是指具有一定數目質子和一定數目中子的一種原子;
(2)具有相同質子數,不同中子數同一元素的不同原子互為同位素;
(3)根據同位素的概念和原子的表示方法思考;
(4)根據質量數=質子數+中子數的關系計算;
(5)根據氫原子有三種同位素和氯原子有兩種同位素,它們兩兩結合生成氯化氫進行判斷。
(1)核素是指具有一定數目的質子和一定數目的中子的一種原子,屬于原子的有11H、12H、614C、36Li、1123Na、714N、37Li,1224Mg,它們都表示核素,即共有8種核素;
(2)質子數相同而中子數不同的同一元素的不同原子互稱同位素,在8種微粒中,36Li、37Li質子數都是3,而中子數分別為3和4,即二者互為同位素.11H、12H質子數都是1,而中子數分別為0和1,即二者互為同位素;
(3)在8中微粒中,質量數相等的是614C、714N,它們的質子數分別為6和7而不相同,它們不能互稱同位素;
(4)根據質子數等于質子數與中子數之和得,11H、12H、614C、36Li、1123Na、714N、37Li、1224Mg的中子數分別為0、1、8、3、12、7、4、12,因此中子數相等,但質子數不相等的是1123Na、1224Mg;
(5)氫原子有三種同位素1H、2H、3H,氯原子有兩種同位素35Cl、37Cl,故氯化氫分子可能為:H35Cl、H37Cl、D35Cl、D37Cl、T35Cl、T37Cl,則形成的氯化氫分子的種類有6種。


 龍人圖書快樂假期暑假作業鄭州大學出版社系列答案
龍人圖書快樂假期暑假作業鄭州大學出版社系列答案科目:高中化學 來源: 題型:
【題目】某小組設計如圖裝置,用![]() 與
與![]() 反應制取氫化鈣
反應制取氫化鈣![]() 。下列有關該實驗的說法不正確的是( )
。下列有關該實驗的說法不正確的是( )
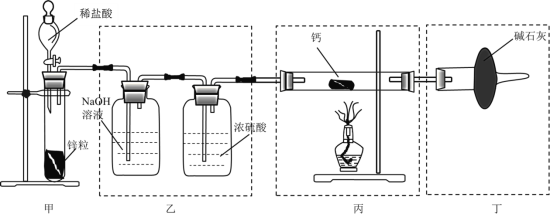
A.甲中若將稀鹽酸改為稀硫酸,裝置乙中裝![]() 溶液的洗氣瓶可舍去
溶液的洗氣瓶可舍去
B.裝置丁中堿石灰的作用是防止外界的水蒸氣與二氧化碳進入
C.實驗時應先通一段時間氫氣,檢驗尾氣純度后再點燃酒精燈加熱
D.取少量反應后固體與水反應,通過觀察是否有氣體產生來判斷產物是否為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以電解食鹽水為基礎制取氯氣等產品的工業稱為“氯堿工業”,它是目前化學工業的重要支柱之一。
(1)若電解食鹽水時消耗NaCl的質量為234 g,則在理論上最多可得氯氣的體積為________升(標準狀況)。
(2)若將2 mol的氯氣通入足量石灰乳中,理論上可得到次氯酸鈣________克。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知H2(g)+2ICl(g)=I2(g)+2HCl(g),該反應分①、②兩步進行,其能量曲線如圖所示, 已知:ICl中氯為-1價,碘為+1價。下列有關說法正確的是
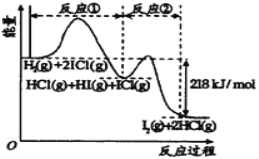
A.反應①為吸熱反應
B.反應①和②均是同種元素間發生的氧化還原反應
C.反應①比反應②的速率慢,與相應正反應的活化能有關
D.HI(g)+ICl(g) ![]() I2(g)+HCl(g) △H=-218 kJ/mol
I2(g)+HCl(g) △H=-218 kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氰[(CN)2]的化學性質與鹵素(X2)很相似,化學上稱之為擬鹵素,其氧化性介于Br2和I2之間,下列有關反應方程式不正確的是
A. (CN)2和NaOH溶液反應:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反應:MnO2+4HCN(濃)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
D. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】認真觀察下列裝置,下列說法錯誤的是
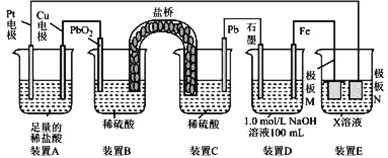
A.鹽橋中的陽離子向裝置B移動
B.裝置A中總反應的離子方程式為 Cu+2H+ ![]() Cu2++H2 ↑
Cu2++H2 ↑
C.若在裝置 D 中生成 0. 2 mol Fe(OH)3,則消耗水的物質的量共為0. 5mol
D.若裝置E的目的是在Cu材料上鍍銀,則極板 N 的材料為Cu
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室制取氯氣,將多余的氯氣用100 mL 1.7mol/L的NaOH溶液完全吸收。對吸收后的溶液進行分析化驗,測知c(OH-)=0.1mol/L (不考慮反應前后溶液的體積變化) 。ClO-和ClO3-的物質的量濃度之比為5∶1。請回答:
(1)吸收氯氣消耗的NaOH的物質的量為_______________mol。
(2)被氧化的氯氣的物質的量為_______________mol,被還原的氯氣的物質的量為 _______________mol。
(3)若采用二氧化錳和濃鹽酸共熱的方法制氯氣,制備尾氣中的氯氣所消耗的二氧化錳的質量為_______________g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年5月23日,《南陽日報》發消息稱,“水氫發動機”在當地下線,文中稱,“車載水可以實時制取氫氣,車輛只需加水即可行駛。”文章發布后引發廣泛質疑。據報道,該發動機的核心原理是用鋁粉與水進行反應得到氫氣,作為發動機的燃料。美軍曾經報道過“尿氫能”技術,與“水氫汽車”的原理如出一轍,納米鋁粉加尿可得大量氫氣,且用尿液與鋁粉反應的產氫速率比正常的水高出一倍。下列說法不正確的是( )
A.常溫下鋁和水的反應不能自發反應,將鋁加工為精細鋁粉,增大了反應接觸面積,使該反應變為自發反應
B.推測尿液與鋁粉反應比水快的可能原因是因為尿液呈弱酸性,金屬與酸反應速率加快
C.水作為鋁的氧化劑的缺點是反應生成的氫氧化鋁或氧化鋁會吸附在鋁表面,阻礙反應進行
D.若需得到標況下體積為10L的氫氣,加入的鋁粉至少為8.0g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的離子方程式正確的是
A.向Fe2(SO4)3溶液中加入過量鐵粉:Fe3++Fe=2Fe2+
B.向Al2(SO4)3溶液中加入少量氨水:![]()
C.向明礬溶液中加入過量的氫氧化鋇溶液:![]()
D.向小蘇打溶液中加少量澄清石灰水:![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com