
【題目】氮化鉻具有極高的硬度和力學強度、優異的抗腐蝕性能和高溫穩定性能,因而具有廣泛應用前景。實驗室制備CrN 反應原理為 CrCl3 +NH3![]() CrN+3HCl,裝置如圖所示
CrN+3HCl,裝置如圖所示
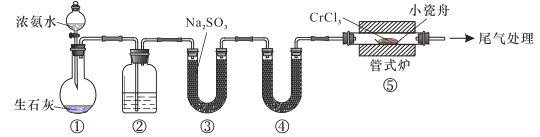
下列說法錯誤的是
A.裝置①還可以用于制取O2、Cl2、CO2等氣體
B.裝置②、④中分別盛裝NaOH溶液、KOH固體
C.裝置③中也可盛裝維生素c,其作用是除去氧氣
D.裝置⑤ 中產生的尾氣冷卻后用水吸收得到純鹽酸
科目:高中化學 來源: 題型:
【題目】科學家最近在-100℃的低溫下合成一種烴X,烴X分子的結構如圖所示(圖中的連線表示化學鍵)。下列說法正確的是( )
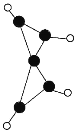
A.充分燃燒等質量的X和甲烷,X消耗的氧氣較多
B.X是一種常溫下能穩定存在的液態烴
C.X和乙烷類似,都易發生取代反應,不易發生加成反應
D.X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)據科技日報網報道,南開大學科研團隊借助鎳和苯基硼酸共催化劑,首次實現烯丙醇高效、綠色合成。烯丙醇的結構簡式為![]() 。請回答下列問題:
。請回答下列問題:
①基態鎳原子的價電子排布式為________。
②![]() 鍵,烯丙醇分子中碳原子的雜化類型是__________。
鍵,烯丙醇分子中碳原子的雜化類型是__________。
(2)乙炔是有機合成的一種重要原料。實驗室可用![]() 與水反應得到乙炔。
與水反應得到乙炔。
①將乙炔通入![]() 溶液中生成
溶液中生成![]() 紅棕色沉淀。基態
紅棕色沉淀。基態![]() 的核外電子排布式為____。
的核外電子排布式為____。
②乙炔與![]() 反應可得丙烯腈(
反應可得丙烯腈(![]() ),丙烯腈分子中碳原子的的雜化軌道類型是_______,分子中含有
),丙烯腈分子中碳原子的的雜化軌道類型是_______,分子中含有![]() 鍵的數目為___________。
鍵的數目為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】離子液體是一種由離子組成的液體,在低溫下也能以液態存在,是一種很有研究價值的溶劑。研究顯示最常見的離子液體主要由圖示正離子和負離子組成:
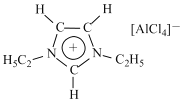
回答下列問題:
(1)按電子排布,Al劃分在元素周期表中的______區(填“s”“p”“d”或“ds”),圖中負離子的空間構型為____________________。
(2)基態Cl原子的價電子排布圖為____________________。
(3)圖中正離子有令人驚奇的穩定性, 它的電子在其環外結構中高度離域。該正離子中C原子的雜化方式為_________。該化合物中不存在____(填標號)。
A.離子鍵 B.極性鍵 C.非極性鍵 D.配位鍵 E.氫鍵
(4)C、N、H三種元素的電負性由大到小的順序為 __________,NH3與CH4的中心原子均為 sp3雜化,但是H-N-H 的鍵角小于H-C-H的鍵角,原因是________。
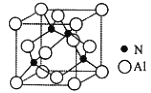
(5)AlN是一種陶瓷絕緣體,具有較高的導熱性和硬度, 其立方晶胞如圖所示,Al原子周圍緊鄰的Al原子有_____個。已知:氮化鋁的密度為dg/cm3, 阿伏加德羅常數為NA,則最近的N原子與Al原子間的距離為_____________pm。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有8種物質:①新戊烷 ②甲苯 ③聚乙烯 ④![]() ⑤2-丁炔 ⑥環己烷 ⑦鄰二甲苯 ⑧2-甲基-1,3-丁二烯,既能和酸性高錳酸鉀溶液反應又能與溴水反應的是
⑤2-丁炔 ⑥環己烷 ⑦鄰二甲苯 ⑧2-甲基-1,3-丁二烯,既能和酸性高錳酸鉀溶液反應又能與溴水反應的是
A.④⑤⑦⑧B.④⑦⑧C.④⑤⑧D.③④⑤⑦⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2是一種大氣污染物,但它在化工和食品工業上卻有廣泛應用。某興趣小組同學對SO2的實驗室制備和性質實驗進行研究。
(1)甲同學按照教材實驗要求設計如圖所示裝置制取SO2
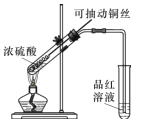
①本實驗中銅與濃硫酸反應的化學方程式是 ______,銅絲可抽動的優點是_______。
②實驗結束后,甲同學觀察到試管底部出現黑色和灰白色固體,且溶液顏色發黑。甲同學認為灰白色沉淀應是生成的白色CuSO4夾雜少許黑色固體的混合物,其中CuSO4以白色固體形式存在體現了濃硫酸的________性。
③乙同學認為該實驗設計存在問題,請從實驗安全和環保角度分析,該實驗中可能存在的問題是________。
(2)興趣小組查閱相關資料,經過綜合分析討論,重新設計實驗如下(加熱裝置略):
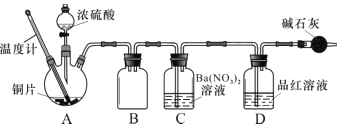
實驗記錄 A 中現象如下:
序號 | 反應溫度/℃ | 實驗現象 |
1 | 134 | 開始出現黑色絮狀物,產生后下沉,無氣體產生 |
2 | 158 | 黑色固體產生的同時,有氣體生成 |
3 | 180 | 氣體放出的速度更快,試管內溶液為黑色渾濁 |
4 | 260 | 有大量氣體產生,溶液變為藍色,試管底部產生灰白色固體,品紅溶液褪色 |
5 | 300 | 同上 |
查閱資料得知: 產物中的黑色和灰白色固體物質主要成分為 CuS、Cu2S 和 CuSO4,其中CuS 和 Cu2S為黑色固體,常溫下都不溶于稀鹽酸,在空氣中灼燒均轉化為CuO和SO2。
①實驗中盛裝濃硫酸的儀器名稱為 ____________。
②實驗記錄表明__________對實驗結果有影響,為了得到預期實驗現象,在操作上應該____________。
③裝置C 中發生反應的離子方程式是 ___________________。
④將水洗處理后的黑色固體烘干后,測定灼燒前后的質量變化,可以進一步確定黑色固體中是否一定含有 CuS其原理為__________(結合化學方程式解釋)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國成功研制出一種全新的鋁-石墨雙離子電池(AGDIB),這種新型AGDIB電池采用廉價且易得的石墨、鋁箔作為電極材料,以常規鋰鹽和碳酸酯溶劑為電解液。該電池工作原理是:充電過程中,石墨發生陰離子插層反應,而鋁電極發生鋁-鋰合金化反應,放電過程則相反。電池反應式為CxPF6+ LiyAl![]() Cx+LiPF6+ Liy-1Al,下列說法不正確的是
Cx+LiPF6+ Liy-1Al,下列說法不正確的是
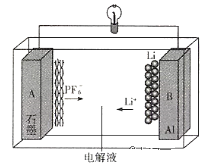
A.鋁箔是電池負極
B.充電時,鋁電極發生鋁—鋰合金化反應是還原反應
C.充電時A作陽極,放電時A電極的電極反應式為CxPF6+e-=Cx+![]()
D.廢舊AGDIB電池進行“放電處理”,讓Li+進入石墨中而有利于回收
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物 X 分子式為C3H6O,有多種同分異構體。其中之一丙醛(液態)的燃燒熱為1815kJ/mol。下列說法不正確的是
A.X 的同分異構體中,含單官能團的共 5 種
B.1mol X 最多能和 1mol H2 加成
C.表示丙醛燃燒熱的熱化學方程式為:C3H6O(l)+4O2(g) = 3CO2 (g)+3H2O(l) △H=+1815kJ/mol
D.X 的同分異構體其中之一 CH2=CHCH2OH 可以發生取代反應、加成反應、加聚反應、氧化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】As2O3(砒霜)是兩性氧化物(分子結構如圖所示),溶于鹽酸生成 AsCl3,AsCl3用 LiAlH4還原生成 AlH3。下列說法正確的是( )
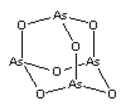
A.As2O3 分子中 As 原子的雜化方式為 sp
B.LiAlH4為共價化合物
C.AsCl3空間構型為平面正三角形
D.AlH3分子鍵角大于 109.5°
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com