
【題目】鋁是一種重要金屬,從鋁土礦(主要成分為Al2O3 , Fe2O3、SiO2等)中冶煉Al的工業生產流程如下圖: 
(1)沉淀B的化學式為 , 溶液A中含的陽離子主要有 .
(2)寫出步驟II生成溶液C 的離子方程式 , 步驟I、Ⅱ、Ⅲ都要用到的分離方法是 .
(3)生產過程中,除CaO可以循環使用外,還可以循環使用的物質有:(填化學式).
(4)生產中曾用鋁熱反應焊接鋼軌,則鋁與氧化鐵發生反應的化學方程式為:
(5)經分析,a噸鋁土礦可以冶煉出b噸的鋁(假設各生產環節中無損耗),則原鋁土礦中Al2O3的純度(質量分數)(用含a、b的最簡式表示).
【答案】
(1)SiO2;Al3+、Fe3+、H+
(2)Al3++4OH﹣=[Al(OH)4]﹣;過濾
(3)CO2、NaOH
(4)2Al+Fe 2O3 ![]() Al 2O3 +2Fe
Al 2O3 +2Fe
(5)![]() ×100%
×100%
【解析】解:由工藝流程可知,鋁土礦(主要成分為Al2O3 , Fe2O3、SiO2等),鋁土礦與過量的鹽酸反應得沉淀B和溶液A,則固體B為SiO2 , 過濾得濾液A含有氯化鋁、氯化鐵、鹽酸等,濾液中加入過量的NaOH,可推知沉淀D為氫氧化鐵,過濾得濾液C含有偏鋁酸鈉、氯化鈉,所以向濾液C中通入二氧化碳,生成氫氧化鋁沉淀與溶液E為碳酸氫鈉或碳酸鈉溶液,過濾后向E溶液中加入氧化鈣得沉淀G為碳酸鈣,同時得到氫氧化鈉溶液,氫氧化鈉溶液可以循環利用,碳酸鈣煅燒分解得氧化鈣和二氧化碳都可以循環利用,Al(OH)3灼燒得氧化鋁,電解熔融的氧化鋁可得鋁,(1)根據上面的分析可知,沉淀B的化學式為SiO2 , 溶液A中含的陽離子主要有 Al3+、Fe3+、H+ , 所以答案是:SiO2; Al3+、Fe3+、H+;(2)步驟II過量的氫氧化鈉與氯化鋁反應生成偏鋁酸鈉,反應的離子方程式 為Al3++4OH﹣=[Al(OH)4]﹣ , 根據上面的分析可知,步驟I、Ⅱ、Ⅲ都要用到的分離方法是 過濾,所以答案是:Al3++4OH﹣=[Al(OH)4]﹣;過濾;(3)生產過程中,除CaO可以循環使用外,還可以循環使用的物質有CO2、NaOH,所以答案是:CO2、NaOH;(4)鋁與氧化鐵發生反應的化學方程式為:2Al+Fe 2O3 ![]() Al 2O3 +2Fe, 所以答案是:2Al+Fe 2O3
Al 2O3 +2Fe, 所以答案是:2Al+Fe 2O3 ![]() Al 2O3 +2Fe;(5)a噸鋁土礦可以冶煉出b噸的鋁,則根據鋁元素守恒可知,需要純氧化鋁的質量為
Al 2O3 +2Fe;(5)a噸鋁土礦可以冶煉出b噸的鋁,則根據鋁元素守恒可知,需要純氧化鋁的質量為 ![]() b噸,所以原鋁土礦中Al2O3的純度為
b噸,所以原鋁土礦中Al2O3的純度為 ![]() ×100%=
×100%= ![]() ×100%,所以答案是:
×100%,所以答案是: ![]() ×100%.
×100%.


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】下列儀器能直接用酒精燈加熱的是( )
①量筒 ②錐形瓶 ③燒杯 ④試管 ⑤燒瓶 ⑥蒸發皿 ⑦坩堝
A. ②③④⑥⑦ B. ③④⑥⑦ C. ④⑥⑦ D. ②④⑦
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定濃度的鹽酸分別與等體積的NaOH溶液和氨水反應,恰好中和,消耗的鹽酸體積相同,則NaOH溶液與氨水
A. OH―濃度相等B. pH相等C. 電離度相等D. 物質的量濃度相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗事實與相應結論不正確的是
選項 | 實驗事實 | 結論 |
A | 其他條件不變,0.01 mol·L-1的酸性KMnO4溶液分別與0.1 mol·L-1的H2C2O4溶液和0.2 mol·L-1的H2C2O4溶液反應,后者褪色時間短 | 當其他條件不變時,增大反應物濃度可以使化學反應速率加快 |
B | 其他條件不變,分別將等體積、等物質的量濃度的Na2S2O3溶液和H2SO4混合液放在冷水和熱水中,放在熱水中的混合液先出現渾濁 | 當其他條件不變時,反應體系的溫度越高,化學反應速率越快 |
C | 將少量MnO2粉末加入盛有10%雙氧水的錐形瓶內,在化學反應前后,MnO2的質量和化學性質都沒有發生改變 | 催化劑雖然可以加快化學反應的速率,但一定不參與化學反應過程 |
D | 一定條件下,分別在容積為1 L和容積為2 L的兩個密閉容器中加入等量的氫氣和碘蒸氣,發生如下反應:H2(g)+I2(g) | 當其他條件不變時,氣態反應體系的壓強越大,化學反應速率越快 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定物質的量的SO2與NaOH溶液反應,所得溶液中含Na2SO3和NaHSO3,若兩者物質的量之比為3﹕5,則參加反應的SO2與NaOH的物質的量之比為
A. 3﹕5 B. 1﹕2 C. 18﹕8 D. 8﹕11
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在氯化鐵、氯化銅和鹽酸的混合溶液中加入鐵粉,待反應結束,剩余的固體能被磁鐵吸引,則反應后溶液中大量存在的陽離子是
A. Fe2+B. Fe3+C. Cu2+D. H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷及其化合物在磁性材料、電池材料、超硬材料及催化劑等領域有廣泛應用.
(1)CoxNi(1-x)Fe2O4可用作H2O2分解的催化劑
①已知CoxNi(1-x)Fe2O4中Co、Ni化合價均為+2,則該化合物這鐵元素的化合價為_______
②如圖1表示兩種不同方法制得的催化劑CoxNi(1-x)Fe2O4在10℃時催化分解6%的H2O2溶液的相對初始速率隨x變化曲線.由圖中信息可知:_______法制取得到的催化劑活性更高;Co2+、Ni2+兩種離子中催化效果更好的是__________
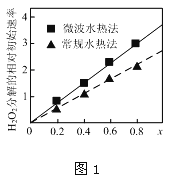
③CoxNi(1-x)Fe2O4能與氫碘酸發生氧化還原反應,所得溶液這含有三種金屬離子,寫出反應的離子方程式____________
(2)草酸鈷是制備鈷的氧化物的重要原料。下圖2為二水合草酸鈷(CoC2O4·2H2O)在空氣中受熱的質量變化曲線,曲線中300℃及以上所得固體均為鈷氧化物。

① 通過計算確定C點剩余固體的化學式為________
② 取一定質量二水合草酸鈷分解后的鈷氧化物(其中Co的化合價為+2、+3),用480 mL 5 mol/L鹽酸恰好完全溶解固體,得到CoCl2溶液和4.48 L(標準狀況)黃綠色氣體。試確定該鈷氧化物中Co、O的物質的量之比為______________。
(3)以硫化鈷(Co3S4)為原料冶煉鈷的原理為在空氣中焙燒礦石得到兩種氧化物,反應中只有一種元素被氧化,然后利用鋁熱反應可得到鈷。寫出焙燒時的化學方程式:________;寫出鋁熱反應的引發操作_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】檢驗淀粉、蛋白質、葡萄糖溶液,依次可分別使用的試劑和對應的現象正確的是
A. 碘水,變藍色 ;濃硝酸,變黃色;新制Cu(OH)2,磚紅色沉淀
B. 濃硝酸,變黃色;新制Cu(OH)2,磚紅色沉淀;碘水,變藍色
C. 新制Cu(OH)2,磚紅色沉淀;碘水,變藍色;濃硝酸,變黃色
D. 碘水,變藍色 ;新制Cu(OH)2,磚紅色沉淀;濃硝酸,變黃色
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com