
【題目】氣體A,B分別為0.6mol和0.5mol,在0.4L密閉容器中發生反應:3A+B![]() aC+2D,經5min后,此時氣體C為0.2mol;又知在此反應時間內,D的平均反應速率為0.1mol/(L·min),下面的結論正確的是( )
aC+2D,經5min后,此時氣體C為0.2mol;又知在此反應時間內,D的平均反應速率為0.1mol/(L·min),下面的結論正確的是( )
A.此時,反應混合物總物質的量為1molB.B的轉化率40%
C.A的平均反應速率為0.1mol/(L·min)D.a值為2
【答案】D
【解析】
經5min后,D的平均反應速率為0.1mol/(Lmin),則生成D的物質的量為0.1mol/(Lmin)×5min×0.4L=0.2mol,氣體C為0.2mol,則:
3A + B aC + 2D
起始量(mol) 0.6 0.5 0 0
變化量(mol) 0.3 0.1 0.2 0.2
5min后(mol)0.3 0.4 0.2 0.2
A.此時,反應混合物總物質的量為0.3mol+0.4mol+0.2mol+0.2mol=1.1mol,故A錯誤;
B.B的轉化率為![]() ×100%=20%,故B錯誤;
×100%=20%,故B錯誤;
C.v(A)═![]() =
=![]() =
=![]() =0.15mol/(Lmin),故C錯誤;
=0.15mol/(Lmin),故C錯誤;
D.物質的量之比等于化學計量數之比,故0.2mol∶0.2mol=a∶2,則x=2,故D正確;
故選D。


科目:高中化學 來源: 題型:
【題目】
(1)寫出下列儀器的名稱:
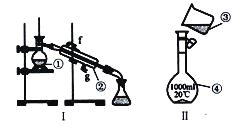
①__________________;②__________________;④__________________;
(2)儀器①~④中,使用時必須檢査是否漏水的有_______________(填序號〉
(3)現需配制250 mL0.2mol/LNaCl溶液,裝置II是某同學轉移溶液的示意圖,圖中兩處錯誤是_____________,___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外活動小組欲利用CuO與NH3反應,研究NH3的某種性質并測定其組成,設計了如下實驗裝置(夾持裝置未畫出)進行實驗。請回答下列問題:

(1)儀器a的名稱為______;儀器b中可選擇的試劑為______。
(2)實驗室中,利用裝置A,還可制取的無色氣體是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)實驗中觀察到裝置C中黑色CuO粉末變為紅色固體,量氣管有無色無味的氣體,上述現象證明NH3具有______性,寫出相應的化學方程式______。
(4)E裝置中濃硫酸的作用______。
(5)讀取氣體體積前,應對裝置F進行的操作:______。
(6)實驗完畢,若測得干燥管D增重mg,裝置F測得氣體的體積為n L(已折算成標準狀況),則氨分子中氮、氫的原子個數比為______(用含m、n字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新型鎂-鋰雙離子二次電池如圖,下列關于該電池的說法不正確的是( )
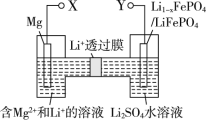
A.放電時,Li+由左向右移動
B.放電時,導線上每通過1 mol e-,左室溶液質量減輕5 g
C.充電時,外加電源的正極與Y相連
D.充電時,陽極上的電極反應式為LiFePO4 -xe-=Li1-xFePO4+xLi+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在密閉容器中一定量混合氣體發生反應:2A(g)+B(g)![]() xC(g),達到平衡時測得A的濃度為0.5mol/L,在溫度不變的條件下,將容器中的容積擴大到原來2倍,再達平衡時,測得A的濃度為0.3mol/L,下列有關判斷正確的是
xC(g),達到平衡時測得A的濃度為0.5mol/L,在溫度不變的條件下,將容器中的容積擴大到原來2倍,再達平衡時,測得A的濃度為0.3mol/L,下列有關判斷正確的是
A. x=3 B. 平衡向正反應方向移動
C. B的轉化率降低 D. C的體積分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:FeCl3+3KSCN![]() Fe(SCN)3+3KCl,離子方程式為:Fe3++3SCN-
Fe(SCN)3+3KCl,離子方程式為:Fe3++3SCN-![]() Fe(SCN)3,達到平衡后,進行下列操作,平衡怎樣移動?
Fe(SCN)3,達到平衡后,進行下列操作,平衡怎樣移動?
(1)加入少量FeCl3固體:平衡向____________移動;
(2)加入少量KSCN固體:平衡向____________移動;
(3)加入少量KCl固體:平衡____________移動,其理由是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂用于照明彈,是因為鎂能在空氣中燃燒產生耀眼光芒,并發生如下三個反應:
①2Mg+O2![]() 2MgO、②3Mg+N2
2MgO、②3Mg+N2![]() Mg3N2、③2Mg+CO2
Mg3N2、③2Mg+CO2![]() 2MgO+C(黑色)。
2MgO+C(黑色)。
關于上述三個反應的敘述不正確的是( )
A.反應①②③的還原劑都是金屬鎂B.反應①和③中都是氧元素被還原
C.反應②的生成物中氮元素為-3價D.反應③的氧化劑是二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外活動小組欲利用CuO與NH3反應,研究NH3的某種性質并測定其組成,設計了如下實驗裝置(夾持裝置未畫出)進行實驗。請回答下列問題:

(1)儀器a的名稱為______;儀器b中可選擇的試劑為______。
(2)實驗室中,利用裝置A,還可制取的無色氣體是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)實驗中觀察到裝置C中黑色CuO粉末變為紅色固體,量氣管有無色無味的氣體,上述現象證明NH3具有______性,寫出相應的化學方程式______。
(4)E裝置中濃硫酸的作用______。
(5)讀取氣體體積前,應對裝置F進行的操作:______。
(6)實驗完畢,若測得干燥管D增重mg,裝置F測得氣體的體積為n L(已折算成標準狀況),則氨分子中氮、氫的原子個數比為______(用含m、n字母的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)等物質的量的氧氣(O2)和臭氧(O3),所含的分子數之比為___,所含的氧原子數之比為___,其相對分子量之比為___,其質量之比為___;若O2和 O3質量相等,則其分子數之比為___,氧原子數之比___。
(2)一定條件下,硝酸銨受熱分解的化學方程式為:5NH4NO3═2HNO3+4N2↑+9H2O,用雙線橋標出電子轉移情況___。5NH4NO3═2HNO3+4N2↑+9H2O,在該反應中是氧化產物___,被氧化與被還原的N原子個數之比為___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com