
(15分)(1)右圖是![]() 和
和![]() 反應(yīng)生成
反應(yīng)生成![]() 和
和![]() 過程中能量變化示意,請寫出
過程中能量變化示意,請寫出![]() 和
和![]() 反應(yīng)的熱化學(xué)方程式_________________________________。
反應(yīng)的熱化學(xué)方程式_________________________________。
(2)已知下列熱化學(xué)方程式:
![]()
![]() =-393.5 kJ?mol-1
=-393.5 kJ?mol-1
![]()
![]() =-483.6 kJ?mol-1
=-483.6 kJ?mol-1
![]()
![]() =-283.0 kJ?mol-1
=-283.0 kJ?mol-1
由此可知反應(yīng):![]() 9
9![]() 的焓變?yōu)開________。
的焓變?yōu)開________。
 (3)某溫度時
(3)某溫度時![]() 在水中的沉淀溶解平衡曲線如同所示。(提示
在水中的沉淀溶解平衡曲線如同所示。(提示![]() ⇋
⇋![]() (aq)的平衡稈數(shù)
(aq)的平衡稈數(shù)![]() ?
?![]() ,稱為溶度積常數(shù)。)下列說法正確的是_____(填字母序號)。
,稱為溶度積常數(shù)。)下列說法正確的是_____(填字母序號)。
A.加入![]() 可以使溶液由a點變到b點
可以使溶液由a點變到b點
B.通過蒸發(fā)可以使溶液由d點變到c點
C.d點無![]() 沉淀生成
沉淀生成
D.a(chǎn)點對應(yīng)的![]() 等于c點對應(yīng)的
等于c點對應(yīng)的![]()
(4)在一固定體積的密閉容器中,進行如下化學(xué)反應(yīng):
![]()
![]() <0,其化學(xué)平衡常數(shù)K與t關(guān)系如下表:
<0,其化學(xué)平衡常數(shù)K與t關(guān)系如下表:
t/K | 298 | 398 | 498 | …… |
K/(mol?L | 4.1× | K | K | …… |
請完成下列問題:
①試比較K![]() 、K
、K![]() 的大小,K1_______K2(填寫“>”“=”或“<”)
的大小,K1_______K2(填寫“>”“=”或“<”)
②下列各項能作為判斷浚反應(yīng)達到化學(xué)平衡狀態(tài)的依據(jù)的是__________(填字母序號)。
A.容器內(nèi)![]() 、
、![]() 、
、![]() 的濃度之比為1:3:2 B.
的濃度之比為1:3:2 B. ![]()
C.容器內(nèi)坼強保持不變 D.混合氣體的密度保持不變
E.混合氣體的平均相對分子質(zhì)量不再改蠻 E.混合氣體中各成分的濃度不再改變
 口算題卡北京婦女兒童出版社系列答案
口算題卡北京婦女兒童出版社系列答案科目:高中化學(xué) 來源: 題型:閱讀理解
| H2SO4、134~135℃ |
| H2SO4 |
| 135℃ |

查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
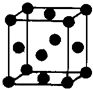 (2012?武漢模擬)[化學(xué)一選修 3:物質(zhì)結(jié)構(gòu)與性質(zhì)]有U、V、W、X、Y、Z 六種前四周期元素,原子序數(shù)依次增大,其相關(guān)信息如下表:
(2012?武漢模擬)[化學(xué)一選修 3:物質(zhì)結(jié)構(gòu)與性質(zhì)]有U、V、W、X、Y、Z 六種前四周期元素,原子序數(shù)依次增大,其相關(guān)信息如下表:| 元素編號 | 相關(guān)信息比 |
| U | 所處的周期數(shù)、族序數(shù)分別與其原子序數(shù)相等 |
| V | 基態(tài)時,電子分布在三個能級上,且各能級中電子數(shù)相等 |
| W | 基態(tài)時,2p 軌道處于半充滿狀態(tài) |
| X | 與W元素處于同一周期,且X的第一電離能小于W的第一電離 |
| Y | 是第四周期元素中未成對電子數(shù)最多的元素 |
| Z | Z 的一種核素的質(zhì)量數(shù)為65,中子數(shù)為 36 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:閱讀理解
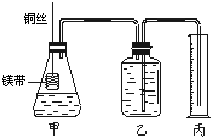 Ⅰ.銅與稀硝酸反應(yīng)的離子方程式為
Ⅰ.銅與稀硝酸反應(yīng)的離子方程式為查看答案和解析>>
科目:高中化學(xué) 來源:2010年浙江省高一第二學(xué)期期中考試(8-12班)化學(xué)試題 題型:實驗題
(6分)、右圖是研究外界因素對過氧化氫分解反應(yīng)速率影響的實驗裝置圖。某學(xué)生研究小組在50mL量筒中盛滿水,倒置于水槽中,通過分液漏斗把過氧化氫溶液加入錐形瓶中(內(nèi)中已有適量二氧化錳催化劑),記錄各時間段在室溫下收集到的氧氣的體積。

第1組:粉末狀的二氧化錳0.2g+ 5ml 6% H2O2
第2組:粉末狀的二氧化錳0.2g+ 3ml 12% H2O2
第3組:粉末狀的二氧化錳0.1g+ 5ml 6% H2O2[來源:ZXXK]
第4組:顆粒狀的二氧化錳0.1g+ 5ml 6% H2O2
|
催化劑:MnO2 |
第1組 |
第2組 |
第3組 |
第4組 |
|
前15s產(chǎn)生氧氣的量(ml) |
11 |
15 |
8 |
7 |
|
前30s產(chǎn)生氧氣的量(ml) |
21 |
24 |
11 |
9 |
|
前45s產(chǎn)生氧氣的量(ml) |
31 |
35 |
18[來源:] |
12 |
|
前60s產(chǎn)生氧氣的量(ml) |
45 |
48 |
26 |
15 |
(1)寫出H2O2分解的反應(yīng)方程式: ;
(2)從實驗的幾組數(shù)據(jù)中能得到的是: ;
(3)實驗比較反應(yīng)速率時可以測定相同時間內(nèi)產(chǎn)生氣體的體積,也可測 。
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com