
Ⅰ、下列實驗操作或對實驗事實的描述正確的是____________________
① 用量筒量取稀硫酸溶液8.0mL;
②中和熱的測定實驗中,可用金屬絲(棒)代替環形攪拌玻璃棒;
③用熱的濃鹽酸洗滌附著有MnO2的試管;
④在硫酸銅晶體結晶水含量的測定中,若加熱后的無水硫酸銅粉末表面發黑,則所測結晶水含量可能會偏高 ;
⑤Fe(OH)3膠體與FeCl3溶液可用過濾的方法分離;
⑥用堿式滴定管量取KMnO4溶液20.50mL ;
⑦將水沿燒杯內壁緩緩注入濃硫酸中,不斷用玻璃棒攪拌以稀釋濃硫酸;
⑧用濕潤的pH試紙測量某溶液pH時,測量值一定比真實值小;
⑨鋅和一定量稀硫酸反應,為加快速率而不影響H2的量可向溶液中加適量Cu(NO3)2晶體。
Ⅱ、2013年初,霧霾天氣多次肆虐天津、北京等地區。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g) 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
①該反應平衡常數表達式
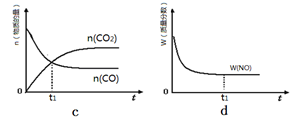
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。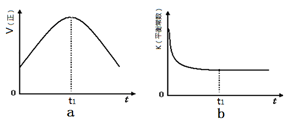
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
②2NO2(g)  N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
③H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
Ⅰ ①③④ Ⅱ(1)①K="{" C2(CO2)·C(N2) } /{ C2(NO) ·C2(CO)} ②bd
(2)CH4(g)+N2O4(g) =N2(g) +2H2O(l) + CO2(g) △H=" —898.1kJ/mol"
解析試題分析:Ⅰ①用量筒量取液體準確到小數點后一位。②金屬絲導熱性強,容易造成熱量損失。錯誤。③濃鹽酸與二氧化錳在加熱時反應產生容易溶解于水的二氯化錳、氯氣和水。④在硫酸銅晶體結晶水含量的測定中,若加熱后的無水硫酸銅粉末表面發黑,說明一部分硫酸銅發生了分解反應,把產生的三氧化硫也當作水,所以測定的水的含量偏高。⑤Fe(OH)3膠體與FeCl3溶液都能透過濾紙,不能用過濾的方法分離;⑥要用酸式滴定管量取KMnO4溶液20.50mL ;⑦濃硫酸的稀釋原則是注酸入水。將濃硫酸沿燒杯內壁緩緩注入水中,不斷用玻璃棒攪拌以使產生的熱量迅速擴散;⑧用pH試紙測量某溶液pH時不能濕潤。若用濕潤的pH試紙測量某溶液pH時,測量值可能比真實值小;也可能比真實值大;還可能無影響。⑨鋅和一定量稀硫酸反應,若加適量Cu(NO3)2晶體,會起到加入硝酸的作用,這時一般不產生氫氣。所以正確做法是①③④。
Ⅱ(1)①該反應達到化學平衡時化學平衡常數的表達式是K="{" C2(CO2)·C(N2) } /{ C2(NO) ·C2(CO)}②當反應達到化學平衡時V正="V" 逆,各種物質的濃度不變,個各種生成物濃度冪指數的乘積與各種反應物濃度冪指數的乘積是個常數。即K是定值。某物質的含量在混合物中保持不變。所以選項為:bd。(2)①-②+2×③可得熱化學方程式:CH4(g)+N2O4(g) =N2(g) +2H2O(l) + CO2(g) △H= —898.1kJ/mol
考點:考查實驗操作、平衡狀態的判斷、平衡常數及熱化學方程式的書寫等的知識。


科目:高中化學 來源: 題型:填空題
氮是地球上含量豐富的一種元素,其單質及化合物在工農業生產、生活中有著重要作用。
(1)一定溫度下,在1L容積恒定的密閉容器中充入2 mol N2和8molH2并發生反應。10min達平衡,測得氨氣的濃度為0.4 mol·L-1,此時氮氣的轉化率為________。若想提高氨氣的產率,根據化學平衡移動原理,提出合理的建議______________(寫出一條即可)。
(2)如圖是1mol NO2(g)和1mol CO(g)反應生成lmol CO2(g)和1 mol NO(g)過程中能量變化示意圖,請寫出該反應的熱化學方程式_____________________。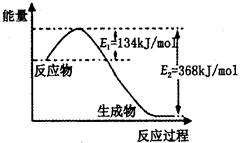
(3)在容積恒定的密閉容器中,進行如下反應:N2(g)+3H2(g)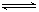 2NH3(g)△H<0,其平衡常數K與溫度T的關系如下表:
2NH3(g)△H<0,其平衡常數K與溫度T的關系如下表: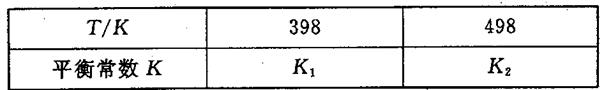
①該反應的平衡常數表達式:K=_____________;
②試判斷K1__________K2(填寫“>”“=”或“<”);
③NH3(g)燃燒的方程式為:4NH3(g)+7O2(g)=4NO2(g)+6H2O(l),已知:
①2H2(g)+O2(g)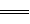 2H2O(l) △H=-483.6 kJ/mol
2H2O(l) △H=-483.6 kJ/mol
②N2(g)+2O2(g)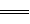 2NO2(g) △H=+67.8 kJ/mol
2NO2(g) △H=+67.8 kJ/mol
③N2(g)+3H2(g)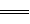 2NH3(g) △H=-92.0 kJ/mol
2NH3(g) △H=-92.0 kJ/mol
請計算NH3(g)的燃燒熱________kJ/mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
化學反應原理在工業生產中具有十分重要的意義。
(1)工業生產可以用NH3(g)與CO2(g)經過兩步反應生成尿素,兩步反應的能量變化示意圖如下:
則NH3(g)與CO2(g)反應生成尿素的熱化學方程式為 。
(2)已知反應Fe(s) +CO2(g)  FeO(s) +CO(g) ΔH ="a" kJ/mol
FeO(s) +CO(g) ΔH ="a" kJ/mol
測得在不同溫度下,該反應的平衡常數K隨溫度的變化如下:
①該反應的化學平衡常數表達式K= ,a 0(填“>”、“<”或“=”)。在500℃ 2L密閉容器中進行反應,Fe和CO2的起始量均為4 mol,則5 min后達到平衡時CO2的轉化率為 ,生成CO的平均速率v(CO)為 。
②700℃反應達到平衡后,要使該平衡向右移動,其他條件不變時,可以采取的措施有
(填字母)。
| A.縮小反應器容積 | B.增加Fe的物質的量 |
| C.升高溫度到900℃ | D.使用合適的催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
廢舊印刷電路板的回收利用可實現資源再生,并減少污染。廢舊印刷電路板經粉碎分離,能得到非金屬粉末和金屬粉末。
(1)下列處理印刷電路板非金屬粉末的方法中,不符合環境保護理念的是 (填字母)。
| A.熱裂解形成燃油 | B.露天焚燒 | C.作為有機復合建筑材料的原料 | D.直接填埋 |

| 溫度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 銅平均溶解速率(×10-3 mol·L-1·min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
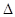 H
H
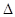 H,
H,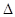 H= 。
H= 。查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(11分)研究燃料的燃燒和對污染氣體產物的無害化處理,對于防止大氣污染有重要意義。
(1)將煤轉化為清潔氣體燃料:
已知:H2(g)+1/2O2(g)=H2O(g)  H= ?241.8kJ/mol
H= ?241.8kJ/mol
C(s)+1/2O2(g)=CO(g)  H= ?110.5kJ/mol
H= ?110.5kJ/mol
寫出焦炭與水蒸氣反應制H2和CO的熱化學方程式 。
(2)一定條件下,在密閉容器內,SO2被氧化成SO3的熱化學方程式為:2SO2(g)+O2(g) 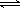 2SO3(g);
2SO3(g);
△H=?a kJ/mo1,在相同條件下要想得到2akJ熱量,加入各物質的物質的量可能是
A.4mo1 SO2和2mol O2 B.4mol SO2、2mo1 O2和2mol SO3
C.4mol SO2和4mo1 O2 D.6mo1 SO2和4mo1 O2
(3)汽車尾氣中NOx和CO的生成及轉化:
①已知氣缸中生成NO的反應為:N2(g)+O2(g)  2NO(g)
2NO(g)  H>0
H>0
在一定溫度下的定容密閉容器中,能說明此反應已達平衡的是
A.壓強不變 B.混合氣體平均相對分子質量不變
C.2v正(N2)=v逆(NO) D. N2的體積分數不再改變
②汽車燃油不完全燃燒時產生CO,有人設想按下列反應除去CO:2CO(g)=2C(s)+O2(g)  H>0,
H>0,
簡述該設想能否實現的依據 。
(4)燃料CO、H2在一定條件下可以相互轉化:CO(g)+H2O(g)  CO2(g)+H2(g)。在420℃時,平衡常數K=9。若反應開始時,CO、H2O的濃度均為0.1mol/L,則CO在此反應條件下的轉化率為 。
CO2(g)+H2(g)。在420℃時,平衡常數K=9。若反應開始時,CO、H2O的濃度均為0.1mol/L,則CO在此反應條件下的轉化率為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2SO2(g)+O2(g) 2SO3(g),反應過程的能量變化如圖所示。已知1 mol SO2(g)氧化為1 mol SO3(g)的ΔH=-99 kJ/mol。
2SO3(g),反應過程的能量變化如圖所示。已知1 mol SO2(g)氧化為1 mol SO3(g)的ΔH=-99 kJ/mol。
請回答下列問題:
(1)圖中A、C分別表示__________、__________,E的大小對該反應的反應熱有無影響?____________。該反應通常用V2O5作催化劑,加V2O5會使圖中B點升高還是降低?___________。
(2)圖中ΔH=__________kJ/mol;
(3)如果反應速率v(SO2)為0.05 mol/(L·min),則v(O2)=____mol/(L·min)
(4)已知單質硫的燃燒熱為296 kJ/mol,計算由S(s)生成3 mol SO3(g)的ΔH=_ 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
蓋斯定律在生產和科學研究中有很重要的意義。有些反應的反應熱雖然無法直接測得,但可通過間接的方法測定。現根據下列3個熱化學反應方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=―24.8kJ?mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=―47.2kJ?mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ?mol-1
寫出CO氣體還原FeO固體得到Fe固體和CO2氣體的熱化學反應方程式:__________________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
2011年11月1日,我國自行研制的“長征二號F”遙八運載火箭將“神舟八號”飛船送入太空預定軌道,兩天后與“天宮一號”目標飛行器實現成功對接。偏二甲肼(C2H8N2)和四氧化二氮(N2O4)是長征系列火箭的常規推進劑。請回答下列相關問題:
(1)偏二甲肼(C2H8N2)與四氧化二氮(N2O4)反應的化學方程式可表示為:
C2H8N2+2N2O4 3N2+2X+4H2O
3N2+2X+4H2O
則X的化學式為____________(選填下列選項的編號字母)。
A.O2 B.CO2 C.H2
(2)1 g液態偏二甲肼與足量的液態四氧化二氮完全反應生成氣態產物,放出Q kJ熱量,則相同條件下0.1 mol偏二甲肼發生該反應能放出的熱量為_____________kJ (選填下列編號字母)。
A.6Q B.30Q C.60Q
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
SO2和NOx在化學工業上有重要用途,也是大氣污染的主要來源,開發和利用并重,預防和治理并舉是當前工業上和環境保護領域研究的主要課題之一。
(1)在接觸法制硫酸的過程中,發生2SO2(g)+O2(g)  2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
2SO3(g) △H<0反應,某溫度下,SO2的平衡轉化率(α)與體系總壓強(p)的關系如下圖所示,根據圖示回答下列問題:
①平衡狀態由A到B時,平衡常數K(A) K(B)(填“>”、“<”或“=”);
②將2.0molSO2和1.0molO2置于10L的密閉容器中,若40s后反應達到平衡,此時體系總壓強為0.10MPa,這一段時間內SO2的平均反應速率為 。
該反應的平衡常數為 。
(2)用CH4催化還原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=—574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=—1160kJ·mol—1
取標準狀況下4.48LCH4并使之完全反應:
①若將NO2還原至N2,整個過程中轉移電子的物質的量為 ;
②若還原NO2和NO的混合物,放出的總熱量Q的取值范圍是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com