
請回答氯堿工業中的如下問題:
(1)氯氣、燒堿是電解食鹽水時按照固定的比率k(質量比)生成的產品。理論上k= (要求寫出計算表達式和結果);
(2)原料粗鹽中常含有泥沙和Ca2+、Mg2+、Fe3+、SO等雜質,必須精制后才能供電解使用。精制時,粗鹽溶于水過濾后,還要加入的試劑分別為①Na2CO3、②HCl(鹽酸)、③BaCl2,這3種試劑添加的合理順序是 (填序號);
(3)氯堿工業是高耗能產業,一種將電解池與燃料電池相組合的新工藝可以節(電)能30%以上。在這種工藝設計中,相關物料的傳輸與轉化關系如下圖所示,其中的電極未標出,所用的離子膜都只允許陽離子通過。
①圖中X、Y分別是 、 (填化學式),分析比較圖示中氫氧化鈉質量分數a%與b%的大小 ;
②分別寫出燃料電池B中正極、負極上發生的電極反應,正極: ;負極: ;
③這樣設計的主要節(電)能之處在于(寫出2處) 、 。
 金鑰匙試卷系列答案
金鑰匙試卷系列答案科目:高中化學 來源: 題型:填空題
(10分)某研究性學習小組,為了探究電極與原電池的電解質之間關系,設計了下列實驗方案:用鋁片、銅片、鎂片作電極,分別與下列溶液構成原電池,并接電流表。
(1)若電解質溶液為0.5mol/L硫酸,電極為銅片和鋁片,則電流計指針偏向 (填“鋁”或“銅”)。
(2)若用濃硝酸作電解質溶液,電極為銅片和鋁片,則電流計指針偏向 (填“鋁”或“銅”),鋁做 (填“正”或“負”),正極上電極反應式為:
(3)若電解質溶液為0.5mol/L氫氧化鈉溶液,電極為鎂片和鋁片,則正極發生的電極反應為 。
通過上述實驗探究,你受到的啟示是
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某課外小組分別用下圖所示裝置對原電池和電解池原理進行實驗探究。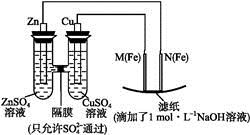

圖1 圖2
請回答:
Ⅰ.用圖1所示裝置進行第一組實驗。
(1)在保證電極反應不變的情況下,不能替代Cu作電極的是 (填序號)。
| A.鋁 | B.石墨 | C.銀 | D.鉑 |
 (填“從左向右”“從右向左”或“不”)移動;濾紙上能觀察到的現象有 。
(填“從左向右”“從右向左”或“不”)移動;濾紙上能觀察到的現象有 。  )在溶液中呈紫紅色。
)在溶液中呈紫紅色。
 +4H2O和 。
+4H2O和 。  Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2查看答案和解析>>
科目:高中化學 來源: 題型:填空題
近幾年開發的甲醇燃料電池采用鉑作電極催化劑,電池中的質子交換膜只允許質子和水分子通過。其工作原理的示意圖如下:
請回答下列問題:
(1)Pt(a)電極是電池的 極,電極反應式為 ;Pt(b)電極發生 反應(填“氧化”或“還原”),電極反應式為 。
(2)電池的總反應方程式為 。
(3)如果該電池工作時電路中通過2 mol電子,則消耗的CH3OH有 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
如圖甲、乙是電化學實驗裝置。
(1)若甲、乙兩燒杯中均盛有飽和NaCl溶液。
①甲中石墨棒上的電極反應式為__________________________________;
②乙中總反應的離子方程式為____________________________________;
③將濕潤的淀粉-KI試紙放在乙燒杯上方,發現試紙先變藍后褪色,這是因為過量的Cl2氧化了生成的I2。
若反應中Cl2和I2的物質的量之比為5:1,且生成兩種酸,該反應的化學方程式為________________________________。
(2)若甲、乙兩燒杯中均盛有CuSO4溶液。
①甲中鐵棒上的電極反應式為____________________________________;
②如果起始時乙中盛有200 mL pH=5的CuSO4溶液(25℃),一段時間后溶液的pH變為1,若要使溶液恢復到電解前的狀態,可向溶液中加入___________(填寫物質的化學式)________g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下圖中a為生鐵,A燒杯中放入苯,B燒杯中為1 mol·L-1的稀硫酸,C燒杯中為海水。
(1)B中Pt極的電極反應式為________。
(2)C中Cu極的電極反應式為________,Cu極附近溶液的pH________(填“增大”、“減小”或“不變”)。
(3)比較A、B、C中鐵被腐蝕的速率,由快到慢的順序是________。
(4)要使B中的鐵難被腐蝕,可將B中的稀硫酸改為________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某興趣小組同學利用氧化還原反應:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O設計如下原電池,其中甲、乙兩燒杯中各物質的物質的量濃度均為1 mol·L-1,鹽橋中裝有飽和K2SO4溶液。回答下列問題:
(1)發生氧化反應的燒杯是________(填“甲”或“乙”)。
(2)外電路的電流方向為:從________到________。(填“a”或“b”)
(3)電池工作時,鹽橋中的SO42—移向________(填“甲”或“乙”)燒杯。
(4)甲燒杯中發生的電極反應為______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
ZnMnO2干電池應用廣泛,其電解質溶液是ZnCl2NH4Cl混合溶液。
(1)該電池的負極材料是________。電池工作時,電子流向________(填“正極”或“負極”)。
(2)若ZnCl2NH4Cl混合溶液中含有雜質Cu2+,會加速其電極的腐蝕,其主要原因是______________________________________________。
欲除去Cu2+,最好選用下列試劑中的________(填代號)。
| A.NaOH | B.Zn | C.Fe | D.NH3·H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業廢水中常含有一定量的Cr2O72-和CrO42-,它們會對人類及生態系統產生很大損害,必須進行處理。常用的處理方法之一是電解法。
(1)該法用Fe作電極電解含Cr2O72-的酸性廢水,隨著電解進行,在陰極附近溶液pH升高,產生Cr(OH)3沉淀。用Fe作電極的原因為 。
(2)在陰極附近溶液pH升高的原因是(用電極反應解釋) ,溶液中同時生成的沉淀還有 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com