
【題目】FeCl3在現代工業生產中應用廣泛.某化學研究性學習小組模擬工業流程制備無水FeCl3,再用副產品FeCl3溶液吸收有毒的H2S。
經查閱資料得知:無水FeCl3在空氣中易潮解,加熱易升華.他們設計了制備無水FeCl3的實驗方案,裝置示意圖(加熱及夾持裝置略去)及操作步驟如下:
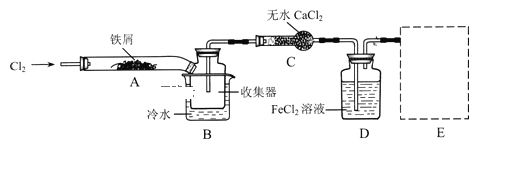
①檢驗裝置的氣密性;
②通入干燥的Cl2,趕盡裝置中的空氣;
③用酒精燈在鐵屑下方加熱至反應完成;
④…
⑤體系冷卻后,停止通入Cl2,并用干燥的N2趕盡Cl2,將收集器密封.
請回答下列問題:
(1)裝置A中反應的化學方程式為 _______________________
(2)第③步加熱后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管A右端.要使沉積的FeCl3進入收集器,第④步操作是 ________________________
(3)操作步驟中,為防止FeCl3潮解所采取的措施有(填步驟序號) _________________________
(4)裝置B中冷水浴的作用為;_________裝置C的名稱為 ______________;裝置D中FeCl2全部反應后,因失去吸收Cl2的作用而失效,寫出檢驗FeCl2是否失效的試劑:__________________________
(5)在虛線框中尾氣吸收裝置E所用試劑為____________________________
(6)用含有A12O3、SiO2和少量FeO·xFe2O3的鋁灰制備A12(SO4)3·18H2O。,工藝流程如下(部分操作和條件略):
Ⅰ.向鋁灰中加入過量稀H2SO4,過濾:
Ⅱ.向濾液中加入過量KMnO4溶液,調節溶液的pH約為3;
Ⅲ.加熱,產生大量棕色沉淀,靜置,上層溶液呈紫紅色:
Ⅳ.加入MnSO4至紫紅色消失,過濾;
V.濃縮、結晶、分離,得到產品。
已知:金屬離子的起始濃度為0.1mol·L-1
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
開始沉淀時 | 3.4 | 6.3 | 1.5 |
完全沉淀時 | 4.7 | 8.3 | 2.8 |
根據表中數據解釋步驟Ⅱ的目的:______________________________________________________
【答案】2Fe+3Cl2![]() 2FeCl3 在沉積的氯化鐵固體下方加熱 ②通入干燥的Cl2 ⑤用干燥的N2趕盡Cl2 冷卻FeCl3使其沉積,便于收集產品 干燥管 K3[Fe(CN)6]溶液,或酸性高錳酸鉀溶液 氫氧化鈉溶液 將Fe2+全部氧化為 Fe3+,調節pH將Fe3+全部轉化為沉淀
2FeCl3 在沉積的氯化鐵固體下方加熱 ②通入干燥的Cl2 ⑤用干燥的N2趕盡Cl2 冷卻FeCl3使其沉積,便于收集產品 干燥管 K3[Fe(CN)6]溶液,或酸性高錳酸鉀溶液 氫氧化鈉溶液 將Fe2+全部氧化為 Fe3+,調節pH將Fe3+全部轉化為沉淀
【解析】
(1)裝置A中鐵與氯氣發生反應制取氯化鐵,反應的化學方程式為2Fe+3Cl2![]() 2FeCl3;答案為:2Fe+3Cl2
2FeCl3;答案為:2Fe+3Cl2![]() 2FeCl3;
2FeCl3;
(2)第③步加熱后,生成的煙狀FeCl3大部分進入收集器,少量沉積在反應管A右端.要使沉積的FeCl3進入收集器,可利用FeCl3加熱易升華的性質,在沉積的氯化鐵固體下方加熱,讓氯化鐵升華后進入收集器。答案為:在沉積的氯化鐵固體下方加熱;
(3)為防止FeCl3潮解,所采取的措施主要應從無水的角度考慮。從步驟中可找到如下操作:②通入干燥的Cl2,⑤用干燥的N2趕盡Cl2。答案為:②通入干燥的Cl2 ⑤用干燥的N2趕盡Cl2;
(4)裝置B中冷水浴的作用為冷卻FeCl3使其沉積,便于收集產品。答案為:冷卻FeCl3使其沉積,便于收集產品;
裝置C的名稱為干燥管。答案為干燥管;
裝置D中FeCl2全部反應后,因失去吸收Cl2的作用而失效,檢驗FeCl2是否失效就是檢驗Fe2+,最好選用K3[Fe(CN)6]溶液,也可選用酸性高錳酸鉀溶液。答案為:K3[Fe(CN)6]溶液,或酸性高錳酸鉀溶液;
(5)在虛線框中尾氣吸收裝置E所用試劑為氫氧化鈉溶液。答案為氫氧化鈉溶液;
(6)步驟Ⅱ中,向濾液中加入過量KMnO4溶液的目的,將Fe2+全部氧化為 Fe3+;調節溶液的pH約為3的目的,將Fe3+全部轉化為Fe(OH)3沉淀。答案為:將Fe2+全部氧化為 Fe3+,調節pH將Fe3+全部轉化為沉淀。


科目:高中化學 來源: 題型:
【題目】石墨烯(如圖a)是一種由單層碳原子構成的平面結構新型碳材料,石墨烯中部分碳原子被氧化后,其平面結構會發生改變,轉化為氧化石墨烯(如圖b)。
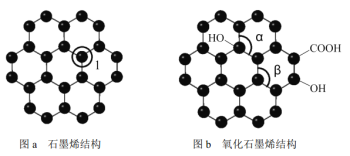
(1)圖a中,1號C與相鄰C形成σ鍵的個數為___________,該C原子雜化方式是______;圖b中鍵角α_________鍵角β。(填“>” 、 “<” 或“=” )
(2)若將圖乙所示的氧化石墨烯分散在H2O中,則氧化石墨烯中可與H2O形成氫鍵的原子有_______(填元素符號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、Q、M為常見的短周期元素,其原子序數依次增大,有關信息如下表:
X | 動植物生長不可缺少的元素,是蛋白質的重要成分 |
Y | 地殼中含量位居第一位 |
Z | 短周期中,其原子半徑最大 |
Q | 生活中大量使用其合金制品,工業上可用電解其氧化物的方法制備 |
M | 海水中大量富集的元素之一,其最高正化合價與負價的代數和為6 |
請用對應元素的化學符號或化學式回答下列問題:
(1)X在周期表中的位置為_________;X的氣態氫化物的大量生產曾經解決了地球上因糧食不足而導致的饑餓和死亡問題.請寫出該氣態氫化物的電子式_________。
(2)已知37Rb和53I都位于第五周期,分別與Z和M同一主族。下列有關說法中正確的是________(填序號)。
a.原子半徑:Rb>I
b.RbM中含有共價鍵
c.氣態氫化物熱穩定性:M>I
d.Rb、Q、M的最高價氧化物對應的水化物可以兩兩發生反應
(3)化合物QX導熱性好,熱膨脹系數小,是良好的耐熱沖擊材料,其抗熔融金屬侵蝕的能力強,是熔鑄純鐵、鋁或鋁合金理想的坩堝材料。可用Q的氧化物、焦炭和X的單質在高溫下生成QX,已知每生成1mol QX,消耗18g碳,吸收a kJ的熱量。據此,寫出以上制取QX的熱化學方程式__________。
(4)X、Y組成的一種無色氣體遇空氣變為紅棕色,將一定量該無色氣體與氧氣通入水中,恰好被完全吸收,生成一種酸,請寫出該反應的化學方程式_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將3 mol A和3 mol B混合于2 L的密閉容器中,發生如下反應:3A(g)+B(g)![]() xC(g)+2D(g),經5 min后,測得D的濃度為0.5 mol/L,C的平均反應速率為0.15 mol/(L·min)。試求:
xC(g)+2D(g),經5 min后,測得D的濃度為0.5 mol/L,C的平均反應速率為0.15 mol/(L·min)。試求:
(1)5 min后A的濃度__________________。
(2)B的平均反應速率為___________________。
(3)x的值為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在通風櫥中進行下列實驗:
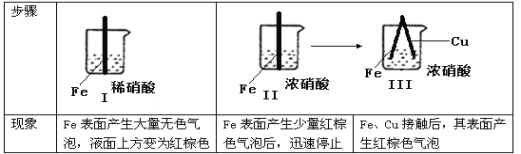
下列說法中正確的是:
A.Ⅰ中紅棕色的氣體的生成的化學方程式為:Fe + 6HNO 3== Fe(NO) 3+3H2O + 3NO2
B.Ⅱ中的現象說明Fe表面形成致密的氧化層,阻止Fe進一步反應
C.對比Ⅰ、Ⅱ中現象,說明稀HNO3的氧化性強于濃HNO3
D.針對Ⅲ中現象,在Fe、Cu之間連接電流計,可判斷Fe是否被還原
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機物的說法正確的是
A.分子式為C5H10O2,且屬于酯的同分異構體共有9種(不考慮立體異構)
B.環己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C.乙醇和丙三醇互為同系物
D.二環己烷( ![]() )的一氯代物有3種結構(不考慮立體異構)
)的一氯代物有3種結構(不考慮立體異構)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下鐵可以和 CO2 發生反應:Fe(s)+CO2(g)FeO(s)+CO(g)。一定溫度下,向某密閉容器中加入足量鐵粉并充入一定量的 CO2 氣體,反應過程中 CO2 氣體和 CO 氣體的濃度與時間的關系如圖所示:

(1)t1 時,正、逆反應速率的大小關系為 v 正_____v 逆(填“>”“<”或“=”)。
(2)4 min 內,CO 的平均反應速率 v(CO)=_____。
(3)下列條件的改變能減慢其反應速率的是_____(填序號,下同)。
①降低溫度
②減少鐵粉的質量
③保持壓強不變,充入 He 使容器的體積增大
④保持容積不變,充入 He 使體系壓強增大
(4)下列描述能說明上述反應已達平衡狀態的是_____。
①v(CO2)=v(CO)
②單位時間內生成 n mol CO2 的同時生成 n mol CO
③容器中氣體壓強不隨時間變化而變化
④容器中氣體的平均相對分子質量不隨時間變化而變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙醇(C2H6O)的結構可能有兩種:
(Ⅰ) (Ⅱ)
(Ⅱ)
關于確定其結構是(Ⅰ)而不是(Ⅱ)的方法,下列敘述中正確的是 ( )
A.1 mol乙醇與足量的鈉作用生成0.5 mol H2B.乙醇具有揮發性
C.1 mol乙醇完全燃燒時生成3 mol水D.乙醇可以制酒精飲料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鈦(Ti)是一種具有許多優良性能的金屬,鈦和鈦合金被認為是21世紀的重要金屬材料。
(1)Ti(BH4)2是一種過渡元素硼氫化物儲氫材料。
①Ti2+基態電子排布式可表示為_____。
②與BH4-互為等電子體的陽離子的化學式為_____。
③H、B、Ti原子的第一電離能由小到大的順序為_____。
(2)二氧化鈦(TiO2)是常用的、具有較高催化活性和穩定性的光催化劑,常用于污水處理。納米TiO2催化的一個實例如圖所示。
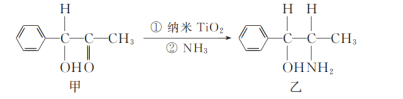
化合物乙的分子中采取sp3雜化方式的原子個數為_____。
(3)水溶液中并沒有[Ti(H2O)6)]4+離子,而是[Ti(OH)2(H2O)4]2+離子,1mol[Ti(OH)2(H2O)4]2+中σ鍵的數目為____。
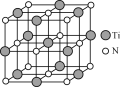
(4)氮化鈦(TiN)具有典型的NaCl型結構,某碳氮化鈦化合物,結構是用碳原子取代氮化鈦晶胞(結構如圖)頂點的氮原子,則此碳氮化鈦化合物的化學式是_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com