
【題目】下列說法不正確的是
A.容量瓶、量筒和滴定管上都標有使用溫度,量筒、容量瓶無 “0”刻度,滴定管有“0”刻度;使用時滴定管水洗后還需潤洗,但容量瓶水洗后不用潤洗
B.用電子天平稱量化學藥品時,必須先稱小燒杯的質量,再稱量加入試劑后的總質量,兩者之差即為藥品的質量
C.金屬著火時,可用細沙覆蓋滅火;電器設備引起的火災,不可用泡沫滅火器滅火
D.在4mL0.1mol·L-1的K2Cr2O7溶液中滴加數滴1mol·L-1的NaOH溶液,溶液顏色從橙色變成黃色
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】下列說法正確的是![]()
A.合成纖維、淀粉、蛋白質和地溝油都是高分子化合物
B.“火樹銀花”中的焰火實質上是金屬元素的焰色反應
C.去皮蘋果放在空氣久置變黃與紙張變黃原理相似
D.煤經過氣化、液化和干餾等物理變化過程,可以轉化為清潔能源
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】[化學—選修3:物質結構與性質](15分)A、B、C、D為原子序數依次增大的四種元索,A2-和B+具有相同的電子構型;C、 D為同周期元索,C核外電子總數是最外層電子數的3倍;D元素最外層有一個未成對電子。回答下列問題:
(1)四種元素中電負性最大的是 (填元素符號),其中C原子的核外電子排布式為__________。
(2)單質A有兩種同素異形體,其中沸點高的是 (填分子式),原因是 ;A和B的氫化物所屬的晶體類型分別為 和 。
(3)C和D反應可生成組成比為1:3的化合物E, E的立體構型為 ,中心原子的雜化軌道類型為 。
(4)化合物D2A的立體構型為 ,中心原子的價層電子對數為 ,單質D與濕潤的Na2CO3反應可制備D2A,其化學方程式為 。
(5)A和B能夠形成化合物F,其晶胞結構如圖所示,晶胞參數,a=0.566nm, F 的化學式為 :晶胞中A 原子的配位數為 ;列式計算晶體F的密度(g.cm-3) 。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列敘述中正確的是( )
4NO(g)+6H2O(g),下列敘述中正確的是( )
A. 達到化學平衡時4v正(O2)=5v逆(NO)
B. 若單位時間內生成x mol NO的同時,消耗x mol NH3,則反應達平衡狀態
C. 達到化學平衡時,若升高溫度,則正反應速率減小,逆反應速率增大
D. 平衡混合物中各物質的量濃度相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在3個體積均為1.0 L的恒容密閉容器中反應2H2(g)+CO(g)![]() CH3OH(g) 達到平衡。下列說法正確的是
CH3OH(g) 達到平衡。下列說法正確的是
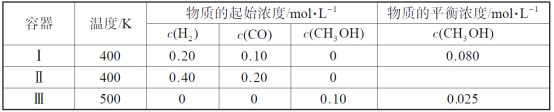
A.該反應的正反應吸熱
B.達到平衡時,容器Ⅰ中反應物轉化率比容器Ⅱ中的大
C.達到平衡時,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的兩倍
D.達到平衡時,容器Ⅲ中的正反應速率比容器Ⅰ中的大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙二酸俗名草酸,下面是化學學習小組的同學對草酸晶體(H2C2O4·xH2O)進行的探究性學習的過程,請你參與并協助他們完成相關學習任務。該組同學的研究課題是:探究測定草酸晶體(H2C2O4·xH2O)中的x值。通過查閱資料和網絡查尋得,草酸易溶于水,水溶液可以用酸性KMnO4溶液進行滴定:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O,學習小組的同學設計了滴定的方法測定x值。
①稱取1.260 g純草酸晶體,將其制成100.00 mL水溶液為待測液。
②取25.00 mL待測液放入錐形瓶中,再加入適量的稀H2SO4。
③用濃度為0.1000 mol·L-1的酸性KMnO4標準溶液進行滴定,達到終點時消耗10.00 mL。
(1)滴定時,將酸性KMnO4標準液裝在如圖中的________(填“甲”或“乙”)滴定管中。
(2)本實驗滴定達到終點的標志是___________________。
(3)通過上述數據,求得x=________。
討論:①若滴定終點時俯視滴定管刻度,則由此測得的x值會________(填“偏大”、“偏小”或“不變”,下同)。
②若滴定時所用的酸性KMnO4溶液因久置而導致濃度變小,則由此測得的x值會________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯乙烷跟化合物之間的轉化如圖所示:

(1)寫出各反應的化學方程式
①__________
②_________
③__________
④__________
(2)根據上述方程式回答下列問題:
①上述化學反應的反應類型有__________,__________,__________。
②用AgNO3溶液通過__________反應可證明鹵代烴中含鹵元素(填序號)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲烷是一種重要的基礎化工原料,不僅可制備多種重要有機產品,還可用于環境保護。請回答下列問題:
(1)用甲烷催化還原氮的氧化物可消除氮氧化物的污染。已知:

反應過程(2)是__反應(填“放熱”或“吸熱”),甲烷還原NO2生成H2O(g)、N2和CO2時的熱化學方程式是__。
(2)工廠利用甲烷與氯氣的反應原理制取氯甲烷,為妥善處理氯甲烷生產企業的副產物CCl4,以減少其對臭氧層的破壞。化學家研究在催化條件下,通過下列反應:CCl4(g)+H2(g)![]() CHCl3(g)+HCl(g),使CCl4轉化為重要的化工原料氯仿(CHCl3)(不考慮副反應)。在固定容積為2L的密閉容器中,該反應達到平衡后,測得如下數據:
CHCl3(g)+HCl(g),使CCl4轉化為重要的化工原料氯仿(CHCl3)(不考慮副反應)。在固定容積為2L的密閉容器中,該反應達到平衡后,測得如下數據:
實驗 序號 | 溫度℃ | 初始n(CCl4)( mol) | 初始n(H2)( mol) | 平衡時n(CHCl3)( mol) |
1 | 110 | 0.8 | 1.2 | |
2 | 110 | 2 | 2 | 1 |
3 | 100 | 1 | 1 | 0.6 |
①此反應在110℃時平衡常數為___。
②實驗l中,CCl4的轉化率為__。
③判斷該反應的正反應是__(填“放熱”或“吸熱”),理由是__。
④為提高實驗3中CCl4的轉化率,可采取的措施是__。
a.使用高效催化劑
b.向容器中再投入1molCCl4和1molH2
c.溫度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com