
 Na2SiO3+CO2↑,故答案為:
Na2SiO3+CO2↑,故答案為: Na2SiO3+CO2↑;
Na2SiO3+CO2↑;

 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| X | Y | Z | M | R | Q | |
| 原子半徑/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合價 | -4,+4 | -2 | -1,+7 | |||
| 其它 | 陽離子核外無電子 | 無機非金屬材料的主角 | 六種元素中原子半徑最大 | 次外層電子數是最外層電子數的4倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| X | Y | Z | M | R | Q | |
| 原子半徑/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合價 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 陽離子核外無電子 | 無機非金屬材料的主角 | 焰色反應呈黃色 |
查看答案和解析>>
科目:高中化學 來源: 題型:
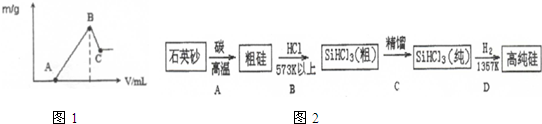
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com