
(12分)為回收和利用廢舊塑料減輕“白色污染”,某興趣小組進行如下探究:
| 實驗課題 | 探究廢舊塑料熱分解的主要產物為多種烴的混合物 |
| 查閱資料 | ①CuO能將烴氧化成CO2和H2O; ②甲苯可被酸性KMnO4溶液氧化為苯甲酸,苯甲酸能溶于苯。 |
| 實驗設計 |   |
| 實驗記錄 | 按上圖連接裝置,隔絕空氣強熱裝置A中的試管(忽略裝置內空氣的影響),一段時間后,可觀察到如下現象: ①B裝置試管中有液態物質生成; ②C中溴水的顏色變淺; ③E中黑色氧化銅變紅; ④F中無水硫酸銅變藍。 |

(1)
(2)取B中液態產物依次加入足量KMnO4溶液、NaOH溶液,待各步充分反應后靜置取上層液體
(3)檢驗并除去氣態不飽和烴 (4)無法判定E中是否有水產生 (5)
解析試題分析:(1)丙烯含有碳碳雙鍵,發生加聚反應生成聚丙烯,反應的化學方程式為 。
。
(2)甲苯能被酸性高錳酸鉀溶液氧化生成苯甲酸,苯不溶于水,苯甲酸能溶于苯,因此除去其中含有的甲苯的實驗操作是取B中液態產物依次加入足量KMnO4溶液、NaOH溶液,待各步充分反應后靜置取上層液體。
(3)廢舊塑料受熱分解可以產生不飽和烴,因此裝置C中溴水的作用是檢驗并除去氣態不飽和烴。
(4)堿石灰可以吸水,水能使無水硫酸銅變藍色,因此如果沒有裝置D,則無法判定E中是否有水產生。
(5)氫氣與氧化銅反應生成銅和水,如果是氣態烴與氧化銅反應生成銅和二氧化碳,因此要驗證使CuO變紅是氣態烴,而不是氫氣,只需要檢驗是否有二氧化碳產生即可,根據二氧化碳能使澄清石灰水變渾濁可以設計,裝置圖為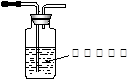 。
。
考點:考查化學實驗方案設計與探究


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:填空題
高鐵酸鉀是一種高效的多功能水處理劑,具有氧化、吸附、絮凝、、助凝、殺菌、除臭等作用,高鐵酸鉀的開發和利用正日益顯示出其廣闊的應用前景。其制備流程如下: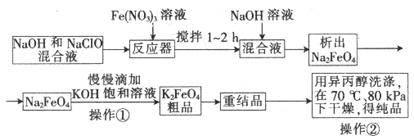
試回答下列問題
(1)反應器中,NaOH、NaClO、Fe(NO3)3發生反應生成Na2FeO4,完成并配平下列離子反應方程式:
□Fe3++□ClO─+□OH─ ==□FeO42─+□Cl─+□___________
(2)次氯酸鈉濃度對高鐵酸鉀產率有一定影響,當NaClO濃度為298g/L時,高鐵酸鈉的產率最高,此時NaClO的物質的量濃度為_______________。
(3)你認為操作①能夠發生轉化的原因是__________,慢慢滴加的原因的是___________。
(4)操作②如果溫度過高會造成高鐵酸鉀的分解,高鐵酸鉀受熱分解時生成金屬氧化物和氧氣,該反應的化學方程式為__________________。
(5)可以用電化學法制取Na2FeO4,其裝置如圖所示,則陽極的電極反應式為 ;
陰極的電極反應式為______________;電解一段時間后溶OH─的濃度會_________(填“升高”、“降低”
或“不變”)。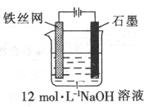
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
【化學與技術】
將磷肥生產中形成的副產物石膏(CaSO4·2H2O)轉化為硫酸鉀肥料和氯化鈣水合物儲熱材料,無論從經濟效益、資源綜合利用還是從環境保護角度看都具有重要意義。以下是石膏轉化為硫酸鉀和氯化鈣的工藝流程示意圖。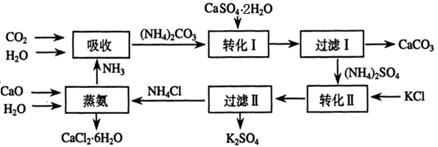
(1)本工藝中所用的原料除CaSO4·2H2O、KCl外,還需要 等原料。
(2)石膏懸濁液中加入碳酸銨溶液后發生反應的離子方程式為 。
(3)過濾Ⅰ操作所得固體中,除CaCO3外還含有 (填化學式)等物質,該固體可用作生產水泥的原料。
(4)檢驗過濾Ⅰ所得濾液中含有CO32-的方法是 。
(5)氯化鈣結晶水合物(CaCl2·6H2O)是目前常用的無機儲熱材料,選擇的依據是 。
a.熔點較低(29℃熔化) b.能導電 c.能制冷 d.無毒
(6)上述工藝流程中體現綠色化學理念的是 。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(15分)浙江省“五水共治”是水質治理的重要舉措,其中化學需氧量(COD)是水質測定中的重要指標,可以反映水中有機物等還原劑的污染程度。COD是指在一定條件下,用強氧化劑氧化水樣中的還原劑及有機物時所消耗氧化劑的量,然后折算成氧化水樣中的這些還原劑及有機物時需要氧氣的量。某學習小組用重鉻酸鉀法測定某水樣中的COD。主要的實驗裝置、儀器及具體操作步驟如下:
實驗裝置及儀器:
操作步驟:
①用儀器c將20.00mL水樣置于250mL錐形瓶中,加入數粒碎瓷片。
②在水樣中加入重鉻酸鉀標準溶液10.00mL,安裝回流裝置(如上圖所示),從冷凝管上口加入30.00mL的H2SO4—Ag2SO4溶液,混勻后加熱回流2h,充分反應。
③冷卻后加指示劑2d,用硫酸亞鐵銨溶液滴定多余重鉻酸鉀,至溶液由綠色變成紅褐色。
已知:Cr2O72—+14H++6Fe2+=6Fe3++2Cr3++7H2O
請你回答下列問題:
(1)儀器c的名稱: ;用儀器c吸取液體時,左手拿洗耳球,右手將儀器c插入溶液中吸取,當 時,立即用食指將管口堵住,將管尖離開液面,稍松食指使液面平穩下降,至凹液面最低處與標線相切,立即按緊管口。
(2)下列有關操作不正確的是 (用相應編號填寫)
A.用硫酸亞鐵銨溶液滴定時需上述儀器中的儀器b
B. 儀器c在使用時需要先用待取液進行潤洗,管尖殘留的液體一般不要吹出
C.加入數粒碎瓷片的作用是可以防止液體暴沸
D.上述操作步驟③中在滴定時判斷滴定終點的指示劑可以是甲基橙
E.加熱回流結束后,要用蒸餾水對冷凝管管壁進行沖洗
(3)在加熱回流過程中,可以用水浴作為恒溫加熱源嗎?同時請說明理由。
(4)下列因素對測定水樣中的COD能產生影響的有 (用相應編號填寫)
①硫酸的用量 ②反應裝置中的錐形瓶在反應前用蒸餾水洗滌
③重鉻酸鉀的用量 ④回流時間的長短
(5)實驗室配制重鉻酸鉀標準溶液的主要步驟及裝置如下所示: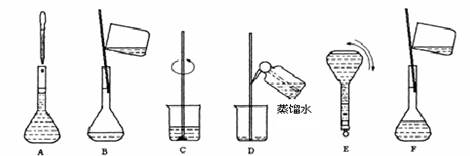
將上述實驗步驟A到F按實驗過程先后次序排列
(6)已知:重鉻酸鉀標準溶液的c(Cr2O72—)=0.0250mol·L—1,硫酸亞鐵銨溶液的c(Fe2+)=0.0100 mol·L—1,滴定終點時所消耗的硫酸亞鐵銨溶液的體積為12.00mL,則按上述實驗方法,測得的該水樣的化學需氧量CODCr(O2)= mg/L
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(13分)硫代硫酸鈉是一種重要的化工產品。某興趣小組擬制備硫代硫酸鈉晶體(Na2S2O3·5H2O)。
I.[查閱資料]
(1)Na2S2O3·5H2O是無色透明晶體,易溶于水。其稀溶液與BaCl2溶液混合無沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得產品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3難溶于水,可溶于稀HCl。
Ⅱ.[制備產品]
實驗裝置如圖所示(省略夾持裝置)
實驗步驟:
(1)檢查裝置氣密性,按圖示加入試劑。儀器a的名稱是____;E中的試劑是___(選填下列字母編號)。
A.稀H2SO4 B.NaOH溶液 C.飽和NaHSO3溶液
(2)先向C中燒瓶加入Na2S和Na2CO3混合溶液,再向A中燒瓶滴加濃H2SO4。
(3)待Na2S和Na2CO3完全消耗后,結束反應。過濾C中混合液,濾液經____(填寫操作名稱)、結晶、過濾、洗滌、干燥、得到產品。
Ⅲ.[探究與反思]
(1)為驗證產品中含有Na2SO3和Na2SO4,該小組設計了以下實驗方案,請將方案補充完整。(所需試劑從稀HNO3、稀H2SO4、稀HCl、蒸餾水中選擇)
取適量產品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____,若沉淀未完全溶解,并有刺激性氣味的氣體產生,則可確定產品中含有Na2SO3和Na2SO4。
(2)為減少裝置C中生成的Na2SO4的量,在不改變原有裝置的基礎上對原有實驗步驟(2)進行了改進,改進后的操作是_______。
(3)Na2S2O3·5H2O的溶解度隨溫度升高顯著增大,所得產品通過_____方法提純。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
(15分)高氯酸銅[Cu(ClO4)2·6H2O]易溶于水,120 ℃開始分解,常用于生產電極和作催化劑等。可由氯化銅通過下列反應制備:2CuCl2+2Na2CO3+H2O===Cu2(OH)2CO3↓+CO2↑+4NaCl;Cu2(OH)2CO3+4HClO4+9H2O===2Cu(ClO4)2·6H2O+CO2↑。HClO4是易揮發的發煙液體,溫度高于130 ℃易爆炸。下表列出相應金屬離子生成氫氧化物沉淀的pH(開始沉淀的pH按金屬離子濃度為1 mol·L-1):
| 金屬離子 | 開始沉淀 | 沉淀完全 |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
氨基甲酸銨是一種用途廣泛的化工原料。有關它的資料如下:①常溫下,在干燥的空氣中穩定,遇水或潮濕空氣則生成碳酸銨或碳酸氫銨;②熔點58℃,59℃則可分解成NH3和CO2氣體;③在密封管內加熱至120℃~140℃時失水生成尿素[CO(NH2)2];④酸性溶液中迅速分解;⑤合成氨基甲酸銨原理為:

(1)寫出氨基甲酸銨在密封管內加熱至120°C~140°C生成尿素的反應方程式:_______________
(2)儀器B名稱________;盛放藥品是: ________;
(3)合成氨基甲酸銨的反應在一定條件下能自發進行,該反應的反應熱ΔH_____0(填“>” “=”或“<”)
(4)有同學建議該CO2發生裝置直接改用“干冰”,你認為他的改進有何優點:(回答二點)
①________________;②________________
(5)該實驗裝置中有明顯導致實驗失敗的隱患有:(指出主要二處)
①________________;②________________
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
三氧化二鐵和氧化亞銅是紅色粉末,常作顏料。某校一化學實驗小組通過實驗來探究一紅色粉末是Fc2O3、Cu2O或二者的混合物。探究過程如下:
查閱資料知:Cu2O是一種堿性氧化物,溶于稀硫酸生成Cu和CuSO4,在空氣中加熱生成CuO。
提出假設:假設l:紅色粉末是Fc2O3 假設2:紅色粉末是Cu2O
假設3:紅色粉末是Fc2O3和Cu2O的混合物
設計實驗:取少量粉末放人足量稀硫酸中,在所得溶液中再滴加KSCN溶液。
(1)若假設1成立,則實驗現象是__ 。
(2)若滴入 KSCN溶液后溶液不變紅色,則證明原固體粉末中一定不含三氧化二鐵。你認為這種說法合理嗎?____。筒述你的理由 .
(3)若固體粉末完全溶解無固體存在,滴加KSCN溶液時溶液不變紅色,則證明原固體粉末是Fc2O3,和Cu2O的混合物,則其質量比為____,寫出其中發生的氧化還原反應的離子方程式 。探究延伸:經實驗分析,確定紅色粉末為Fc2O3,和Cu2O的混合物。
(4)實驗小組欲用加熱法測定Cu2O的質量分數。取ag固體粉末在空氣中充分加熱,待質量不再變化時,稱其質量為bg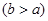 ,則混合物中Cu2O的質量分數為 。
,則混合物中Cu2O的質量分數為 。
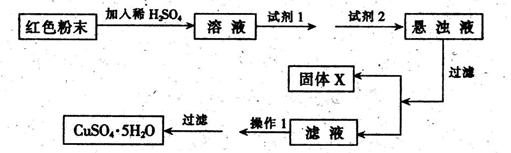
(5)實驗小組欲利用該紅色粉末制取較純凈的膽礬(CuSO4·5H2O)。經查閱資料得知在溶液中通過調節溶液的酸堿性而使Cu2+、Fe3+、Fe2+分別生成沉淀的pH如下:
| 物 質 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 開始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com