
【題目】設NA為阿伏加德羅常數值,下列說法正確的是
A. 在標準狀況下,4.48L水中含有的分子數目為0.2NA
B. 0.1mol![]() 離子含有的電子、中子數均為1.0NA
離子含有的電子、中子數均為1.0NA
C. 一定條件下,0.1mol![]() 與0.3mol
與0.3mol![]() 充分反應后的0.1NA個分子
充分反應后的0.1NA個分子
D. 總物質的量為0.1mol的CaO和![]() 混合物中,所含離子總數為0.2NA
混合物中,所含離子總數為0.2NA
科目:高中化學 來源: 題型:
【題目】下列關于化學與生產、生活的認識正確的是
A.禁止使用化學合成的化肥與農藥,促進綠色食品和有機食品的生產
B.用Ba(OH)2處理含Cu2+的廢水,可消除水中重金屬離子的污染
C.煤經過氣化和液化等物理變化可轉化為清潔燃料
D.![]() 和CO2生成可降解聚合物
和CO2生成可降解聚合物 ![]() ,反應符合綠色化學的原則
,反應符合綠色化學的原則
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自然界中時刻存在著氮的轉化。實現氮按照一定方向轉化一直是科學領域研究的重要課題,如圖為N2分子在催化劑的作用下發生的一系列轉化示意圖:
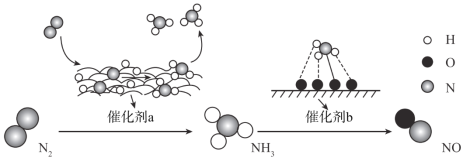
下列敘述正確的是
A.N2![]() NH3,NH3
NH3,NH3![]() NO均屬于氮的固定
NO均屬于氮的固定
B.催化劑a作用下氮原子發生了氧化反應
C.催化劑a、b表面均發生了極性共價鍵的斷裂
D.使用催化劑a、b均可以提高單位時間內生成物的產量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向mg鎂和鋁的混合物中加入適量的稀硫酸,恰好完全反應生成標準狀況下的氣體bL。向反應后的溶液中加入cmol/L氫氧化鉀溶液VmL,使金屬離子剛好沉淀完全,得到的沉淀質量為ng。再將得到的沉淀灼燒至質量不再改變為止,得到固體pg。則下列關系不正確的是
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A~I分別表示中學化學中常見的一種物質,它們之間相互關系如下圖所示(部分反應物、生成物沒有列出)。已知H為固態氧化物,F是紅褐色難溶于水的沉淀,且A、B、C、D、E、F六種物質中均含同一種元素。

請填寫下列空白:
(1)A、B、C、D、E、F六種物質中所含的同一種元素的名稱是________。
(2)反應①的化學方程式為_____________________________________
反應③的離子方程式為________________________
反應⑧的化學方程式為_____________________________________
(3)反應⑥過程中的現象是______________________________。
(4)1molI發生反應后生成的A高溫下與足量的水蒸氣反應,生成的氣體換算成標準狀況下占______L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫時,在H2CO3溶液中逐滴加入NaOH溶液,溶液中H2CO3、HCO3-和CO32-的物種分布分數![]() (X)=
(X)=![]() 與pH的關系如圖所示:
與pH的關系如圖所示:

下列說法正確的是
A. 反應HCO3-![]() H++CO32-的lgK=-6.4
H++CO32-的lgK=-6.4
B. pH═8的溶液中:c(Na+)>c(HCO3-)
C. NaHCO3溶液中滴入少量鹽酸至溶液顯中性:c(Na+)═c(Cl-)
D. 向pH=6.4的溶液中滴加NaOH溶液至pH=8,主要發生的離子反應:HCO3-+OH-═CO32-+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高鐵酸鉀(K2FeO4)是一種集氧化、吸附、絮凝于一體的新型多功能水處理劑。其生產工藝如下:
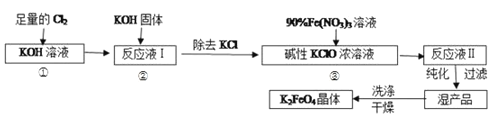
已知:①2KOH+Cl2=KCl+KClO+H2O(條件:溫度較低)
②6KOH+3Cl2=5KCl+KClO3+3H2O(條件:溫度較高)
③K2FeO4在水溶液中易水解:4FeO42-+10H2O![]() 4Fe(OH)3(膠體)+8OH-+3O2↑
4Fe(OH)3(膠體)+8OH-+3O2↑
回答下列問題:實驗室可利用如圖裝置完成流程①和②

(1)寫出工業上制取Cl2的化學方程式__;兩水槽中的水為___(填“熱水”或“冷水”)。
(2)反應一段時間后,停止通氯氣,再往儀器a中加入濃KOH溶液的目的是___;
A.為下一步反應提供堿性的環境
B.使KClO3轉化為 KClO
C.與溶液I中過量的Cl2繼續反應,生成更多的KClO
D.KOH固體溶解時會放出較多的熱量,有利于提高反應速率
(3)從溶液Ⅱ中分離出 K2FeO4后,還會有副產品KNO3、KCl,則反應③中發生的離子方程式為:___。
(4)用重結晶法提純粗產品:將粗產品先用KOH稀溶液溶解,再加入飽和的KOH溶液,冷卻結晶,過濾,用少量異丙醇洗滌,最后低溫真空干燥。
①洗滌粗品時選用異丙醇而不用水的理由是___。
②如何判斷 K2FeO4 晶體已經洗滌干凈__。
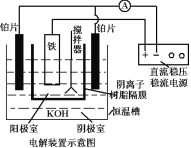
(5)從環境保護的角度看,制備K2FeO4較好的方法為電解法,其裝置如圖,電解過程中陽極的電極反應式為___。
(6)FeO42-在水溶液中的存在形態如圖所示。下列說法正確的是___。
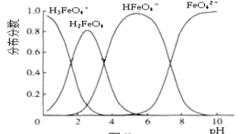
A.不論溶液的酸堿性如何變化,鐵元素都有4 種存在形態
B.向pH=10的這種溶液中加硫酸至pH=2,HFeO4-的分布分數逐漸增大
C.向pH=6 的這種溶液中加KOH溶液,發生反應的離子方程式為HFeO4-+OH-=FeO42- +H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a mol FeS與b mol FeO投入V L c mol·L-1的HNO3溶液(過量)中,充分反應,產生氣體為NO,則反應后溶液中NO3-的量為( )
A.62(a+b) gB.186(a+b) gC.![]() molD.
molD.![]() mol
mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學對教材中銅與濃硫酸的實驗作出如下改進。實驗裝置如圖所示(加熱和夾持裝置已略去)。
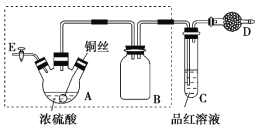
實驗步驟:
①組裝儀器,檢查裝置氣密性;
②加入試劑,關閉旋塞E,加熱A,觀察C中溶液顏色變化;
③將銅絲上提離開液面,停止加熱。
(1)檢查虛線框內裝置氣密性的方法是____________________________。
(2)裝置A的名稱是________,裝置B的作用是_________,裝置D中所盛藥品是__________。
(3)裝置A中發生反應的化學方程式為____________________________。
(4)實驗后,拆除裝置前,為避免有害氣體的泄漏,應當采取的操作是__________。
(5)實驗后裝置A中有白色固體產生,將裝置A中固液混合物緩慢轉移至盛有少量水的燒杯中,可觀察到的現象是______________;不可直接向裝置A中加水的原因是__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com