
【題目】某水溶液中可能含有Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-離子中的若干種。某同學取200 mL該溶液分成兩等份依次進行如下實驗:①向第一份溶液中加過量的NaOH溶液后加熱,充分反應后生成0.02 mol氣體(標況),無沉淀產生,同時得到溶液甲;②向溶液甲中通入過量的CO2,充分反應生成白色沉淀,沉淀經過濾、洗滌、灼燒至恒重得到1.02 g固體;③向第二份溶液中加入足量的BaCl2溶液,充分反應生成白色沉淀,沉淀用鹽酸充分洗滌、干燥,得到11.65 g固體。據此,該同學得到的結論正確的是( )
A. 實驗①中產生的氣體為氨氣,并可得原溶液中c(NH4+)=0.02 mol/L
B. 實驗③中的沉淀里一定有BaSO4,可能有Mg(OH)2
C. 若要確定原溶液中是否含有Cl-,無需另外再設計實驗驗證
D. 原溶液中一定含有Na+,且c(Na+)≥0.2 mol/L
【答案】D
【解析】
①第一份加過量NaOH溶液后加熱,收集到0.02mol氣體,該氣體為氨氣,溶液中一定含有NH4+,物質的量為0.02mol,其濃度為:c(NH4+)=![]()
無沉淀生成,則一定不含有Fe3+、Mg2+;
②向甲溶液中通入過量CO2,生成白色沉淀,該白色沉淀即為Al(OH)3,則原溶液中一定有Al3+,由于Al3+與CO32-不能大量共存,所以一定不含有CO32-,Al3+和過量的NaOH反應生成NaAlO2溶液,向溶液中通入過量CO2,生成白色沉淀,即為氫氧化鋁,氫氧化鋁沉淀經過濾、洗滌、灼燒后,得到1.02g固體即為氧化鋁,根據鋁元素守恒,得到鋁離子的物質的量是n(Al3+)=2×![]() =0.02mol;c(Al3+)=
=0.02mol;c(Al3+)=![]()
③第二份溶液中加足量BaCl2溶液后,生成白色沉淀,則一定含有SO42-離子,無Ba2+。沉淀經足量鹽酸洗滌、干燥后,得到11.65g固體即BaSO4的質量是11.65g,物質的量為:n(BaSO4)=11.65g÷233g/mol=0.05mol,根據S元素守恒,可知SO42-的物質的量是0.05mol,c(SO42-)=0.05mol÷0.1L=0.5mol/L。
綜上可知,一定含有的離子是:NH4+、Al3+、SO42-,其濃度分別是:0.2mol/L;0.2mol/L;0.5mol/L,一定不含Fe3+、Mg2+、Ba2+、SO42,不能確定是否存在氯離子。
A.根據以上分析可知,c(NH4+)=0.2 mol/L,A錯誤;
B.根據以上分析可知,③中的白色沉淀中一定有BaSO4,因溶液不存在鎂離子,則沒有生成氫氧化鎂,B錯誤;
C.由以上分析可知,不能確定氯離子是否存在,C錯誤;
D.任何溶液中都存在電荷守恒,NH4+、Al3+、SO42-,其濃度分別是:0.2mol/L;0.2mol/L;0.5mol/L,可知NH4+、Al3+的正電荷總量小于SO42-負電荷總量,依據溶液中陽離子帶的正電荷總數等于陰離子帶的負電荷總數,則一定有Na+存在,若無氯離子存在,則0.2×1+0.2×3+c(Na+)×1=0.5×2,解得c(Na+)=0.2mol/L,若含有氯離子,則c(Na+)>0.2mol/L,D正確;
故合理選項是D。


科目:高中化學 來源: 題型:
【題目】工業中很多重要的化工原料都來源于石油化工,如圖中的苯、丙烯、有機物 A 等,其中 A 的產量可以用來衡量一個國家的石油化工發展水平。請回答下列問題:

(1)A 的結構簡式為_________,丙烯酸中官能團的名稱為_________。
(2)寫出下列反應的反應類型①_________,②_________。
(3)下列說法正確的是_________。
A.硝基苯中混有濃 HNO3 和 H2SO4,將其倒入到 NaOH 溶液中,靜置,分液
B.除去乙酸乙酯中的乙酸,加 NaOH 溶液、分液
C.聚丙烯酸能夠使酸性高錳酸鉀溶液褪色
D.有機物 C 與丙烯酸屬于同系物
(4)寫出下列反應方程式:
丙烯酸生成聚丙烯酸:_________。
丙烯酸 + B →丙烯酸乙酯_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下將1 mol N2和3 mol H2置于密閉容器中發生反應N2+3H2![]() 2NH3(正反應是放熱反應)。下列關于該反應的說法正確的是
2NH3(正反應是放熱反應)。下列關于該反應的說法正確的是
A. 降低溫度可以加快反應速率
B. 達到化學反應限度時,生成2mol NH3
C. 向容器中再加入N2可以加快反應速率
D. 1mol N2 和3mol H2的總能量低于2mol NH3的總能量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】幾種無機物之間轉化關系如下圖(反應條件省略。部分產物省略)。下列推斷不正確的是
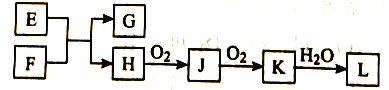
A. 若L為強堿,則E可能為NaCl溶液、F為鉀
B. 若L為強酸,則E可能為NaHS、F為HNO3
C. 若L為弱酸,則E可能為Mg、F為CO2
D. 若L為強酸,則E可能為NH4Cl、F為Ca(OH)2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】右圖是化學課外活動小組設計的用化學電源使LED燈發光的裝置示意圖。下列有關該裝置的說法正確的是( )

A. 銅片為負極,其附近的溶液變藍,溶液中有Cu2+產生
B. 如果將鋅片換成鐵片,電路中的電流方向將改變
C. 其能量轉化的形式主要是“化學能→電能→光能”
D. 如果將稀硫酸換成檸檬汁,LED燈將不會發光
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從有機反應R-H+Cl2R-Cl(液)+HCl(氣)制取副產品鹽酸的設想已成為現實。高一興趣小組設計了如圖模擬裝置圖,請回答下列問題:

(1)寫出實驗室制Cl2 的離子方程式_________。
(2)裝置B 中盛放的溶液是_________;作用是_________。
(3)裝置C有三種功能:①_________②_________③觀察氣泡的產生情況,便于控制兩種氣體的配比。
(4)玻璃管E中放在石棉碎塊上的碘化鉀的作用是________;導管末端“肚形”裝置的作用是________。
(5)從F 中分離出鹽酸的最佳方法是________;該套實驗裝置還存在的缺陷是________。
(6)內江六中高一另一興趣小組設計Cl2與NH3反應來驗證非金屬元素氯的氧化性強于和氮,請寫出Cl2與足量NH3反應的化學方程式_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. ![]() 互為同系物
互為同系物
B. ![]() 的系統命名是2-甲基-1-丙醇
的系統命名是2-甲基-1-丙醇
C. 相同壓強下的沸點:乙醇>乙二醇>丙烷
D. 室溫下,在水中的溶解度:甘油>苯酚> 1-氯丁烷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】解釋下列事實的方程式不正確的是
A. 次氯酸鈣溶液中通入過量二氧化硫:Ca2+ + 2ClO-+ H2O + SO2=CaSO3↓+ 2HClO
B. 硫酸型酸雨放置一段時間溶液的pH下降:2H2SO3+O2=2H2SO4
C. 純堿液可以清洗油污的原因:CO32+H2O![]() HCO3+OH
HCO3+OH
D. 向K2Cr2O7溶液中加入少量NaOH濃溶液,溶液由橙色變為黃色:Cr2O72—+H2O![]() 2CrO42—+2H+
2CrO42—+2H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用廢鍍鋅鐵皮制備磁性Fe3O4膠體粒子及副產物ZnSO4晶體的實驗流程如下:

已知:Zn及其化合物的性質與Al及其化合物的性質相似。
(1)用NaOH溶液處理廢鍍鋅鐵皮除溶解鋅外,另一個作用是_______________。為縮短用NaOH溶液處理廢鍍鋅鐵皮的時間,可采取的措施是_____________(答兩條)。
(2)加入適量H2O2溶液的主要作用是______________。溶液B中n(Fe2+):n(Fe3+)=______。
(3)在由溶液B制得Fe3O4膠體粒子的過程中,須緩慢滴加稀NaOH溶液并持續通入N2,持續通入N2的原因是_____________________。
(4)請補充完整下列由溶液A獲得副產品ZnSO4晶體的實驗步驟:
①向溶液A中通入CO2氣體,得到Zn (OH)2沉淀;
②______________、洗滌得到沉淀;
③______________;
④將溶液加熱濃縮、冷卻結晶、過濾、洗滌、干燥即可得到產品。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com