
【題目】以氨作為燃料的燃料電池,具有能量效率高的特點,另外氨氣含氫量高,易液化,方便運輸和貯存,是很好的氫源載體。NH3-O2燃料電池的結構如圖所示,下列說法正確的是( )
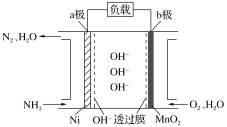
A.a極為電池的正極
B.負極的電極反應式為2NH3-6e-+6OH-=N2+6H2O
C.當生成1 mol N2時,電路中通過的電子的物質的量為3 mol
D.外電路的電流方向為從a極流向b極
科目:高中化學 來源: 題型:
【題目】(每空1分)Ⅰ.根據結構對有機物進行分類,有助于對其性質的掌握。
(1)下列有機物屬于芳香烴的是____________ (填字母),它與苯的關系是____________,寫出苯與溴發生反應的化學方程式 ___________________________________,
預測該芳香烴____________ (填“能”或“不能”)發生該類反應。
A.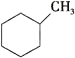 B.
B. C.
C.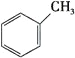
(2)下列有機物屬于羧酸類的是_________ (填字母)。
a.CH3CHO b.![]() c.
c. 
(3)下列有機物屬于糖類的是_________ (填字母)。
A.油脂 B.纖維素 C.蛋白質
Ⅱ.下列幾組物質中,互為同位素的有____________,互為同素異形體的有___________,互為同系物的有____________,互為同分異構體的有____________,屬于同種物質的有____________。
①O2和O3 ②35Cl和37Cl
③![]() 和
和![]() ④
④ 和
和
⑤CH3(CH2)2CH3和(CH3)2CHCH3 ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列為元素周期表中的一部分,用化學式或元素符號回答下列問題。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)10種元素中,化學性質最不活潑的是__________。
(2)①②⑤中,最高價氧化物的水化物,堿性最強的是__________。
(3)10種元素中最高價氧化物的水化物,酸性最強的是__________。
(4)元素⑦組成的含非極性鍵的分子的電子式:__________。
(5)區分①、②的碳酸正鹽的簡單實驗方法__________。
(6)①和⑤最高價氧化物對應的水化物相互反應的離子方程式為__________。
(7)③的單質與⑥的最高價氧化物反應的方程式:__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,下列反應中水蒸氣含量隨反應時間的變化趨勢符合題圖10 的是
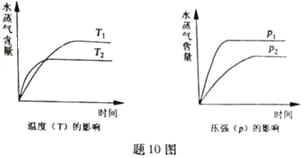
A. CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g);△H<0
CO(NH2)2(s)+H2O(g);△H<0
B. CO2(g)+H2(g)![]() CO(g)+H2O(g);△H>0
CO(g)+H2O(g);△H>0
C. CH3CH2OH (g)![]() CH2=CH2(g)+H2O(g);△H>0
CH2=CH2(g)+H2O(g);△H>0
D. 2C6H5CH2CH3(g)+O2(g)![]() 2 C6H5CH=CH2(g)+2H2O(g);△H<0
2 C6H5CH=CH2(g)+2H2O(g);△H<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】蘋果醋是一種由蘋果發酵而形成的具有解毒、降脂、減肥等明顯藥效的健康食品。蘋果酸(2-羥基丁二酸)是這種飲料的主要酸性物質,蘋果酸的結構簡式為![]() ,下列相關說法不正確的是( )
,下列相關說法不正確的是( )
A. 蘋果酸在一定條件下能發生酯化反應
B. 蘋果酸在一定條件下能發生催化氧化反應
C. 蘋果酸能與鈉、鎂等活潑金屬發生置換反應生成H2
D. 1mol蘋果醋與Na2CO3溶液反應一定消耗2molNa2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“酒是陳的香”,就是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用如圖所示的裝置制取乙酸乙酯。回答下列問題:
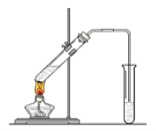
(1)寫出制取乙酸乙酯的化學反應方程式:_____________
(2)在大試管中配制一定比例的乙醇、乙酸和濃硫酸的混合液的順序是:________________。
(3)濃硫酸的作用是:①_________;②________。
(4)飽和碳酸鈉溶液的主要作用是________、____ 、______。
(5)裝置中通蒸氣的導管要插在飽和碳酸鈉溶液的液面上,不能插入溶液中,目的是___________。
(6)若要把制得的乙酸乙酯分離出來,應采用的實驗操作是__________。
(7)做此實驗時,有時還向盛乙酸和乙醇的試管里加入幾塊碎瓷片,其目的是_________。
(8)生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,就達到了該反應的限度,也即達到化學平衡狀態。下列描述能說明乙醇與乙酸的酯化反應已達到化學平衡狀態的有(填序號)________。
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
④正反應的速率與逆反應的速率相等
⑤混合物中各物質的濃度不再變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】滴定實驗是化學學科中重要的定量實驗。 請回答下列問題:
(1)酸堿中和滴定——用標準鹽酸滴定未知濃度的NaOH溶液,下列操作造成測定結果偏高的是________ (填選項字母)
A.滴定終點讀數時,俯視滴定管刻度,其他操作正確。
B.盛裝未知液的錐形瓶用蒸餾水洗過,未用未知液潤洗
C.酸式滴定管用蒸餾水洗凈后,未用標準鹽酸潤洗
D.滴定前,盛裝標準液的滴定管尖嘴有氣泡,滴定后氣泡消失
(2)氧化還原滴定——取一定量的草酸溶液置于錐形瓶中,加入適量稀硫酸,用濃度為0.1mol·L-1的高錳酸鉀溶液滴定,表格中記錄了實驗數據:
滴定次數 | 待測液體積 (mL) | 標準KMnO4溶液體積(mL) | |
滴定前讀數 | 滴定后讀數 | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 3.00 | 23.00 |
第三次 | 25.00 | 4.00 | 24.10 |
①滴定時發生的離子反應方程式___________,KMnO4溶液應裝在______________ (填“酸”或“堿”)式滴定管中,滴定終點時滴定現象是_________________________________。
②該草酸溶液的物質的量濃度為_____________。
(3)沉淀滴定――滴定劑和被滴定物的生成物比滴定劑與指示劑的生成物更難溶。參考下表中的數據,若用AgNO3滴定NaSCN溶液,可選用的指示劑是______(填選項字母)。
難溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
顏色 | 白 | 淺黃 | 白 | 磚紅 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表標出的是元素周期表的一部分元素,回答下列問題:
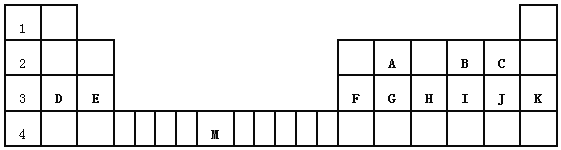
(1)除稀有氣體外第三周期中原子半徑最小的是_____(填元素符號)
(2)表中用字母標出的12種元素中,化學性質最不活潑的是_____(用元素符號表示,下同),金屬性最強的是___(用元素符號表示),屬于過渡元素的是___(該空格用表中的字母表示)
(3)元素B的單質含有的化學鍵為_____。(填“離子鍵’’、“極性共價鍵”、“非極性共價鍵”)
(4)D、F元素最高價氧化物對應水化物相互反應的離子方程式為_____________
(5)為比較元素A和G的非金屬性強弱,用圖所示裝置進行實驗(夾持儀器已略去,裝置氣密性良好)。溶液B應該選用_____溶液,作用是_________,能說明A和G非金屬性強弱的化學方程式是:________________________。
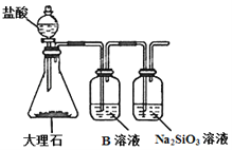
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,將緊緊纏繞不同金屬的鐵釘放入培養皿中,再加入含有適量酚酞和NaCl的瓊脂熱溶液,冷卻后形成瓊膠(離子在瓊膠內可以移動),下列敘述正確的是( )
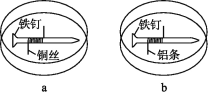
A. a中鐵釘發生反應:Fe-3e-=Fe3+
B. b中鐵釘上發生還原反應
C. a中銅絲上發生氧化反應:O2+2H2O+4e-=4OH-
D. b中鋁條附近有氣泡產生
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com