
【題目】【題目】烴A的質譜圖中,質荷比最大的數值為42。碳氫兩元素的質量比為6:1,其核磁共振氫譜有三個峰,峰的面積比為1:2:3。A與其他有機物之間的關系如下:
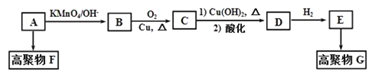
已知:CH2=CH2![]() HOCH2CH2OH,回答下列問題:
HOCH2CH2OH,回答下列問題:
(1)有機物B的分子式___________________________。
(2)高聚物F結構簡式為___________________。
(3)寫出C與新制的氫氧化銅反應的化學方程式___________________________。
(4)E在一定條件下可以相互反應生成一種六元環有機物H,H的結構簡式________.。
(5)寫出生成G的化學方程式_____________________________________________;
【答案】 )C3H8O2 ![]()
![]()
 n
n![]()
![]()
![]() +(n-1)H2O
+(n-1)H2O
【解析】試題分析:本題考查有機推斷,涉及有機物分子式和結構簡式的確定、有機物分子式和結構簡式的書寫、有機反應方程式的書寫。A的質譜圖中質荷比最大的數值為42,A的相對分子質量為42,烴A中n(C):n(H)=![]() :
: ![]() =1:2,A的實驗式為CH2,A的分子式為(CH2)x,14x=42,解得x=3,A的分子式為C3H6,A的核磁共振氫譜有三個峰且峰的面積比為1:2:3,A的結構簡式為CH2=CHCH3。A發生加聚反應生成的高聚物F的結構簡式為
=1:2,A的實驗式為CH2,A的分子式為(CH2)x,14x=42,解得x=3,A的分子式為C3H6,A的核磁共振氫譜有三個峰且峰的面積比為1:2:3,A的結構簡式為CH2=CHCH3。A發生加聚反應生成的高聚物F的結構簡式為![]() ;A→B發生題給已知的反應,B的結構簡式為
;A→B發生題給已知的反應,B的結構簡式為![]() ;B→C發生醇的催化氧化,C的結構簡式為
;B→C發生醇的催化氧化,C的結構簡式為![]() ;C與Cu(OH)2加熱時,C中-CHO被氧化,酸化后得到的D的結構簡式為
;C與Cu(OH)2加熱時,C中-CHO被氧化,酸化后得到的D的結構簡式為![]() ;D與H2發生加成反應生成E,E的結構簡式為
;D與H2發生加成反應生成E,E的結構簡式為![]() ;E中含羥基和羧基,E發生縮聚反應生成高聚物G,G的結構簡式為
;E中含羥基和羧基,E發生縮聚反應生成高聚物G,G的結構簡式為![]() 。
。
(1)B的結構簡式為![]() ,B的分子式為C3H8O2。
,B的分子式為C3H8O2。
(2)高聚物F的結構簡式為![]() 。
。
(3)C的結構簡式為![]() ,C與新制Cu(OH)2反應的化學方程式為
,C與新制Cu(OH)2反應的化學方程式為![]() +2Cu(OH)2+NaOH
+2Cu(OH)2+NaOH![]()
![]() +Cu2O↓+3H2O。
+Cu2O↓+3H2O。
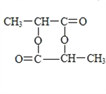
(4)E的結構簡式為![]() ,2分子E通過酯化反應形成六元環有機物H,H的結構簡式為
,2分子E通過酯化反應形成六元環有機物H,H的結構簡式為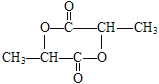 。
。
(5)G由E發生縮聚反應生成,生成G的化學方程式為n![]()
![]()
![]() +(n-1)H2O。
+(n-1)H2O。


 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案 欣語文化快樂暑假沈陽出版社系列答案
欣語文化快樂暑假沈陽出版社系列答案科目:高中化學 來源: 題型:
【題目】在常溫下,鐵與水并不起反應,但在高溫下,鐵與水蒸氣可發生反應。 應用下列裝置,在硬質玻璃管中放入還原鐵粉和石棉絨的混合物,加熱,并通入水蒸氣,就可以完成高溫下“鐵與水蒸氣的反應實驗”。
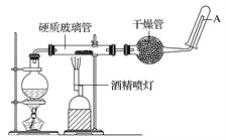
請回答該實驗中的問題。
(1)寫出該反應的反應方程式:__________________________________;并指明該氧化還原反應的還原劑是____________,氧化劑是______________。
(2)實驗前必須對整套裝置進行氣密性檢查,操作方法是_______________________________。
(3)圓底燒瓶中盛裝有水,該裝置受熱后的主要作用是____________________________;燒瓶底部放置了幾片碎瓷片,碎瓷片的作用是__________________。
(4)酒精燈和酒精噴燈點燃的順序是__________________________________,為什么?___________________________________________________________________。
(5)干燥管中盛裝的物質是________________________,作用是_______________________。
(6)試管中收集的氣體是__________,如果要在A處玻璃管處點燃該氣體,則必須對該氣體進行____________________,方法是________________________________。這一操作的目的是________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 原子及其離子的核外電子層數等于該元素所在的周期數
B. 零族元素與同周期ⅠA、ⅡA族陽離子具有相同的核外電子排布
C. 同周期的X、Y元素,且電負性X>Y,則第一電離能也是X>Y
D. 基態原子p能級上半充滿的元素一定位于p區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列A、B、C、D是中學常見的混合物分離或提純的基本裝置。請根據裝置圖回答下列問題:

(1)將A、B、C、D 填入適當的空格中。
①從碘水中提取碘_______;
②分離酒精與水的混合物_______;
③除去粗鹽中的泥沙________;
④與海水曬鹽原理相符的是_________;
(2)裝置A中儀器①的名稱是_________________,冷卻水是從______口進水(填“下”或“上”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某次實驗需用0.4molL﹣1 NaOH溶液480mL.配制方法如下:
(1)配制該溶液所需的儀器有:量筒、天平、藥匙、燒杯、玻璃棒、___、_____;
(2)用托盤天平準確稱量___________g 固體NaOH;
(3)若在配制過程中出現下列情況,將使所配制的NaOH溶液的濃度偏高的是_________,對實驗結果沒有影響的是_____________(填各選項的序號).
A.所用的NaOH中混有少量Na2O
B.用托盤天平稱量一定質量固體NaOH時,所用的小燒杯內壁不太干燥
C.配制溶液所用的容量瓶洗凈后沒有烘干
D.固體NaOH在燒杯中溶解后,立即將溶液轉移到容量瓶內并接著進行后續操作
E.轉移溶液后,未洗滌燒杯和玻璃棒就直接定容
F.最后確定NaOH溶液體積(定容)時,仰視容量瓶刻度線
G.定容搖勻后靜止,發現液面低于刻度線,再加蒸餾水至刻度線.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鋅被廣泛應用于醫藥領域和工農業生產。工業上由氧化鋅礦(主要成分為ZnO,另含ZnSiO3、FeCO3、CuO等)生產ZnSO47H2O的一種流程如圖:

(1)步驟Ⅰ的操作是____________。
(2)步驟Ⅰ加入稀硫酸進行酸浸時,需不斷通入高溫水蒸氣的目的是______________。
(3)步驟Ⅱ中,在pH約為5.1的濾液中加入高錳酸鉀,生成Fe(OH)3和MnO(OH)2兩種沉淀,該反應的離子方程式為____________________________________________。
(4)步驟Ⅲ中,加入鋅粉的作用是______________。
(5)已知硫酸鋅的溶解度與溫度之間的關系如下表:
溫度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
從硫酸鋅溶液中獲得硫酸鋅晶體的實驗操作為________________、冷卻結晶、過濾。烘干操作需在減壓低溫條件下進行,原因是_________________________________。
(6)取28.70 g ZnSO47H2O加熱至不同溫度,剩余固體的質量變化如圖所示。分析數據,680℃時所得固體的化學式為______。

a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按如圖所示裝置進行實驗,并回答下列問題。
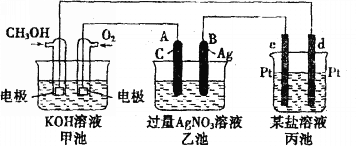
(1)甲池是_________池,通入CH3OH(甲醇)的電極作為_______極,電極反應式為________________________________________________。
(2)乙池是________池,A電極名稱為______極,電極反應式為_______________________,乙池中的總反應化學方程式為________________________________,溶液的pH________(填“增大”、“減小”或“不變”)。
(3)當甲池中消耗O2 0.56L(標準狀況下)時,理論上乙池中B極的質量增加_______g;此時丙裝置中_____________(填“c”或“d”)電極析出1.20g金屬,則丙裝置中的某鹽溶液可能是________(填序號)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com