
【題目】下列變化屬于化學變化的是
A.過濾B.蒸餾C.氧化D.分液
科目:高中化學 來源: 題型:
【題目】在通常條件下,NO2和SO2可以很容易發生反應生成NO和SO3 . 現將碳跟濃硫酸共熱產生的氣體X和碳跟濃硝酸共熱產生的氣體Y同時通入盛有足量氯化鋇溶液的洗氣瓶中(如圖裝置),下列有關說法正確的是( ) 
A.洗氣瓶中產生的沉淀是碳酸鋇
B.洗氣瓶中產生的沉淀是硫酸鋇
C.在Z導管出來的氣體中無二氧化碳
D.反應一段時間后洗氣瓶中溶液的酸性減弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實中能證明碳的非金屬性比硅強的是( ) ①往Na2SiO3溶液中通入CO2產生白色沉淀
②石墨是導體,晶體硅是半導體
③制玻璃過程中發生反應Na2CO3+SiO2 ![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
④CH4比SiH4穩定.
A.①④
B.②③
C.③④
D.①②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于烯烴、炔烴的敘述中,正確的是
A. 某物質的名稱為2-乙基-1-丁烯,它的結構簡式為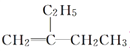
B. CH3—CH===CH—C≡C—CF3分子結構中6個碳原子可能都在一條直線上
C. 相同物質的量的乙炔與苯分別在足量的氧氣中完全燃燒,消耗氧氣的量相同
D. β—月桂烯的結構如圖![]() 所示,該物質與等物質的量溴發生加成反應的產物(不考慮立體異構)理論上最多有5種
所示,該物質與等物質的量溴發生加成反應的產物(不考慮立體異構)理論上最多有5種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某高分子化合物R的結構簡式如圖,下列有關R的說法正確的是

A. R的單體之一的分子式為C9H10O2
B. R完全水解后生成物均為小分子有機物
C. 堿性條件下,1molR完全水解消耗NaOH的物質的量為2mol
D. 通過加聚反應和縮聚反應可以生成R
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如表為元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列問題:
(1)Z元素在周期表中的位置為 .
(2)表中元素原子半徑最大的是(寫元素符號) .
(3)下列事實能說明Y元素的非金屬性比S元素的非金屬性強的是 .
a.Y單質與H2S溶液反應,溶液變渾濁
b.在氧化還原反應中,1molY單質比1molS得電子多
c.Y和S兩元素的簡單氫化物受熱分解,前者的分解溫度高
(4)X與Z兩元素的單質反應生成1mol X的最高價化合物,恢復至室溫,放熱687kJ.已知該化合物的熔、沸點分別為﹣69℃和58℃.寫出該反應的熱化學方程式: .
(5)碳與鎂生成的1mol化合物Q與水反應生成2mol Mg(OH)2和1mol烴,該烴分子中碳氫質量比為9:1,烴的電子式為 . Q與水反應的化學方程式為 .
(6)銅與一定濃度的硝酸和硫酸的混合酸反應,生成的鹽只有硫酸銅,同時生成的兩種氣體均由上表中兩種元素組成,氣體的相對分子質量都小于50,為防止污染,將產生的氣體完全轉化為最高價含氧酸鹽,消耗1L 2.2molL﹣1 NaOH溶液和1mol O2 , 則兩種氣體的分子式及物質的量分別為 , 生成硫酸銅物質的量為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】配制一定物質的量濃度的溶液是高中化學一個重要實驗.實驗室要配制1mol/L的稀硫酸溶液100mL,回答下列有關問題:
(1)配制時,必須用到下列儀器中的 . 
(2)配制時兩次用到玻璃棒,兩次的作用分別是和 .
(3)配制時,正確的操作順序是(用字母表示,每個字母只能用一次);A.用30mL水洗滌燒杯2~3次,洗滌液均注入容量瓶
B.用一定規格的量筒準確量取所需濃硫酸的體積,緩緩注入水中,用玻璃棒慢慢攪動,使其充分溶解
C.將已冷卻的溶液沿玻璃棒注入100mL的容量瓶中
D.將容量瓶蓋緊,搖勻
E.改用膠頭滴管加水,使溶液凹面恰好與刻度相切
F.繼續往容量瓶內小心加水,直到液面接近刻度1~2cm處
(4)配制過程中出現以下情況,使所配溶液濃度偏低的有(填代號).①沒有洗滌燒杯和玻璃棒.②如果加水超過了刻度線,取出水使液面恰好到刻度線.③容量瓶沒有干燥.④定容時仰視刻度線.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com