
【題目】向NaOH和Na2CO3混合溶液中滴加0.1mol·L-1稀鹽酸,CO2的生成量與加入鹽酸的體積(V)的關系如圖所示。下列判斷正確的是
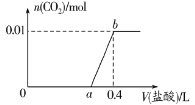
A.在0~a范圍內,只發生中和反應
B.a=0.2
C.ab段發生反應的離子方程式為CO32-+2H+=CO2↑+H2O
D.原混合溶液中NaOH與Na2CO3的物質的量之比為2:1
【答案】D
【解析】
對NaOH和Na2CO3混合配成的溶液,當滴加鹽酸時,先發生氫氧化鈉與鹽酸的中和反應,再發生碳酸鈉與鹽酸的反應生成碳酸氫鈉和氯化鈉,最后發生碳酸氫鈉與鹽酸反應才有二氧化碳氣體生成,利用物質的量的關系并結合圖象即可解答。
A.向NaOH和Na2CO3混合溶液中滴加鹽酸時,首先和NaOH反應生成水和氯化鈉,NaOH+HCl=NaCl+H2O,繼續滴加時,鹽酸和Na2CO3開始反應,首先發生HCl+Na2CO3=NaHCO3+NaCl,不放出氣體,繼續滴加時,發生反應:NaHCO3+HCl=NaCl+H2O+CO2↑;此時開始放出氣體,故A錯誤;
B.生成CO20.1mol,根據碳元素守恒,混合物中碳酸鈉的物質的量是0.01mol,所以兩步反應:HCl+Na2CO3=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑,分別消耗的鹽酸的量是0.01mol,消耗0.1molL-1稀鹽酸的體積分別是0.1L,所以a=0.3,故B錯誤;
C.ab段發生反應為:NaHCO3+HCl=NaCl+H2O+CO2↑,反應的離子方程式為:HCO3-+H+=H2O+CO2↑,故C錯誤;
D.oa段HCl+Na2CO3=NaHCO3+NaCl消耗0.1molL-1稀鹽酸的體積是0.1L,則發生中和反應時消耗0.1molL-1稀鹽酸的體積是0.2L,則混合溶液中NaOH物質的量是0.02mol,故原混合溶液中NaOH與Na2CO3的物質的量之比為2:1,故D正確;
故答案為D。


科目:高中化學 來源: 題型:
【題目】化學中常用圖像直觀地描述化學反應的進程或結果。下列圖像描述正確的是
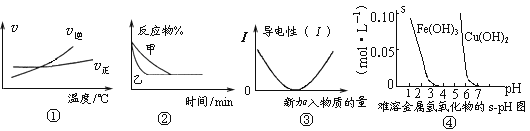
A. 根據圖①可判斷可逆反應“A2(g)+3B2(g)![]() 2AB3(g)”的ΔH>0
2AB3(g)”的ΔH>0
B. 圖②表示壓強對可逆反應2A(g)+2B(g)![]() 3C(g)+D(s)的影響,乙的壓強大
3C(g)+D(s)的影響,乙的壓強大
C. 圖③可表示乙酸溶液中通入氨氣至過量過程中溶液導電性的變化
D. 根據圖④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入適量CuO,至pH在4左右
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列方程式書寫錯誤的是
A. HCO3-的電離方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. Cu2+的水解方程式:Cu2++2H2O![]() Cu(OH)2+2H+
Cu(OH)2+2H+
C. NH4+的水解方程式:NH4++2H2O![]() NH3·H2O+H3O+
NH3·H2O+H3O+
D. CaCO3的電離方程式:CaCO3![]() Ca2++CO32-
Ca2++CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)羥基的電子式________;
(2)﹣C3H7結構簡式:________、________;
(3)CH3C(CH3)2CH2C(CH3)3系統命名為________該烴一氯取代物有________種。
(4)支鏈只有一個乙基且相對分子質量最小的烷烴的結構簡式________。
(5)鍵線式 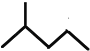 表示的分子式________。
表示的分子式________。
(6)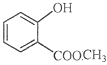 中含有的官能團的名稱為________。
中含有的官能團的名稱為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,將3molA氣體和1molB氣體混合于固定容積為2L的密閉容器中,發生反應:3A(g)+B(g)C(g)+2D(g)。2min末該反應達到平衡,生成D的物質的量隨時間的變化情況如圖所示。下列判斷正確的是( )
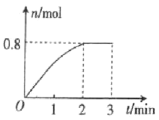
A.當混合氣體的密度不再改變時,該反應不一定達到平衡狀態
B.2min后,加壓會使正反應速率加快,逆反應速率變慢
C.從2min到3min過程中,氣體所占的壓強不會變化
D.反應過程中A和B的轉化率之比為3:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在不同溫度下,水溶液中c(H+)與c(OH-)關系如圖所示。下列說法不正確的是
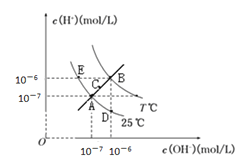
A. 圖中五點Kw間的關系:B>C>A=D=E
B. 在溫度不變的水中,加入適量的NH4Cl,無法實現從A點變到C點
C. D點對應的水溶液中,可能有NH4+、Fe3+、Cl-、NO3-大量同時存在
D. 若處在B點時,將pH =2的硫酸溶液與 pH = 10的KOH溶液等體積混合,所得溶液呈中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學電源在生產生活中有著廣泛的應用,請回答下列問題:
(1)根據構成原電池的本質判斷,下列方程式正確且能設計成原電池的是________。
A.KOH+HCl=KCl+H2O
B.Cu+Fe3+=Fe2++Cu2+
C.Na2O+H2O=2NaOH
D.Fe+H2SO4=FeSO4+H2
(2)為了探究化學反應中的能量變化,某同學設計了如下兩個實驗(圖Ⅰ、圖Ⅱ中除連接的銅棒不同外,其他均相同)。有關實驗現象,下列說法正確的是___________。

A.圖Ⅰ中溫度計的示數高于圖Ⅱ的示數
B.圖Ⅰ和圖Ⅱ中溫度計的示數相等,且均高于室溫
C.圖Ⅰ和圖Ⅱ的氣泡均產生于鋅棒表面
D.圖Ⅱ中產生氣體的速度比Ⅰ快
(3)將鋅片和銀片浸入稀硫酸中組成原電池,若該電池中兩電極的總質量為80,工作一段時間后,取出二者洗凈,干燥后稱重,總質量為54g,則產生氫氣的體積_____mL(標準狀況)
(4)將鋁片和鎂片放入氫氧化鈉溶液中,負極的電極反應式為:______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室利用如圖裝置進行中和熱的測定。回答下列問題:
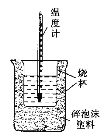
(1)該圖中有兩處未畫出,它們是____________、____________。
(2)在操作正確的前提下提高中和熱測定的準確性的關鍵是____________。
(3)如果用0.50 mol/L的鹽酸和氫氧化鈉固體進行實驗,則實驗中所測出的“中和熱”將____________(填“偏大”、“偏小”或“不變”);原因是____________。
(4)乙醇是未來內燃機的首選環保型液體燃料。2.0g乙醇完全燃燒生成液態水放出59.43 kJ的熱量,表示乙醇燃燒熱的熱化學方程式為____________________________。
(5)由N2O和NO反應生成N2和NO2的能量變化如圖所示,若生成1molN2,其△H=__________kJ·mol-1。
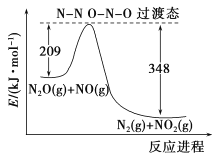
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】自來水是自然界中的淡水經過絮凝、沉淀、過濾、消毒等工藝處理后得到的。常用的自來水消毒劑有二氧化氯(ClO2)和高鐵酸鉀(K2FeO4)等。
(1)某研究小組用下圖裝置制備少量ClO2(夾持裝置已略去)。

資料:ClO2常溫下為易溶于水而不與水反應的氣體,水溶液呈深黃綠色,11℃時液化成紅棕色液體。以NaClO3和HCl的乙醇溶液為原料制備ClO2的反應為2NaClO3 + 4HCl= 2ClO2↑+ Cl2↑+ 2NaCl + 2H2O。
①冰水浴的作用是____________。
② NaOH溶液中發生的主要反應的離子方程式為________________。
(2)將ClO2水溶液滴加到KI溶液中,溶液變棕黃;再向其中加入適量CCl4,振蕩、靜置,觀察到____,證明ClO2具有氧化性。
(3)ClO2在殺菌消毒過程中會產生副產物亞氯酸鹽(ClO2-),需將其轉化為Cl-除去。下列試劑中,可將ClO2-轉化為Cl-的是_____________________(填字母序號)。
a. FeSO4 b. O3 c. KMnO4 d. SO2
(4)K2FeO4是一種新型、綠色的多功能凈水劑,集氧化、吸附、絮凝、沉淀、滅菌、消毒、脫色、除臭等性能為一體。實驗室制備K2FeO4的方法如下:在冰水浴中,向KClO和KOH的混合溶液中少量多次加入硝酸鐵,并不斷攪拌。
①上述制備K2FeO4反應的離子方程式為______________________。
②凈水過程中,K2FeO4起到吸附、絮凝作用的原理是____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com