
【題目】如果25℃時,Kw=1.0×10﹣14 , 100℃下Kw=1.0×10﹣12 . 下列說法錯誤的是( )
A.100℃下水的電離程度較大
B.前者的C(H+)較后者小
C.水的電離過程是一個放熱過程
D.溫度越高,Kw越大
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】H3PO2(次磷酸)是一種一元弱酸,H3PO2易溶于水且具有較強的還原性。
(1)H3PO2的結構式為。
(2)H3PO2在水溶液中的電離方程式為。
(3)不斷將新制的PH3通入攪拌的碘懸浮液中,直至碘的顏色消失,可得到次磷酸和氫碘酸,則該反應中氧化產物與還原產物的物質的量之比為。
(4)酸性條件下,H3PO2可將Cr2O72-還原為Cr3- , 其本身被氧化為磷酸,該反應的離子方程式為。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“材料”的發現和使用往往會極大地推動生產、生活的發展,一些材料的出現甚至具有里程碑式劃時代的意義。請回答下列問題:
Ⅰ、(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其組成__________________。
(2)漂白粉的有效成分是________(均填化學式)。硅是無機非金屬材料的主角,請你舉出一種含硅的材料名稱__________________。
(3)缺鐵性貧血患者應補充Fe2+,通常以硫酸亞鐵的形式補充,而硫酸鐵無這種藥效。當用硫酸亞鐵制成藥片時外表包有一層特殊的糖衣,這層糖衣的作用是________________________________。
(4)高分子材料可以分成無機高分子材料和有機高分子材料。[AlFe(OH)n Cl6-n]m屬于無機高分子材料,是一種新型高效凈水劑,它廣泛應用生活用水和工業污水的處理,其中鐵元素的化合價為________;
Ⅱ、高純二氧化硅可用來制造光纖。某稻殼灰的成分為:
組 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
質量分數 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
通過如下流程可由稻殼灰制備較純凈的二氧化硅。
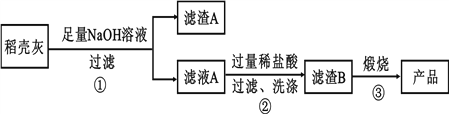
請回答下列問題:
(1)根據氧化物的性質進行分類,稻殼灰中屬于兩性氧化物的是____________。
(2)步驟①中涉及SiO2的離子反應方程式為________________________________。
(3)濾渣A的成分有______________(填化學式)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數,則下列說法正確的是
A. 5.6克鐵與足量的氯氣點燃充分反應,失電子數為0.2 NA
B. 2.3克金屬鈉常溫下在空氣中充分反應和在空氣中點燃失電子數之比為1:2
C. 7.8克過氧化鈉與足量水反應轉移電子數為0.2NA
D. 標況下22.4L純凈的NO2溶于水轉移電子數為2/3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下述實驗中均有紅棕色氣體產生,對比分析所得結論不正確的是( )
|
|
|
① | ② | ③ |
A. 由①中的紅棕色氣體,推斷產生的氣體一定是混合氣體
B. 紅棕色氣體不能表明②中木炭與濃硝酸產生了反應
C. 由③說明濃硝酸具有揮發性,生成的紅棕色氣體為還原產物
D. ③的氣體產物中檢測出CO2,由此說明木炭一定與濃硝酸發生了反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某鐵紅涂料中添加有CuO或FeO中的一種,為探究添加物的成分設計如下實驗方案。
(1)請寫出實驗步驟、預期現象,對應的離子方程式。
(限選試劑:鐵粉、3mol/LH2SO4、0.1mol/L酸性KMnO4溶液、10%H2O2、KSCN溶液)
① , ② , , ③ ,
④操作步驟③中反應的離子方程式為。
(2)經分析該鐵紅涂料中有FeO,為測定鐵紅中鐵的質量分數,興趣小組的同學稱量11.6g該鐵紅涂料進行了如下實驗。
已知:氣體由草酸晶體受熱分解得到:H2C2O4·2H2O ![]() CO2↑+CO↑+3H2O。且除鐵紅外所用試劑均過量。
CO2↑+CO↑+3H2O。且除鐵紅外所用試劑均過量。
①裝置A、B中的試劑依次是、。
②氣體通入后,接下來的操作是 , 然后對C裝置加熱。
③實驗前后稱得D裝置增重8.8g,則此鐵紅中鐵的質量分數是。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定質量的Mg-Al合金投入100mL一定物質的量濃度的某HCl溶液中,充分反應。向反應后的溶液中逐滴加入一定物質的量濃度的NaOH溶液,生成沉淀的質量與所加NaOH溶液的體積關系如下圖。回答下列問題:
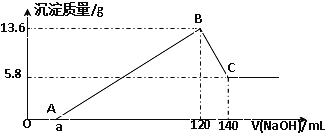
(1)寫出OA段和BC段反應的離子方程式:
OA:________________________________ ; BC:_____________________________;
(2)原Mg-Al合金的質量是_____________。
(3)原HCl溶液的物質的量濃度是________________。
(4)所加NaOH溶液的物質的量濃度是____________。
(5)a的值是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液可能含有H+、K+、Mg2+、Al3+、Fe3+、Cl-、SO![]() 、CO
、CO![]()
(1)取該溶液20 mL,加入NaOH溶液,只產生白色沉淀,且產生的沉淀量與加入1.0 mol·L-1NaOH溶液的體積之間的關系如圖所示;水樣中一定含有的陽離子是___________,其物質的量之比是_________,并可排除______的存在。
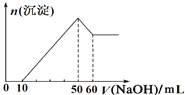
(2)另取該溶液20 mL,加足量BaCl2溶液,得到4.66 g不溶于鹽酸的沉淀。試根據上述實驗推測Cl-是否存在?___ (填“是”或“否”)。
(3)無法確定的離子是______,可通過____________方法確定其是否存在。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關自然資源的開發利用的說法不正確的是( )
A. 證明海帶中存在碘元素的實驗中,需將干海帶洗凈后置于坩堝中灼燒
B. 以Cu2S為原料可采用火法煉銅冶煉出金屬Cu
C. 海水曬鹽后的母液中,直接加入CCl4可萃取Br2單質
D. 資料表明,藍銅礦的主要成分為2CuCO3·Cu(OH)2,當它與焦炭一起高溫加熱時,可以生成銅、二氧化碳和水。該反應的化學方程式為:2[2CuCO3·Cu(OH)2]+3C![]() 6Cu+7CO2↑+2H2O
6Cu+7CO2↑+2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com