
(1)已知:2Al(s)+O2(g)=Al2O3(s) △H=-1644.3kJ·mol-1
2Fe(s)+O2(g)=Fe2O3(s) △H=-815.88kJ·mol-1
寫出鋁粉與氧化鐵粉末發生鋁熱反應的熱化學方程式 。
(2)高鐵酸鉀(K2FeO4)在水中的反應為4FeO42-+10H2O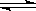 4Fe(OH)3+8OH-+3O2。圖1是25℃時K2FeO4在不同pH溶液中濃度的變化情況,圖2是K2FeO4在不同溫度時溶液濃度的變化情況。
4Fe(OH)3+8OH-+3O2。圖1是25℃時K2FeO4在不同pH溶液中濃度的變化情況,圖2是K2FeO4在不同溫度時溶液濃度的變化情況。
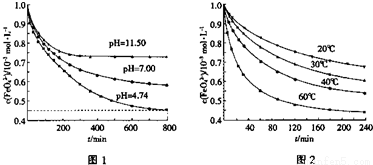
①pH=4.74時,反應從開始到800min時平均反應速率v(OH-)= 。
②圖1在800min后,三種溶液中的c(FeO42-)均不再改變。隨著pH的變大,此反應的平衡常數K (填“變大”、“變小”或“不變”)。
③圖2在240min后,四種溶液中FeO42-的濃度不再變化,下列說法正確的是
a.上述反應的△H>0 b.升高溫度,該反應pH減小
c.溫度越高,反應速率越慢 d.加入鹽酸,FeO42-的濃度減小
④FeO42-在水溶液中的存在形態如圖3所示。下列說法正確的是

A.不論溶液酸堿性如何變化,鐵元素都有4種存在形態
B.向pH=10的這種溶液中加硫酸至pH=2,HFeO4-的分布分數逐漸變大
C.向pH=6的這種溶液中加KOH溶液,發生反應的離子方程式為:HFeO4-+OH-=FeO42-+H2O
⑤高鐵酸鉀(K2FeO4)具有極強的氧化性,是一種優良的水處理劑。
已知:4FeO42-+10H2O=4Fe(OH)3+8OH-+3O2,K2FeO4在處理水的過程中所起的作用是 。
(3)常溫常壓下,飽和氯水中氯氣總濃度約為0.09mol/L,且存在可逆反應:Cl2 + H2O  HCl + HClO,實驗測得約有三分之一的氯氣與水發生了反應。反應Cl2+H2O
HCl + HClO,實驗測得約有三分之一的氯氣與水發生了反應。反應Cl2+H2O HCl+HClO的平衡常數為 。
HCl+HClO的平衡常數為 。
科目:高中化學 來源:2017屆江西省高三上學期第一次段考化學卷(解析版) 題型:選擇題
向下列溶液中通入氯氣,現象和結論描述正確的是
A.品紅溶液:紅色褪去,加熱該褪色溶液,仍無色;氯氣具有漂白性
B.紫色石蕊溶液:先變紅,后褪色;氯氣與水反應生成鹽酸和次氯酸
C.含酚酞的氫氧化鈉溶液:紅色褪去;氯氣只作氧化劑
D.硫化鈉溶液:溶液變渾濁;氯氣只作還原劑
查看答案和解析>>
科目:高中化學 來源:2016-2017學年吉林省高二上學期9月月考化學試卷(解析版) 題型:選擇題
下列敘述正確的是( )
A.反應AlCl3+4NaOH===NaAlO2+3NaCl+2H2O,可以設計成原電池
B.Zn和稀硫酸反應時,加入少量CuSO4溶液能加快產生H2的速率
C.把Fe片和Cu片放入稀硫酸中,并用導線把二者相連,觀察到Cu片上產生大量氣泡,說明Cu與H2SO4能發生反應而Fe被鈍化
D.Zn-Cu原電池工作過程中,溶液中H+向負極作定向移動
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省咸寧市高二上學期第一次月考化學試卷(解析版) 題型:選擇題
通過以下反應均可獲取H2。下列有關說法正確的是( )
①太陽光催化分解水制氫:2H2O(l)=2H2(g)+O2(g) △H1=+571.6 kJ.mol-1
②焦炭與水反應制氫:C(s)+H2O(g)=CO(g)+H2(g) △H2=+131.3 kJ.Mol-1
③甲烷與水反應制氫:CH4(g)+H2O(g)=CO(g)+3H2(g) △H3=+206.1 kJ.mol-l
A.反應①中電能轉化為化學能
B.反應②為放熱反應
C.反應③使用催化劑,△H3減小
D.反應CH4(g)=C(s)+2H2(g)的△H=+74.8 kJ.mol-1
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省咸寧市高二上學期第一次月考化學試卷(解析版) 題型:選擇題
一定溫度下,10 mL 0.4 mol/LH2O2溶液發生催化分解。不同時刻測得生成O2的體積(已折算為標準狀況)如下表:
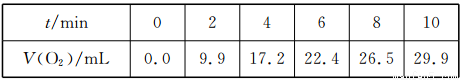
下列敘述錯誤的是(溶液體積變化忽略不計)( )
A.反應至6 min時,c(H2O2)=0.20mol/L
B.反應至6 min時,H2O2分解了40%
C.0~6 min的平均反應速率:v(H2O2)≈3.3×10-2 mol.L-1.min-l
D.6~10 min的平均反應速率:可(H2O2) <3.3×10-2 mol.L-1.min-l
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次段考化學卷(解析版) 題型:選擇題
在一個密閉容器(W)中,進行如下兩個可逆反應:
①A(g)+2B(g) 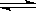 3C(g)+D(s) △H1>0 ②xM(g)+N(g)
3C(g)+D(s) △H1>0 ②xM(g)+N(g)  3Q(g) △H2。反應①中各物質與反應②中各物質均不發生反應。在某容器里只進行反應②,M的轉化率與溫度、壓強的關系如圖所示。下列對W容器中進行的反應推斷合理的是
3Q(g) △H2。反應①中各物質與反應②中各物質均不發生反應。在某容器里只進行反應②,M的轉化率與溫度、壓強的關系如圖所示。下列對W容器中進行的反應推斷合理的是
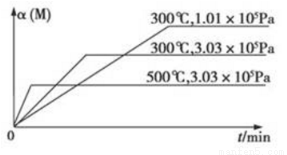
A.反應①一定是自發反應,反應②一定是非自發反應
B.若容器內溫度保持不變,則 v正(B): v逆(C)=2:3
C.若恒壓條件下,充入N,則C的物質的量減小
D.升高溫度,兩個反應的平衡常數都減小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次段考化學卷(解析版) 題型:選擇題
某密閉容器中充入等物質的量的氣體A和B,一定溫度下發生如下反應:A(g)+xB(g)  2C(g)。達到平衡后,只改變反應的一個條件,測得容器中物質的濃度,反應速率隨時間的變化關系如圖所示。下列說法中正確的是
2C(g)。達到平衡后,只改變反應的一個條件,測得容器中物質的濃度,反應速率隨時間的變化關系如圖所示。下列說法中正確的是
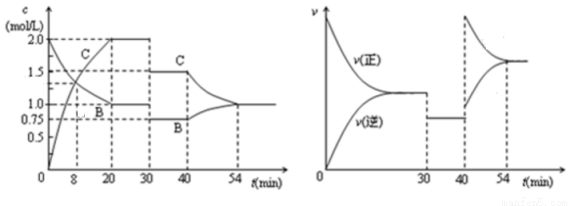
A.8min時表示正反應速率等于逆反應速率
B.前20minA的反應速率為0.05mol/(L·min)
C.反應方程式中的x=1,30min時表示增大壓強
D.40min時改變的條件是升高溫度,且正反應為吸熱反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年北大附中河南分校高二上第一次月考化學卷(解析版) 題型:選擇題
下列說法正確的是( )
①參加反應的物質本身的性質是影響化學反應速率的主要因素 ②光是影響某些化學反應速率的外界條件之一 ③決定化學反應速率的主要因素是濃度 ④不管什么反應,增大濃度、加熱、加壓、使用催化劑都可以加快反應速率
A.①② B.②③ C.③ ④ D.①④
④ D.①④
查看答案和解析>>
科目:高中化學 來源:2016-2017年河北定州中學承智班高二上第一次月考化學卷(解析版) 題型:選擇題
化學與科學、技術、社會、環境密切相關。下列有關說法中不正確的是
A.煤經過氣化和液化等物理變化,可變為清潔能源
B.服用鉻含量超標的藥用膠囊會對人體健康造成危害
C.竹炭具有超強的吸附能力,能吸附新裝修房屋內的有害氣體
D.采用催化轉換技術將汽車尾氣中的NOx和CO轉化為無毒氣體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com