
【題目】下列物質使用(括號內為用途)不正確的是( )
A.碳酸鈉(發酵粉)B.Ca(ClO)2(消毒劑)
C.Al2O3(耐火材料)D.過氧化鈉(供氧劑)
科目:高中化學 來源: 題型:
【題目】在一定條件下,PbO2與Cr3+反應,產物是Cr2O72﹣和Pb2+ , 則與1mol Cr3+反應所需PbO2的物質的量為( )
A.3.0mol
B.1.5mol
C.1.0mol
D.0.75mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值,下列判斷正確的是
A. 通常狀況下,48gO2和O3的混合氣體中含有的氧原子數目約為3NA
B. 標準狀況下,4.48 L甲醛(HCHO)含有的分子數目約為2NA
C. 1L1mol·L-1CH3CH2OH溶液中含有的氧原子數目約為NA
D. 1 molMg中含有的電子數目約為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是一種在生產和生活中應用廣泛的金屬元素。己知:
反應Ⅰ:Fe2O3(s)+ 3H2(g)=2Fe(s)+3H2O(g) ΔH1= +89 .6kJ /mol
反應Ⅱ:4Fe2O3(s)+Fe(s)=3Fe3O4(s) ΔH2=+2833.4kJ/mol
反應Ⅲ:Fe(s)+2HCl(g)![]() FeCl2(l)+H2(g) ΔH3
FeCl2(l)+H2(g) ΔH3
(1)反應Ⅰ的平衡常數表達式K=______________,該反應在高溫下進行,最易生成的副產物是________________ (填化學式)。
(2)溫度為T1時,恒容密閉容器中發生反應Ⅲ,反應時間與體系壓強關系如圖a所示,體系溫度與HCl轉化率關系如圖b所示。
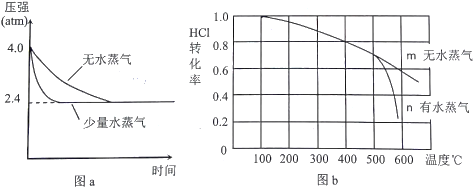
①分析圖a,容器內通入少量水蒸氣的作用是___________________。
②分析圖b,ΔH3________0(填“>”、“<”或“=”),結合圖a分析,T1=___________℃。
③分析圖b,高于500℃后,曲線n發生的副反應熱化學方程式為________________________________, 曲線n中HCl轉化率明顯降低的原因是____________________________________。
(3)①CaFeO4可制作半導體材料,向1L的高鐵酸鈉(Na2FeO4)溶液中加入0.0056g生石灰開始生成CaFeO4沉淀,原高鐵酸鈉溶液的物質的量濃度為________mol/L。已知Ksp(CaFeO4)=4.54×10-9,溶液體積變化忽略不計。
②用K2FeO4代替MnO2制備的堿性干電池(KOH做電解液)具有能量密度大、壽命長、無污染等優點,正極反應生成Fe2O3,寫出正極的電極反應式______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列裝置或操作能達到實驗目的的是

A. 用裝置甲制取一氯甲烷
B. 用裝置乙在實驗室制取氨氣
C. 用裝置丙萃取溴水中的溴
D. 用裝置丁在實驗室制蒸餾水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面所寫的有機反應方程式及其類型都正確的是
A.  取代反應
取代反應
B. 2CH3CHO+ O2 → 2CH3COOH 氧化反應
C. CH2=CH2 + Br2 → CH3CHBr2 加成反應
D. HCOOH + CH3CH2OH ![]() HCOOCH3CH2+ H2O 取代反應
HCOOCH3CH2+ H2O 取代反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種含鋁、鋰、鈷的新型電子材料,生產中產生的廢料數量可觀,廢料中的鋁以金屬鋁箔的形式存在;鈷以鈷以Co2O3CoO的形式存在,吸附在鋁箔的單面或雙面,鋰混雜于其中.從該廢料中回收(CoO) 的工藝流程如圖: 
(1)過程I中采用NaOH溶液溶出廢料中的Al,反應的離子方程式為 .
(2)過程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出鈷.則浸出鈷的化學反應方程式為(產物中只有一種酸根) . 在實驗室模擬工業生產時,也可用鹽酸浸出鈷,但實際工業生產中不用鹽酸,請從反應原理分析不用鹽酸浸出鈷的主要原因 .
(3)過程Ⅲ得到鋰鋁渣的主要成分是LiF和Al(OH)3 , 碳酸鈉溶液在產生Al(OH)3時起重要作用,請寫出該反應的離子方程式 .
(4)碳酸鈉溶液在過程III和IV中所起作用有所不同,請寫出在過程IV中起的作用是 .
(5)在Na2CO3溶液中存在多種粒子,下列各粒子濃度關系正確的是(填序號).
A.c(Na+)=2c(CO32﹣)
B.c(Na+)>c(CO32﹣)>c(HCO3﹣)
C.c(OH﹣)>c(HCO3﹣)>c(H+)
D.c(OH﹣)﹣c(H+)=c(HCO3﹣)+2c(H2CO3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知25℃時,AgI飽和溶液中c(Ag+)為1.22×10﹣8 mol/L,AgCl的飽和溶液中c(Ag+)為1.25×10﹣5 mol/L.若在10mL含有KCl和KI各為0.01mol/L的溶液中,加入16mL 0.01mol/L AgNO3溶液,這時溶液中所含溶質的離子濃度大小關系正確的是( )
A.c(K+)>c(NO3﹣)>c(Ag+)>c(Cl﹣)>c(I﹣)
B.c(K+)>c(NO3﹣)>c(Cl﹣)>c(Ag+)>c(I﹣)
C.c(K+)>c(NO3﹣)>c(Ag+)=c(Cl﹣)+c(I﹣)
D.c(NO3﹣)>c(K+)>c(Ag+)>c(Cl﹣)>c(I﹣)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于能量變化的說法正確的是
A.冰融化成水放出熱量
B.化學鍵斷裂過程一定放出能量
C.生成物的總能量一定低于反應物的總能量
D.化學鍵的斷裂和形成是化學反應中能量變化的主要原因
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com