
 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源:2015-2016學年寧夏育才中學高一下期中化學試卷(解析版) 題型:選擇題
工業制硫酸中的一步重要反應是SO2在400-500℃下的催化氧化:2SO2+O2  2SO3,這是一個正反應放熱的可逆反應。如果反應在密閉容器中進行,下述有關說法中錯誤的是 ( )
2SO3,這是一個正反應放熱的可逆反應。如果反應在密閉容器中進行,下述有關說法中錯誤的是 ( )
A.使用催化劑是為了加快反應速率,提高生產效率
B.在上述條件下,SO2不可能100%轉化為SO3
C.為了提高SO2的轉化率,應適當提高O2的濃度
D.達到平衡時,SO2的濃度與SO3的濃度相等
查看答案和解析>>
科目:高中化學 來源:2016屆陜西省高三第六次適應性考試理綜化學試卷(解析版) 題型:選擇題
熔融碳酸鹽燃料電池是一種高溫電池,具有效率高、噪音低、無污染、燃料多樣化、余熱利用價值高和電池構造材料價廉等諸多優點,是未來的綠色電站。某種熔融碳酸鹽燃料電池以Li2CO3、K2CO3為電解質、以CH4為燃料時,該電池工作原理見下圖。下列說法正確的是
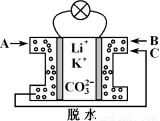
A.Li+、K+移向左側電極
B.外電路中電子由右側電極移向左側電極
C.通入1 mol氣體A時,左側電極上生成5 mol CO2
D.相同條件下通入氣體B與氣體C的體積比為2∶1
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三第八次模擬理綜化學試卷(解析版) 題型:選擇題
化學與人類社會的生產、生活有著密切聯系。下列敘述中正確的是( )
A. “殲﹣20”飛機上大量使用的碳纖維是一種新型的有機高分子材料
B.“神舟十號”宇宙飛船返回艙外表面主要是導電導熱良好的新型金屬材料鈦合金
C.“天宮一號”是中國第一個空間實驗室,其太陽能電池板的主要材料是硅
D.“遼寧艦”上用于艦載機降落攔阻索的特種鋼纜,屬于新型無機非金屬材料
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三第二次模擬理綜化學試卷(解析版) 題型:選擇題
在常溫下,用0.1000 mol/L的鹽酸滴定25 mL 0.1000 mol/LNa2CO3 溶液,所得滴定曲線如下圖所示。下列微粒濃度間的關系不正確的是
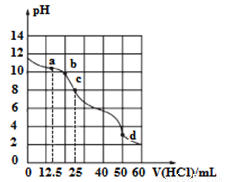
A.a點:c( HCO3-)>c(Cl-)>c(CO32-)
B.b點:c(Na+)+c(H+)=c(Cl-)+c(HCO3-)+c(CO32-)+c(OH-)
C.c點:c(OH-)+c(CO32-)=c(H+)+c(H2CO3)
D.d點:c(Cl-)=c(Na+)
查看答案和解析>>
科目:高中化學 來源:2016屆江西南昌二中、臨川一中等高三4月聯考二理綜化學試卷(解析版) 題型:實驗題
銀氨溶液可用于檢測CO氣體,實驗室研究的裝置如圖:
| 已知:①銀氨溶液的化學式為: Ag(NH3)2OH ②反應結束后試管C底部有黑色 沉淀生成, ③分離出上層清液和底部黑色 固體備用。 |
(1)甲酸(HCOOH)遇濃硫酸分解生成CO和H2O,該反應體現濃硫酸的 性。
(2)裝置A中軟管的作用是 。
(3)為驗證上層清液中產物的成分,進行如下實驗:
a.測得上層清液pH為10。
b.向上層清液中滴加幾滴Ba(OH)2溶液,發現有白色渾濁出現,同時產生能使濕潤紅色石蕊試紙變藍的氣體。
c.取新制的銀氨溶液滴加幾滴Ba(OH)2溶液,無明顯現象。
①實驗c的目的是 。
②根據上述實驗現象判斷,上層清液中產物成分為 (填化學式)。
(4)設計實驗證明黑色固體的成分是Ag:
可供選擇的試劑有:濃硫酸、濃硝酸、NaOH溶液、NaCl溶液。
取少量上述黑色固體,用蒸餾水洗凈, ,說明黑色固體是Ag單質。(補充必要的實驗內容及實驗現象)
(5)從銀氨溶液中回收銀的方法是:向銀氨溶液中加入過量鹽酸,過濾,向沉淀AgCl中加入羥氨(NH2OH),充分反應后可得銀,羥氨被氧化為N2。
①寫出生成AgCl沉淀的離子反應 。
②若該反應中消耗3.3 g羥氨,理論上可得銀的質量為 g。
查看答案和解析>>
科目:高中化學 來源:2016屆江西南昌二中、臨川一中等高三4月聯考二理綜化學試卷(解析版) 題型:選擇題
有機物X、Y、M(已知M為乙酸)的轉化關系為:淀粉→X→Y 乙酸乙酯,下列說法不正確的是
乙酸乙酯,下列說法不正確的是
A.X可用新制的氫氧化銅懸濁液檢驗
B.實驗室由Y和M制取乙酸乙酯時可用飽和Na2CO3溶液來提純
C.乙酸乙酯的同分異構體中含有“-COO-”結構的還有3種
D.Y分子中含有3種不同環境的氫,峰面積比為3:2:1
查看答案和解析>>
科目:高中化學 來源:2016屆陜西省高三第五次適應性考試理綜化學試卷(解析版) 題型:實驗題
鈷(Co)及其化合物在工業上有廣泛應用。為從某工業廢料中回收鈷,某學生設計流程如下(廢料中含有Al、Li、Co2O3和Fe2O3等物質)。
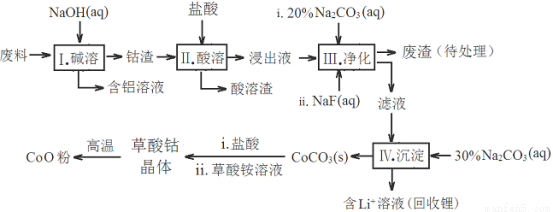
已知:①物質溶解性:LiF難溶于水,Li2CO3微溶于水;
②部分金屬離子形成氫氧化物沉淀的pH見下表:
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(開始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
請回答:
(1)步驟Ⅰ中得到含鋁溶液的反應的離子方程式是____________________________。
(2)寫出步驟Ⅱ中Co2O3與鹽酸反應的離子方程式_________________________
(3)步驟Ⅲ中Na2CO3溶液的作用是調節溶液的pH,應使溶液的pH不超過__________。廢渣中的成分有______________________。
(4)NaF與溶液中的Li+形成LiF沉淀,此反應對步驟Ⅳ所起的作用是___________。
(5)在空氣中加熱CoC2O4固體,經測定,210~290℃的過程中只產生CO2和一種二化合物,該化合物中鈷元素的質量分數為73.44%。此過程發生反應的化學方程式是_________________。
(6)某鋰離子電池的總反應為C+LiCoO2 LixC+Li1-xCoO2,LixC中Li的化合價為______價,該鋰離子電池充電時陽極的電極反應式為______________。
LixC+Li1-xCoO2,LixC中Li的化合價為______價,該鋰離子電池充電時陽極的電極反應式為______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com