
【題目】燒硫酸鋁銨晶體,發生的主要反應為4[NH4Al(SO4)2·12H2O] ![]() 2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。將產生的氣體通過下圖所示的裝置(假設試劑均過量)。下列說法正確的是
2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。將產生的氣體通過下圖所示的裝置(假設試劑均過量)。下列說法正確的是

A. 反應中硫元素既體現氧化性又體現還原性
B. 裝置Ⅰ中可以觀察到出現白色沉淀,其主要成分是BaSO4和BaSO3
C. 裝置Ⅱ中可以觀察到高錳酸鉀紫色褪去
D. 將裝置Ⅰ、Ⅱ順序交換,仍能觀察到相同的現象
【答案】C
【解析】
由硫酸鋁銨晶體分解的方程式可知,生成二氧化硫時硫元素從+6價降到+4價,化合價降低被還原,體現氧化性;將產生的混合氣體通入裝置中,BaCl2溶液吸收SO3,SO3溶于水生成H2SO4,H2SO4與BaCl2反應生成BaSO4白色沉淀;同時H2SO4溶液能與氨水反應,所以混合氣體中被吸收了SO3和NH3;KMnO4具有強氧化性,能將SO2氧化,最終用排水法收集N2。
A. 根據以上分析,反應中硫元素只體現氧化性,故A錯誤;
B. 裝置Ⅰ中可以觀察到出現白色沉淀,其主要成分是BaSO4無BaSO3,故B錯誤;
C. KMnO4具有強氧化性,能將SO2氧化,裝置Ⅱ中可以觀察到高錳酸鉀紫色褪去,故C正確;
D. 將裝置Ⅰ、Ⅱ順序交換,SO2和SO3都被高錳酸鉀溶液吸收,則裝置Ⅰ中不會出現白色沉淀,故D錯誤。
故答案選C。


科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑩中元素,用元素符號或化學式填空回答以下問題:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在這些元素中,金屬性最強的元素是_______,最活潑的非金屬元素是_______;
(2)化學性質最不活潑的元素是__________,其原子的原子結構示意圖為_____________;
(3)元素的最高價氧化物對應的水化物中酸性最強的是______________,堿性最強的是____________,呈兩性的氫氧化物是____________________;
(4)③~⑦元素中,原子半徑最大的是________,原子半徑最小的是____________;
(5)在⑦與⑩的單質中,化學性質較活潑的是_____________,可用什么化學反應說明該事實(寫出反應的化學方程式)____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用鉍酸鈉(NaBiNO3)檢驗溶液中的Mn2+,反應方程式為:4MnSO4+10NaBiO3+14H2SO4═4NaMnO4+5Bi2(SO4)3+3Na2SO4+口,下列說法不正確的是
A. 口內的物質為水,配平系數為14。
B. 若生成1mol NaMnO4,則轉移5mole-
C. 反應方程式中的硫酸可換為鹽酸
D. 溶液中有Mn2+的現象是溶液變為紫紅色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】細胞中各種化合物占細胞鮮重的含量,以下按多到少順序排列,正確的是
A. 水、蛋白質、糖類 B. 蛋白質、糖類、脂質
C. 蛋白質、水、脂質 D. 水、糖類、蛋白質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,下列各組離子在指定溶液中能大量共存的是( )
A. 飽和氯水中:Cl-、NO3-、Na+、SO32-
B. ![]() =10-13 mol·L-1 溶液中:NH4+、Mg2+、NO3-、SO42-
=10-13 mol·L-1 溶液中:NH4+、Mg2+、NO3-、SO42-
C. 通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3-
D. Na2S溶液中:SO42-、K+、Cl-、Cu2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知充分燃燒a g乙炔氣體時生成1 mol二氧化碳氣體和液態水,并放出熱量b kJ,則乙炔燃燒的熱化學方程式正確的是
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=+b kJ/mol
B. C2H2(g)+![]() O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
O2(g)=2CO2(g)+H2O(l);△H=+2b kJ/mol
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-2b kJ/mol
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);△H=-4b kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學為測定Na2CO3固體(含少量NaCl)的純度,設計如下裝置(含試劑)進行實驗。
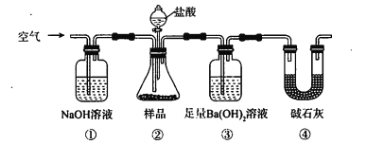
下列說法不正確的是
A. 必須在②③間添加吸收HCl的裝置
B. ④的作用是防止空氣中的氣體影響實驗的精確度
C. 通入空氣的作用是保證②中產生的氣體完全轉移到③中
D. 稱取樣品和③中產生的沉淀的質量即可求算Na2CO3固體的純度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(題文)Ⅰ.某探究性學習小組用相同質量的鋅和相同濃度的足量的稀硫酸反應得到實驗數據如下表所示:
實驗編號 | 鋅的狀態 | 反應溫度/℃ | 收集100 mL氫氣所需時間/s |
1 | 塊狀薄片 | 15 | 200 |
2 | 塊狀薄片 | 25 | 90 |
3 | 粉末 | 25 | 10 |
(1)該實驗的目的是探究________、________對鋅和稀硫酸反應速率的影響;
(2)實驗1和2表明___________________________,化學反應速率越大;
(3)能表明固體的表面積對反應速率有影響的實驗編號是________和_____________;
(4)請設計一個實驗方案證明硫酸的濃度對該反應的速率的影響:_________________________。
Ⅱ.近年來,隨著人們大量的開發使用,不但使得煤、石油、天然氣的儲量大大減少,而且直接燃燒化石燃料造成的環境污染問題,也是人類面臨的重大挑戰,如何實現化石燃料的綜合利用,提高效率,減少污染提上了日程.
為了提高煤的利用率,人們先把煤轉化為CO和H2,再將它們轉化為甲醇,某實驗人員在一定溫度下的密閉容器中,充入一定量的H2和CO,發生反應:2H2(g)+CO(g) ![]() CH3OH(g),測定的部分實驗數據如下:
CH3OH(g),測定的部分實驗數據如下:
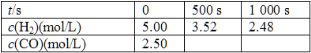
(1)在500 s內用H2表示的化學反應速率是__________________ mol/(L·S)。
(2)在1 000 s內用CO表示的化學反應速率是________ mol/(L·S), 1 000 s時CO的轉化率是__________。
(3)在500 s時生成的甲醇的濃度是________ mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X+、Y2+、Z-、W2-四種離子均具有相同的電子層結構,下列關于X、Y、Z、W四種元素的描述,不正確的是( )
A. 原子半徑:X>Y>Z>WB. 原子序數:Y>X>Z>W
C. 原子最外層電子數:Z>W>Y>XD. 金屬性:X>Y,還原性:W2->Z-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com