
【題目】依據氧化還原反應:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)設計的原電池如圖所示。請回答下列問題:

(1)電極X的材料是________;電解質溶液Y是_________;
(2)銀電極為電池的________極,發生的電極反應為__________________;X電極上發生的電極反應為________________________;
(3)外電路中的電子是從_______電極流向________電極。
(4)若電極X質量減少6.4g,則Ag極質量增加______ g.
【答案】 銅(或Cu) AgNO3溶液 正 Ag++e- = Ag Cu-2e- = Cu2+ 負(Cu) 正(Ag) 21.6
【解析】本題主要考查原電池原理。
(1)從2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)可以判斷電極X的材料是銅;電解質溶液Y是AgNO3溶液;
(2)較不活潑的銀電極為電池的正極,從2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)可知銀電極發生的電極反應為Ag++e- = Ag;X電極上發生的電極反應為Cu-2e- = Cu2+;
(3)外電路中的電子是從負極Cu電極流向正極Ag電極。
(4)Cu~2Ag~2e-,若電極X質量減少6.4g,,則Ag極質量增加21.6 g。


科目:高中化學 來源: 題型:
【題目】某有機物在氧氣中充分燃燒,生成CO2和H2O的物質的量之比為1:2,則該有機物
A.一定含有C、H、O三種元素B.分子中C、H原子個數之比為1:4
C.只含有C、H兩種元素D.最簡式為CH4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO+H2的混合氣體又稱“合成氣”,在合成有機物中應用廣泛。工業上常采用天然氣與水蒸氣或二氧化碳反應等方法來制取合成氣。請回答下列問題:
(1)已知在一定條件下,0.25molCH4 與水蒸氣完全反應制備“合成氣”時吸收51.5kJ 的熱量,請寫出該反應的熱化學方程式__________________________________________________。
(2)天然氣與CO2反應也可制備合成氣,在10L 密閉容器中通入lmolCH4 與1molCO2,在一定條件下發生反應,測得CH4的平衡轉化率與溫度及壓強的關系如下圖1所示。
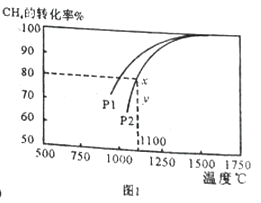
①1100℃、P2時氣體混合后反應經過10min 至x 點的平衡,用CO 的變化量表示反應速率v(CO)=_____________;
②下列選項中能表示該反應已達到平衡狀態的是____________;
A.v(H2)逆=3v (CO)正 B.密閉容器中混合氣體的密度不變
C.密閉容器中總壓強不變 D.c(CH4)=c(CO)
③由圖1可知,壓強P1_______P2 (填“大于”或“小于”);壓強為P2時,在y點: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y點對應溫度下的該反應的平衡常數K= __________。
(3)天然氣中的H2S 雜質常用氨水吸收,產物為NH4HS。
已知: 25℃時,NH3·H2O 的電離常數K=1.8×10-5,H2S 的兩步電離常數分別為Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中離子濃度大小關系_____________________(由大到小)。
(4)合成氣制甲醚的反應方程式為2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化劑、壓強為5.0MPa 的條件下,由H2和CO 直接制備甲醚,結果如圖2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化劑、壓強為5.0MPa 的條件下,由H2和CO 直接制備甲醚,結果如圖2 所示。
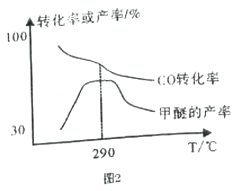
①290℃前,CO轉化率和甲醚產率的變化趨勢不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,體積為2L的密閉容器中,1mol X和3mol Y進行反應:X(g)+3Y(g)2Z(g),經12s達到平衡,生成0.6mol Z.下列說法正確的是( )
A.以X濃度變化表示的反應速率為 ![]() mol(Ls)
mol(Ls)
B.12s后將容器體積擴大為10L,Z的平衡濃度變為原來的 ![]()
C.若增大X的濃度,則物質Y的轉化率減小
D.若該反應的△H<0,升高溫度,平衡常數K減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用某有機物之間的轉換可以貯存太陽能,如降冰片二烯(NBD)經太陽光照可轉化成四環烷(Q),其反應式可表示為:  △H=+88.62kJ/mol
△H=+88.62kJ/mol
下列有關說法不正確的是( )
A.一定條件下,1mol NBD最多可與2 mol Br2發生加成反應
B.物質Q的能量比NBD的低
C.物質Q的一氯取代物只有3種
D.NBD和Q二者互為同分異構體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】弱電解質的電離平衡、鹽類的水解平衡和難溶物的溶解平衡均屬于化學平衡. I.已知H2A在水中存在以下平衡:H2AH++HA﹣ , HA﹣H++A2﹣ .
(1)NaHA溶液(選填“顯酸性”、“顯堿性”、“顯中性”或“無法確定”).
(2)某溫度下,0.1mol/L的NaHA溶液,下列關系中,一定正確的是 .
A.c(H+)c(OH﹣)=1×10﹣14
B.c(Na+)+c(H+)=c(HA﹣)+2c(A2﹣)
C.c(Na+)>c(HA﹣)>c(A2﹣)>c(H2A)
D.c(Na+)=c(HA﹣)+c(A2﹣)+c(H2A)
(3)已知常溫下,H2A的鈣鹽(CaA)飽和溶液中存在以下平衡:CaA(s)Ca2+(aq)+A2﹣(aq)△H>0. ①降低溫度時,Ksp(填“增大”、“減小”或“不變”,下同).
②滴加少量濃鹽酸,c(Ca2+) .
③測得25℃時,CaA的Ksp為2.0×10﹣11 , 常溫下將10g CaA固體投入100mL CaCl2溶液中,充分攪拌后仍有固體剩余,測得溶液中c(Ca2+)=0.1mol/L,則溶液中c(A2﹣)=mol/L
(4)II.工業廢水中常含有一定量的Cr2O72﹣和CrO42﹣ , 它們會對人類及生態系統產生很大的傷害,必須進行處理.常用的處理方法有還原沉淀法,該法的工藝流程為: CrO42﹣ ![]() Cr2O72﹣
Cr2O72﹣ ![]() Cr3+
Cr3+ ![]() Cr(OH)3
Cr(OH)3
其中第①步存在平衡:2CrO42﹣(黃色)+2H+Cr2O72﹣(橙色)+H2O
若平衡體系的pH=2,則溶液顯色.
第②步中,還原1mol Cr2O72﹣離子,需要mol的FeSO47H2O.
第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)Cr3+(aq)+3OH﹣(aq)
常溫下,Cr(OH)3的溶度積Ksp=c(Cr3+)c3(OH﹣)=10﹣32 , 要使c(Cr3+)降至10﹣5mol/L,溶液的pH應調至 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在第3周期中,置換酸中氫的能力最強的元素的元素符號為______,化學性質最穩定的元素符號是________,最高價氧化物的水化物的酸性最強的化合物的化學式是_______,堿性最強的化合物的化學式是___________,顯兩性的氫氧化物的化學式是____________,該兩性氫氧化物與鹽酸、氫氧化鈉溶液分別反應的離子方程式為_______________________________、_________________________________,原子半徑最大的金屬元素的名稱是____________________,離子半徑最小的離子結構示意圖是 ______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com