
定容容器中反應:N2(g)+3H2(g) 2NH3(g),下列措施不能提高其反應速率的是( )。
2NH3(g),下列措施不能提高其反應速率的是( )。
| A.升高溫度 | B.使用催化劑 |
| C.充入稀有氣體,增大體系壓強 | D.增加N2和H2的起始量 |
科目:高中化學 來源: 題型:單選題
在一定溫度下的恒容密閉容器中,能說明反應X2(g)+ Y2(g) 2XY(g) 已達到平衡的是( )
2XY(g) 已達到平衡的是( )
| A.容器中的總壓不隨時間變化 |
| B.容器中的氣體平均相對分子質量不隨時間變化 |
| C.容器中的混合氣體的密度不隨時間變化 |
| D.容器中的各種氣體的質量分數不隨時間變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法正確的是
| A.增大壓強,使單位體積內活化分子數目增加,化學反應速率一定增大 |
| B.升高溫度,使活化分子百分數增加,化學反應速率一定增大 |
| C.活化分子間所發生的分子間的碰撞均為有效碰撞 |
| D.加入反應物,使活化分子百分數增加,化學反應速率一定增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下,可逆反應N2 + 3H2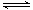 2NH3達到化學平衡狀態,下列說法一定正確的是( )
2NH3達到化學平衡狀態,下列說法一定正確的是( )
| A.每1 mol N≡N斷裂的同時有2 mol N—H生成 |
| B.N2、H2、NH3的濃度之比為1:3:2 |
| C.N2減少的速率和NH3減少的速率之比為1:2 |
D.氣體體積為初始體積的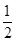 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知N2(g)+3H2(g) 2NH3(g) △H="—92.4" KJ/mol。在一恒溫恒壓的密閉容器里充入2mol N2和8mol H2達到平衡時生成1 mol NH3。現在相同條件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,達到平衡時,NH3的質量分數與原來相同,且放出熱量46.2KJ。則x、y的值分別為( )
2NH3(g) △H="—92.4" KJ/mol。在一恒溫恒壓的密閉容器里充入2mol N2和8mol H2達到平衡時生成1 mol NH3。現在相同條件下的同一容器中充入x mol N2,y mol H2和2 mol NH3,達到平衡時,NH3的質量分數與原來相同,且放出熱量46.2KJ。則x、y的值分別為( )
| A.1.5, 6.5 | B.2, 8 | C.5, 21 | D.3, 13 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下,在容積為10L的密閉容器中,將l mol X和1 mol Y進行如下反應:
2X(g)+Y(g)  Z(g),經60 s達到平衡生成0.3 mol的Z,下列說法正確的是( )
Z(g),經60 s達到平衡生成0.3 mol的Z,下列說法正確的是( )
| A.60 s內X的平均反應速率為0.001 mol·L-1·s-1 |
| B.將容器的容積變為20 L,Z的新平衡濃度將等于原平衡濃度的1/2 |
| C.若溫度和體積不變,往容器內增加1 mol X,Y的轉化率將增大 |
| D.若升高溫度,X的體積分數增大,則正反應的△H>0 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
用足量的鐵片與一定量的稀硫酸反應制氫氣,下列措施既能使氫氣的生成速率加快,又不影響氫氣的產量的是( )
| A.滴入適量Na2SO4溶液 | B.不用稀硫酸,改用98%的濃硫酸 |
| C.加入少量碳酸鈉固體 | D.不用鐵片,改用等質量的鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定條件下存在反應:CO(g)+H2O(g) CO2(g)+H2(g),其正反應放熱。現有三個相同的2L恒容絕熱(與外界沒有熱量交換) 密閉容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO 和2 mol H2O,700℃條件下開始反應。達到平衡時,下列說法正確的是
CO2(g)+H2(g),其正反應放熱。現有三個相同的2L恒容絕熱(與外界沒有熱量交換) 密閉容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2和1 mol H2,在Ⅲ中充入2 mol CO 和2 mol H2O,700℃條件下開始反應。達到平衡時,下列說法正確的是
| A.容器Ⅰ、Ⅱ中正反應速率相同 |
| B.容器Ⅰ、Ⅲ中反應的平衡常數相同 |
| C.容器Ⅰ中CO 的物質的量比容器Ⅱ中的多 |
| D.容器Ⅰ中CO 的轉化率與容器Ⅱ中CO2的轉化率之和小于1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
由可逆反應繪出圖像如圖,縱坐標為生成物在平衡混合物中的百分含量,下列對該反應的判斷正確的是 ( )
| A.反應物中一定有氣體 | B.生成物中一定有氣體 |
| C.正反應一定是放熱反應 | D.正反應一定是吸熱反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com