
【題目】現有10%的Na2CO3溶液,請按下面要求計算:
(1)106 g上述溶液中所含溶質的質量 g。
(2)106 g上述溶液與足量10%的鹽酸反應,最多可生成CO2多少克?
(3)向106 g上述溶液中逐滴加入10%的鹽酸并不斷攪拌,此時發生的反應為Na2CO3+HCl===NaHCO3+NaCl;當Na2CO3全部轉化為NaHCO3后,再加入鹽酸才開始放出CO2。請在圖中畫出產生氣體的曲線。
(4)另取10%的Na2CO3溶液邊攪拌邊加入10%的鹽酸,有關反應物與生成物的量如下表:
物質 | Na2CO3 | HCl | X | NaCl | CO2 | H2O |
質量/g | 31.8 | 14.6 | 16.8 | 23.4 | 4.4 | w |
則w= ,
寫出該反應的化學方程式 。
【答案】(1)10.6; (2)4.4 g;(3)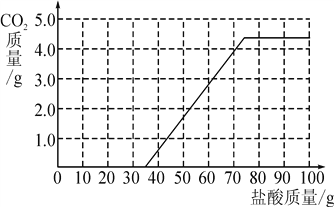 ;(4)1.8;3Na2CO3+4HCl===2NaHCO3+4NaCl+CO2↑+H2O
;(4)1.8;3Na2CO3+4HCl===2NaHCO3+4NaCl+CO2↑+H2O
【解析】(1) ![]() ,106 g上述溶液中所含溶質的質量:106g×10%=10.6g;
,106 g上述溶液中所含溶質的質量:106g×10%=10.6g;
(2)設10.6g碳酸鈉與鹽酸反應生成二氧化碳的質量為x,
Na2CO3+2HCl====2NaCl+H2O+CO2↑
106 44
10.6g x
106/10.6g=44/x x=4.4g
(3)設10.6g碳酸鈉轉化成碳酸氫鈉反應的氯化氫質量為y
Na2CO3+HCl===NaHCO3+NaCl
106 36.5
10.6g y
y =3.65g
需要鹽酸的質量為3.65g÷10%=36.5g
所以滴加鹽酸的過程中反應生成氣體的曲線圖為

(4)據質量守恒定律可知反應前后物質的總質量不變,所以水的質量為31.8+14.6 -16.8-23.4-4.4=1.8g。由反應表中數據和質量守恒定律可知反應后生成碳酸氫鈉;碳酸鈉、氯化氫、碳酸氫鈉、氯化鈉、二氧化碳、水的分子個數比為:
![]() ,所以反應方程式為:3Na2CO3+4HCl===2NaHCO3+4NaCl+CO2↑+H2O
,所以反應方程式為:3Na2CO3+4HCl===2NaHCO3+4NaCl+CO2↑+H2O


 活力課時同步練習冊系列答案
活力課時同步練習冊系列答案科目:初中化學 來源: 題型:
【題目】某同學梳理并歸納了以下知識點:①用肥皂水能區分軟水和硬水;②加入活性炭能降低水的硬度;③可以氮氣為原料制取硝酸和化肥;④最外層電子數為8的粒子一定是稀有氣體的原子;⑤質子數相同的粒子一定屬于同種元素;⑥保護水資源的措施是節約用水和防治水體污染。其中正確的是
A.①②④ B.①③④⑤⑥ C.①③⑥ D.②⑤⑥
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】往硫酸和硫酸銅的混合溶液中,逐滴加入氫氧化鈉溶液直至過量,根據實驗實施繪制如圖所示曲線,下列說法正確的是( )

A.a至b段有藍色沉淀生成
B.d點溶質種類為三種
C.c至d段,溶液pH不斷減少
D.c點所含的溶質種類最少
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】傳統干電池在日常生活中有多方面的應用,如圖顯示的是干電池的內部構造,請回答下列問題:

(1)寫出干電池正極材料主要成分的化學式:_______;
上述材料中屬于金屬材料的是______(寫一種);
(3)MnO2在實驗室利用過氧化氫溶液制取O2中起的是______作用.
(4)干電池是把_________能轉化為電能。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】甲、乙、丙、丁均為初中化學常見物質,它們之間的部分轉化關系如圖所示,關于該轉化關系圖,下列說法正確的是( )
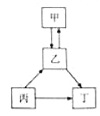
A.如果丙是碳酸鈉,乙是氫氧化鈉,則甲是硝酸鈉
B.若甲、乙、丁都是氧化物,則丙一定是碳酸鈣
C.甲、乙、丙、丁之間的轉化可以全部通過復分解反應實現
D.若甲、乙、丙、丁均含有同一種元素,且乙可用來滅火,則丙一定是單質碳
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】取CaCl2和CaCO3的混合物12.5g于燒杯中,向其中滴加一定溶質質量分數的稀鹽酸,請加稀鹽酸的質量與產生氣體質量的關系如圖所示。求:

(1)混合物CaCO3中的質量為 ;
(2)稀鹽酸中的溶質質量分數為 ;
(3)恰好完全反應時,所得不飽和溶液中溶質的質量分數?(寫出計算過程,計算結果精確到0.1%)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com