
【題目】溶液與人們的生活息息相關。
(1)以下是有關CO2氣體溶解度的幾組數據:
CO2在水中的溶解度(單位:mL)
壓強/大氣壓 | 溫度/℃ | ||||
0 | 25 | 50 | 75 | 100 | |
1 | 1.79 | 0.752 | 0.423 | 0.307 | 0.231 |
10 | 15.92 | 7.14 | 4.095 | 2.99 | 2.28 |
25 | 29.30 | 16.20 | 9.71 | 6.82 | 5.73 |
請根據數據
①根據CO2在水中的溶解度表,敘述外界條件是如何影響氣體溶解度的?_____。
②打開可樂瓶有氣體溢出,說明原瓶中的壓強_____(填“大于”“小于”或“等于”)瓶外大氣壓強。
(2)以飽和NaCl溶液跟飽和NH4HCO3溶液為原料制備NaHCO3的原理為:NaCl+NH4HCO3=NaHCO3↓+NH4Cl,該反應中的四種物質的溶解度曲線如圖所示。
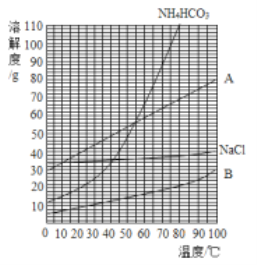
請回答下列問題。
①35℃時,比較A、B溶解度的大小:A_____B。
②圖中表示碳酸氫鈉溶解度曲線的是_____(填“A”或“B”)。
③發生上述反應析出晶體后的母液是碳酸氫鈉的_____(填“飽和”或“不飽和”)溶液。寫出母液中所有溶質的化學式_____。
【答案】當溫度相同時,壓強越大,氣體的溶解度越大;當壓強相同時,溫度越高,氣體的溶解度越小 大于 > B 飽和 NaHCO3、NH4Cl、NaCl、NH4HCO3
【解析】
(1)①根據CO2在水中的溶解度表可以看出:當溫度相同時,壓強越大,氣體的溶解度越大;當壓強相同時,溫度越高,氣體的溶解度越小;故填:當溫度相同時,壓強越大,氣體的溶解度越大;當壓強相同時,溫度越高,氣體的溶解度越小
②打開可樂瓶有氣體溢出,說明氣體溶解度減小,使得氣體的溶解度減少,溫度不變,說明瓶中壓強大于瓶外壓強;故填:大于
(2)①四種物質的溶解度曲線如圖可知,35℃時,A的溶解度大于B的溶解度。故填:>
②從侯氏制堿法的原理可知,四種物質中NaHCO3的溶解度最小,所以B表示NaHCO3的溶解度曲線;故填:B
③侯氏制堿法中生成NaHCO3的反應發生的原理是因為常溫下NaHCO3的溶解度較小,達到飽和后先析出固體,所以得到的母液是NaHCO3的飽和溶液,因此母液中含有的離子是Na+、HCO3-、NH4+、Cl-,所以母液中所有的溶質是NaHCO3、NH4Cl、NaCl、NH4HCO3;故填:飽和;NaHCO3、NH4Cl、NaCl、NH4HCO3


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】如圖是某汽車尾氣凈化裝置中發生反應的微觀示意圖。下列說法正確的是
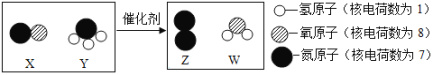
A. 該反應中,Z是由Y分解生成的
B. 一個Y和W分子中均有10個質子
C. 參加反應的X與生成的Z的質量比為9:7
D. 化學反應前后,催化劑的質量和性質一定不變
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】按要求寫出化學方程式
(1)實驗室制取二氧化碳_____。
(2)兩種黑色固體反應生成紅色固體_____。
(3)有沉淀生成的中和反應_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖1為興趣小組的同學在實驗室做將二氧化碳通入石灰水的實驗及現象。
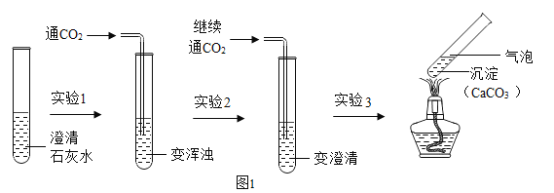
(1)實驗1:發生反應的化學方程式為_____。
(2)實驗2:二氧化碳、水繼續與碳酸鈣沉淀反應生成溶于水的Ca(HCO3)2
實驗3:實驗3中的化學方程式為Ca(HCO3) 2![]() CaCO3↓+H2O+CO2↑,從該實驗可得出結論:CaCO3比Ca(HCO3)2熱穩定性_____(選填“強”或“弱”)。
CaCO3↓+H2O+CO2↑,從該實驗可得出結論:CaCO3比Ca(HCO3)2熱穩定性_____(選填“強”或“弱”)。
(3)某地區硬水中溶有較多的可溶性Ca(HCO3)2、Mg(HCO3)2。
①生活中常用_____來區分硬水和軟水。
②煮沸硬水可降低水的硬度,同時生成難溶性混合物固體A。
(探究實驗一)上述固體A的成份是什么?
(猜想)固體A中除CaCO3外,還含有:
猜想1:只含MgCO3 猜想2:只含Mg(OH)2 猜想3:MgCO3和Mg(OH)2
(實驗1)取10.0g干燥的固體A,加入足量的稀鹽酸充分反應,產生4.4gCO2氣體。
(結論1)
①猜想1、2錯誤。其中判斷猜想1錯誤的理由是_____。
②猜想3正確,固體A中MgCO3和Mg(OH)2的質量比是_____。
(探究實驗二)判斷二氧化碳與氫氧化鈉溶液的是否能發生反應
(1)實驗a:取一充滿CO2的礦泉水瓶,加入一定量的水,立即擰緊瓶蓋,振蕩,發現瓶子變癟。另取一相同的充滿CO2的礦泉水瓶,向其中加入與水等體積的NaOH溶液,立即擰緊瓶蓋,振蕩,得到溶液X,此時觀察到的現象是_____。實驗中,用兩只礦泉水瓶做對比實驗的目的是_____。此對比實驗可證明CO2與NaOH溶液發生了化學反應。
(2)實驗b:如圖2所示的方案中:當A中沒有現象,B中出現白色渾濁,也可證明CO2和NaOH能發生反應。該裝置中,則B中所加試劑X應該是_____。
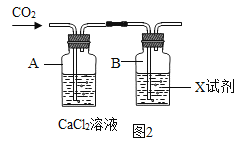
(3)實驗c:將CO2持續通入一定濃度一定量的NaOH溶液中,用數字化實驗技術測定反應過程中溶液的pH和溫度變化情況(結果如圖3、圖4所示)。
資料顯示:在本實驗條件下,Na2CO3溶液和 NaHCO3液的pH分別為11.0和8.5。
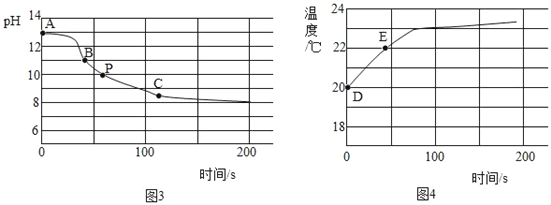
由圖3可知CO2和NaOH能發生反應。
①圖3中,AB段發生反應的化學方程式為_____。BC段發生反應的化學方程式為_____。P點時的溶液中的溶質為_____(寫化學式)。
②圖4中,DE段溫度變化的原因是_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】氨用于制造氮肥(尿素、碳銨等)、復合肥料、硝酸、純堿等,廣泛應用于化工、輕工、化肥制藥、合成纖維等領域。
Ⅰ.工業制氨是以哈伯法通過氮氣和氫氣在高溫高壓和催化劑的作用下化合生成的,請算出氮氣與氫氣恰好完全反應時的質量比________;
Ⅱ.目前有一種“人工固氮”的新方法反應過程示意圖如下:
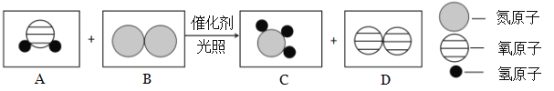
(1)根據反應的微觀示意圖寫出化學方程式:_____________;
(2)氨氣進入大氣后與雨水作用,可能形成“堿雨”。寫出堿雨中堿的化學式,并標出其中氮元素的化合價:_________;
Ⅲ.氨是氮肥的重要原料。某化肥廠生產銨態氮肥(NH4)2SO4的工藝流程如下:
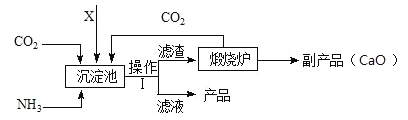
(1)操作Ⅰ中的玻璃棒作用是_________;
(2)加入的X應為_____(填字母)
A H2SO4 B CaSO4 C SO2
Ⅳ.氨也是工業索維爾法制純堿的重要原料。
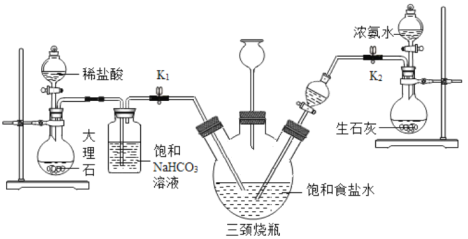
某興趣小組采用下列裝置模擬索維爾法制備碳酸氫鈉,實驗操作如下:
a.關閉K1,打開K2通入NH3,調節氣流速率,待其穩定后,打開K1通入CO2;
b.待三頸燒瓶內出現較多NaHCO3固體時,關閉K2停止通NH3,一段時間后,關閉K1停止通CO2;
c.將三頸燒瓶內的反應混合物過濾、洗滌、低溫干燥,并將所得固體置于敞口容器中加熱,記錄剩余固體質量。
加熱時間/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固體質量/g | 未記錄 | 30.6 | 27.4 | 23.8 | 21.2 | 21.2 |
(資料)常溫常壓下,1體積水約能溶解700體積氨氣,1體積水約能溶解1體積二氧化碳。
請回答下列問題:
(1)三頸燒瓶內生成的另一產物是一種銨態氮肥,寫出其中發生的化學反應方程式:__________;加熱過濾得到的NaHCO3,發生反應:2NaHCO3 ![]() Na2CO3 + CO2↑+ H2O。
Na2CO3 + CO2↑+ H2O。
(2)三頸燒瓶上連接的長頸漏斗的主要作用是__________;
(3)打開K2通入NH3一段時間后,才打開K1通入CO2,原因是__________;
(4)飽和碳酸氫鈉溶液的作用是______________;
(5)根據實驗記錄,計算t2 min時NaHCO3固體的分解率(已分解的NaHCO3質量與加熱前原NaHCO3質量的比值),請寫出計算過程__________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列四個圖象分別與選項中的操作相對應,其中合理的是
A. 溫度不變,向一定量的飽和石灰水中加入生石灰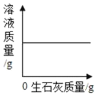
B. 向一定量鹽酸中滴加氫氧化鈉溶液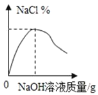
C. 向等質量的碳酸鉀和碳酸氫鈉中分別加入足量稀鹽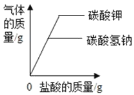
D. 向一定量的用硝酸酸化的硝酸銀溶液中滴加稀鹽酸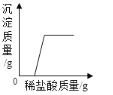
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在一密閉容器中,有四種物質,在一定條件下存在某個反應,測得反應前后各物質的質量如下表:已知X的相對分子質量為n、Q的相對分子質量為2n.下列推理中正確的是 ( )
物質 | X | Y | Z | Q |
反應前質量/g | 4 | 10 | 1 | 21 |
反應后質量/g | 0 | 12 | 15 | 待測 |
A. 該反應后待測Q質量為12g
B. 反應后生成15gZ
C. 該化學方程式中X與Q的化學計量數之比為2:3
D. 該反應中Y與Q質量之比為1:1
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某同學對氣體的實驗室制法作了以下探究,請根據圖回答下列問題:
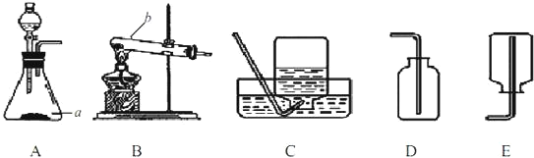
(1)寫出標有序號的儀器的名稱a_____;b_____
(2)請寫出能用B裝置制取氧氣的化學方程式_____;
(3)若發生裝置選A,收集裝置選C,則制取該氣體的化學反應方程式為:_____。
(4)實驗室用加熱氯化銨和氫氧化鈣固體混合物的方法制取氨氣(NH3),同時得到氯化鈣和水。該反應的化學方程式是_____,應選用的制取裝置為_____(填裝置編號
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】t1℃時,向盛有10mL水的A、B兩支試管中分別加入等質量的甲、乙兩種可溶性固體,充分溶解后,觀察到如圖1所示的現象。請回答:
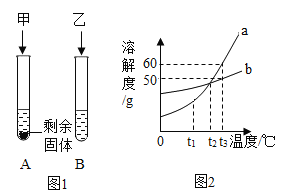
(1)圖2中表示甲物質溶解度曲線的是_____(填“a”或“b”)。
(2)將甲物質的不飽和溶液變為飽和溶液,可采用_____的方法;(任填一種)
(3)t3℃時,甲、乙兩種物質各55g分別加入100g水中,能形成溶液質量為155g的物質是_____(填“甲”或“乙”)。
(4)t3℃時甲乙兩物質的飽和溶液的溶質質量分數關系為:甲_____乙(填“>”、“<”、“=”或“無法確定”)
(5)將t2℃時等質量甲、乙兩物質的飽和溶液(沒有固體剩余)同時升溫到t3℃,所得溶液的質量大小關系為:甲_____乙(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com