
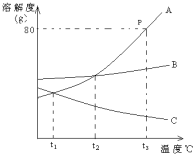
 如圖是A、B、C三種物質的溶解度曲線,據圖回答:
如圖是A、B、C三種物質的溶解度曲線,據圖回答:| 溶解度 |
| 100g+溶解度 |


 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:初中化學 來源: 題型:
 17、如圖是A、B、C三種固體物質的溶解度曲線示意圖,試回答下列問題.
17、如圖是A、B、C三種固體物質的溶解度曲線示意圖,試回答下列問題.查看答案和解析>>
科目:初中化學 來源: 題型:
 29、如圖是a、b、c三種固體物質的溶解度曲線圖.
29、如圖是a、b、c三種固體物質的溶解度曲線圖.查看答案和解析>>
科目:初中化學 來源: 題型:
 16、如圖是A、B、C三種固體物質的溶解度隨溫度變化的曲線圖.根據圖回答:
16、如圖是A、B、C三種固體物質的溶解度隨溫度變化的曲線圖.根據圖回答:查看答案和解析>>
科目:初中化學 來源: 題型:
 (1)如圖是A、B、C三種物質的溶解度曲線.請回答:
(1)如圖是A、B、C三種物質的溶解度曲線.請回答:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com