
【題目】(4分)某煉鋼廠廢氣中含SO2為0.32 g/L,SO2可以用混有CuO的CuSO4稀溶液吸收,得到CuSO4濃溶液,反應的化學方程式為:2CuO + 2SO2 + O2 == 2CuSO4。
(1)1000 L該廠廢氣中含有SO2的質量為 g。
(2)若該廠用足量CuO和足量的含CuSO4100 g的CuSO4稀溶液處理1000 L廢氣(假設SO2完全被吸收)。請計算反應后溶液中CuSO4的質量。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】氯堿工業用電解飽和食鹽水制取氯氣、燒堿。電解飽和食鹽水的化學方程式:
2NaCl + 2H2O![]() 2NaOH + H2↑+ Cl2↑
2NaOH + H2↑+ Cl2↑
化學興趣小組同學認為用上述方法制備的燒堿不純,進行如下探究,請回答有關問題。
①甲同學認為該燒堿可能含有少量食鹽,為了檢驗食鹽是否存在,進行了如下實驗:
實驗步驟 | 實驗現象 | 解釋與結論 |
1.取少量燒堿溶于水,滴加過量稀硝酸。 | 無明顯現象 | 解釋:滴加過量稀硝酸的目的是 (11) 。 |
2.再滴加 (12) 。 | (13) | 結論:燒堿中含有少量食鹽。 寫出有關化學方程式: (14) 。 |
②甲同學在上述檢驗后,根據氫氧化鈉與氯化鎂溶液反應:2NaOH+MgCl2→Mg(OH)2↓+2NaCl。測氫氧化鈉的質量分數,設計實驗步驟下圖所示。
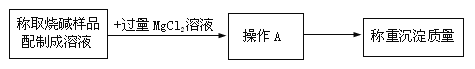
加入過量氯化鎂溶液的目的是 (15) 。
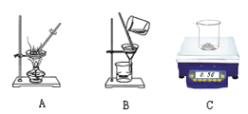
操作A的儀器或裝置如下圖所示,則操作A應選擇 (16) (填字母)裝置。根據上述實驗步驟操作,稱量與計算準確。利用沉淀物的質量計算氫氧化鈉的質量分數偏大,則可能的原因是 (17) 。
③乙同學依據甲檢驗,利用鹽酸與氫氧化鈉的反應測NaOH百分含量。實驗過程如下:稱取燒堿樣品ag,溶于水,滴加鹽酸至過量。滴加鹽酸的體積與pH變化規律如圖。

則根據實驗與圖象中的有關數據能否得出NaOH百分含量。
如果能,說明理由 (18) ;
如果不能,需要補充的數據是 (18) 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】一氧化碳,分子式CO,是無色、無味氣體,劇毒。比空氣略輕。在水中的溶解度很小。一氧化碳是含碳物質不完全燃燒的產物。也可以作為燃料使用。煤和水在高溫下可以生成水煤氣(一氧化碳與氫氣的混合物)。有些現代技術,如煉鐵,會產生副產品一氧化碳。它為中性氣體。燃燒時發出藍色的火焰,放出大量的熱。因此一氧化碳可以作為氣體燃料。一氧化碳作為還原劑,高溫或加熱時能將許多金屬氧化物還原成金屬單質,因此常用于金屬的冶煉。
由于一氧化碳與體內血紅蛋白的親和力比氧與血紅蛋白的親和力大200-300倍,而碳氧血紅蛋白較氧合血紅蛋白的解離速度慢3600倍,當一氧化碳濃度在空氣中達到35ppm,就會對人體產生損害,會造成一氧化碳中毒。
工業上煉鋼、煉焦、燒窯等在生產過程中爐門或窯門關閉不嚴,煤氣管道漏氣,汽車排出尾氣,都可逸出大量的一氧化碳。北方冬季用煤爐、火炕取暖因燃燒不完全而產生一氧化碳。
一氧化碳中毒的癥狀有頭暈、頭痛、惡心、嘔吐、反應遲鈍,嚴重時出現深昏迷。當發現或懷疑有人為一氧化碳中毒時,應立即采取下述措施:立即打開門窗通風;確保呼吸道通暢;迅速送往有高壓氧治療條件的醫院。
(1)一氧化碳的物理性質為 。
(2)為了預防煤氣中毒,冬季用煤爐取暖的家庭下列措施正確的是 。
a.在煤爐或床頭放一盆冷水 b.煙道連接處用膠條密封
(3)CO中毒的原理是 。
(4)工業用煤和水生產水煤氣的化學方程式是 。
(5)CO用于工業煉鐵,寫出此反應的化學方程式 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在一無色溶液中滴入數滴酚酞試液,溶液仍顯無色,則可以得出這樣的結論:①溶液是中性的;②溶液不可能是堿性的;③溶液可能是酸性的;④如果在該溶液中滴入紫色石蕊試液,溶液一定仍顯紫色,結論中正確的是
A.①②③④ B.①④ C.②③ D.以上答案都不對
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(2分)含鋅30%的黃銅用作彈殼的制造。現有一批使用過的、銹跡斑斑的彈殼,處理這些彈殼可以制得銅和硫酸鋅,其主要過程如下圖所示。
提示:彈殼上的銹主要為Cu2(OH)2CO3,能與稀硫酸反應得到硫酸銅溶液;彈殼中其他雜質不溶于水、不參加反應。
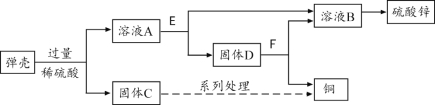
(1)固體D為 。
(2)溶液A中加入E后發生反應的化學方程式為 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(8分)某興趣小組同學對實驗室制備氧氣的條件進行如下探究實驗。
(1)為探究催化劑的種類對氯酸鉀分解速度的影響,甲設計以下對比實驗:
Ⅰ.將3.0 g KClO3與1.0 g MnO2均勻混合加熱。
Ⅱ.將x g KClO3與1.0 g CuO均勻混合加熱。
在相同溫度下,比較兩組實驗產生O2的快慢。
Ⅰ中反應的化學方程式是 ;Ⅱ中x的值應為________。
(2)乙探究了影響雙氧水分解速度的某種因素。反應的化學方程式為 ,有關實驗數據記錄如下:
雙氧水的質量 | 雙氧水的濃度 | MnO2的質量 | 相同時間內產生O2質量 | |
Ⅰ | 50.0 g | 1% | 0.1 g | 0.013 mg |
Ⅱ | 50.0 g | 2% | 0.1 g | 0.023 mg |
Ⅲ | 50.0 g | 4% | 0.1 g | 0.044 mg |
本實驗中,測量O2質量應用了圖的裝置。根據實驗裝置實驗所依據的原理是 。
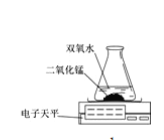
實驗結論:在相同條件下,________,雙氧水分解得越快。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com