在一次化學課外活動中,某同學想除去氯化鉀固體中混有的氯化銅(不引進其他雜質).化學老師為他提供了以下溶液:氫氧化鈉溶液、氫氧化鉀溶液、硫酸鈉溶液.該同學現取氯化鉀和氯化銅的混合物59.8g,全部溶解在200g水中,再加入60g所選溶液,恰好完全反應,生成沉淀9.8g.試回答:
(1)該同學所選的是______溶液.
(2)計算混合物中氯化銅的質量和反應后所得溶液中溶質的質量分數.(結果保留到小數點后一位數字)
解:(1)氫氧化鈉與氯化銅生成氯化鈉,不符合題意;硫酸鈉與氯化銅不形成沉淀、氣體、水,不能發生反應;氫氧化鉀與氯化銅生成氯化鉀和氫氧化銅沉淀;
故答:氫氧化鉀;
(2)設混合物中氯化銅的質量為x,生成氯化鉀的質量為y.
CuCl
2+2KOH═Cu(OH)
2↓+2KCl
135 98 149
x 9.8g y

=

解之得x=13.5g

=

解之得y=14.9g
反應后所得溶液中溶質的質量分數為:
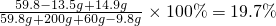
,
答:混合物中氯化銅的質量為13.5g,反應后所得溶液中溶質的質量為19.7%.
分析:除去氯化鉀固體中混有的氯化銅(不引進其他雜質),要求所加入的溶液即沉淀銅離子又能生成氯化鉀,根據復分解反應的規律,應選擇氫氧化鉀溶液;
反應溶液為氯化鉀溶液,其中氯化鉀一部分為原固體中氯化鉀,一部分為為反應生成氯化鉀.
點評:反應后所得溶液的質量根據質量守恒,溶液質量=混合固體物質質量+水的質量+所加溶液質量-生成沉淀質量.

 =
= 解之得x=13.5g
解之得x=13.5g =
= 解之得y=14.9g
解之得y=14.9g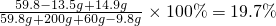 ,
,