
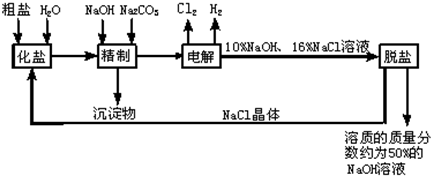
 2NaOH+H2↑+Cl2↑因為有強堿氫氧化鈉生成,所以電解后溶液的pH升高.
2NaOH+H2↑+Cl2↑因為有強堿氫氧化鈉生成,所以電解后溶液的pH升高.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
| ||
| ||
查看答案和解析>>
科目:初中化學 來源:2011年江蘇省無錫市育才中學中考化學二模試卷(解析版) 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com