
【題目】(13分)某興趣小組為了探究鐵粉與水蒸氣反應的產物,做了下面實驗。
資料:在不同溫度下,鐵粉與水蒸氣反應的產物不同。
Fe +H2O![]() FeO+H2 3Fe + 4H2O
FeO+H2 3Fe + 4H2O![]() Fe3O4 + 4H2
Fe3O4 + 4H2
實驗一:某興趣小組用下圖所示裝置,使鐵粉與過量水蒸氣充分反應并檢驗固體產物的組成。

鐵粉與水蒸氣的反應裝置
(1)實驗過程中,應先點燃 (選填“酒精燈”或“酒精噴燈”);目的是 ,裝置中石棉絨的作用是 。
(2)若在實驗中的某段時間內生成H20.04g,則這段時間內參加反應的鐵粉質量至少是 g。
實驗二:鐵粉完全反應后,興趣小組對硬質玻璃管中生成的FeO和Fe3O4的質量進行測定,實驗流程如下圖。

(1)實驗前如何檢查裝置A的氣密性關閉止水夾K,從長頸漏斗向試管內加水,至長頸漏斗中管內的 液面高于管外液面,靜置一段時間,若液面高度差 ,則氣密性良好。
(2)裝置A中發生的反應方程式 。
(3)為了安全,在點燃酒精燈之前,在F裝置出口b處必須 。
(4)裝置C中所放試劑為 ,則裝置B的作用是 。
(5)干燥管E右邊又連接干燥管F的目的是 。
若無干燥管F,測得Fe3O4的質量將 (填“偏大”、“偏小”或“無影響”)。
(6)若FeO和Fe3O4混合物的質量為15.2g,反應完全后干燥管E的質量增加了4.5g,則完全反應后D裝置中固體的質量為 g;混合物中Fe3O4的質量為 g。
【答案】實驗一(1)酒精燈 先產生水蒸氣,排盡空氣 增大鐵粉與水蒸氣接觸面積 (2)0.84
實驗二(1)不變 (2)Zn+2HCl=ZnCl2+H2↑ (3)驗純
(4)濃硫酸 除去HCl氣體 (5)防止空氣中的二氧化碳和水被E吸收 偏大
(6)11.2 11.6
【解析】
試題分析:實驗一(1)實驗過程中,應先點燃酒精燈;目的是:先產生水蒸氣,排盡空氣;裝置中石棉絨的作用是:增大鐵粉與水蒸氣接觸面積
(2)根據在不同溫度下,鐵粉與水蒸氣反應的產物不同,而從化學方程式來看,要產生相同質量的氫氣,當溫度>570℃時,消耗的鐵粉質量更少,故應根據反應:3Fe + 4H2O![]() Fe3O4 + 4H2來計算,反應中Fe 與氫氣的質量關系為168:8,故可設鐵粉質量至少為x,列式為:168:8=x:0.04g ,x=0.84
Fe3O4 + 4H2來計算,反應中Fe 與氫氣的質量關系為168:8,故可設鐵粉質量至少為x,列式為:168:8=x:0.04g ,x=0.84
實驗二(1)檢查裝置A的氣密性關閉止水夾K,從長頸漏斗向試管內加水,至長頸漏斗中管內的液面高于管外液面,靜置一段時間,若液面高度差不變,則氣密性良好
(2)裝置A中是鋅和鹽酸反應,發生的反應方程式:Zn+2HCl=ZnCl2+H2↑
(3)不純的氫氣在點燃時可能發生爆炸,故為了安全,在點燃酒精燈之前,在F裝置出口b處必須驗純,防止發生爆炸
(4)為了不影響后面水的質量的判斷,就必須保證反應前氫氣中不含有水分,故裝置C中所放試劑為濃硫酸,起到干燥的作用;鹽酸具有揮發性,故使得制得的氫氣中混有HCl氣體,故裝置B的作用是:除去HCl氣體
(5)干燥管E右邊又連接干燥管F的目的是:防止空氣中的二氧化碳和水被E吸收;若無干燥管F,則干燥管E的質量就會偏大,即使得水的質量偏大,故測得Fe3O4的質量將偏大
(6)反應完全后干燥管E的質量增加了4.5g,則說明反應過程中生成水的質量=4.5g ,根據反應的特點,反應過程生成水中的氧元素全部來自FeO和Fe3O4混合物中,而水中氧元素質量=4.5g×16/18×100%=4g,故完全反應后D裝置中固體的質量=15.2g-4g=11.2;可設混合物中Fe3O4的質量為x,則FeO 的質量為15.2g-x ;然后根據氧元素質量或鐵元素質量都可以列等式
x×168/232×100%+(15.2g-x) ×56/72×100%=11.2
x=11.6g


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:初中化學 來源: 題型:
【題目】近年來有人提出了利用處理后的海水(主要成份是氯化鈉溶液)吸收含二氧化硫的廢氣,該方法的流程如下圖所示。下列說法正確的是
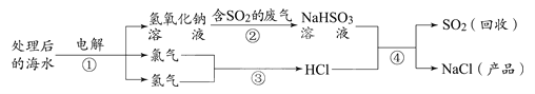
A.反應中硫元素的化合價發生變化
B.圖中反應① 屬于分解反應
C.反應③中,反應前后分子數目沒有變化
D.反應④中的反應物是兩種酸
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】大氣中PM2.5(指大氣中直徑不超過2.5×10—6m的顆粒物)的增多會導致灰霾天氣,對人體健康和環境質量的影響較大.下列措施中不利于PM2.5治理的是
A.發展燃煤發電 B.研究新能源汽車
C.禁止焚燒秸稈 D.加強建筑工地揚塵控制
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(11分)納米碳酸鋇是一種重要的無機化工產品,下圖是生產納米碳酸鋇的工藝流程.請回答下列問題:
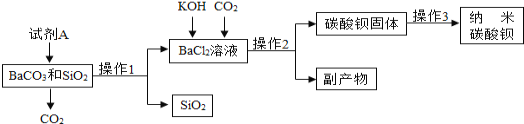
(1)試劑A名稱是 ,試寫出其與BaCO3反應的化學方程式 。
(2)操作1名稱為 ,用到的玻璃儀器有玻璃棒.燒杯和 ,玻璃棒此時的作用為
(3)操作2所得主要副產物為 (填化學式),該主要副產物可用作 (寫一種用途),操作3為洗滌、檢驗和烘干,其中洗滌的作用是 ,檢驗洗滌是否干凈可選用試劑為 (填化學式)溶液。
(4)上述流程中可循環利用的物質是 。
(5)資料:二氧化硅難溶于水,但可以和氫氧化鈉、氫氟酸等物質反應。某同學根據資料重新設計方案提純碳酸鋇:取碳酸鋇和二氧化硅混合物,滴加足量的 ,(從下列選項中選擇)過濾,洗滌,烘干得碳酸鋇固體。
A.蒸餾水 B.氫氧化鈉溶液 C.氫氟酸溶液
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(5分)中和反應是酸與堿生成鹽和水的反應,請你回答以下問題:
(1)下列事實不能表明鹽酸與氫氧化鈉發生了反應的是
A.向氫氧化鈉固體中加入鹽酸后,混合溶液的溫度升高
B.向氫氧化鈉溶液中加入鹽酸后,混合溶液的質量增大
C.向滴有酚酞的氫氧化鈉溶液中加入鹽酸后,紅色褪去
D.向氫氧化鈉溶液中加入鹽酸后,混合溶液的pH<7
(2)化學興趣小組在進行酸堿中和反應的課外研究時做了如下實驗:向裝有50g稀硫酸的小燒杯中,慢慢滴加Ba(OH)2飽和溶液至過量,并測定了其溶液的溫度、電導率變化曲線。請回答以下問題:
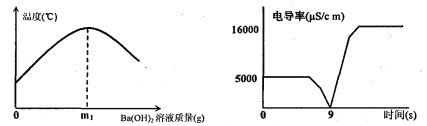
①請寫出稀硫酸與氫氧化鋇溶液反應的化學方程式 。
②稀硫酸溶液能導電,是因為其溶液中有自由移動的 (填微粒符號),當加入質量為m1g的Ba(OH)2溶液時,溶液導電性幾乎為0,其原因是 。
③經過實驗探究他們對中和反應的現象進行了歸類并提出猜想:
I酸堿溶液混合時無明顯現象,如氫氧化鈉溶液與稀鹽酸混合;
II酸堿溶液混合時產生白色沉淀,如氫氧化鋇溶液與稀硫酸混合;
Ⅲ請你模仿I和II,再舉出一種酸堿中和有明顯現象的實例 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列關于溶液的敘述,正確的是( )
A.無色透明的液體一定是溶液
B.溶液中各部分的性質均相同
C.植物油分散到水中可以形成溶液
D.溶液中只能有一種溶質
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗現象描述正確的是
A.硫在氧氣中燃燒發出淡藍色火焰
B.木炭在氧氣中燃燒發出白色火焰
C.細鐵絲在氧氣中燃燒,火星四射
D.磷在空氣中燃燒有大量的白霧
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小明購得用于食用菌種植的輕質碳酸鈣,標簽如圖。為測定其含鈣量小明進行的實驗是:

①稱取樣品5g;
②加入100g的稀鹽酸恰好反應,反應后燒杯內剩余物總質量為102.8g。
(1)計算樣品中碳酸鈣的質量分數是多少?
(2)標簽標示的含鈣量是否正確,若不正確應如何改正?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com