
【題目】我國化學家侯德榜改革國外的純堿生產工藝,生產流程可簡要表示如下:
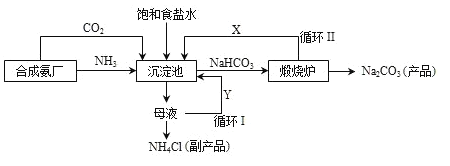
(1)上述生產純堿的方法稱_____,副產品的一種用途為_____。
(2)向沉淀池中通入兩種氣體,先通入的是_____(填“NH3”或“CO2”),沉淀池發生的化學反應方程式是_____。
(3)寫出上述流程中X物質的化學式_____。
(4)使原料氯化鈉的利用率從70%提高到90%以上,主要是設計了_____(填“循環Ⅰ”或“循環Ⅱ”)。從沉淀池中取NaHCO3沉淀的操作是_____。
(5)為檢驗產品碳酸鈉中是否含有氯化鈉,可取少量試樣溶于水后,先滴加足量的_____,排除Na2CO3的干擾,再滴加_____。
【答案】聯合制堿法 作化肥 NH3 ![]()
![]() 循環Ⅰ 過濾 硝酸 硝酸銀
循環Ⅰ 過濾 硝酸 硝酸銀
【解析】
聯合法制堿是以氯化鈉、二氧化碳、氨和水為原料, 制取純堿,副產氯化銨的過程,煅燒碳酸氫鈉時生成二氧化碳,氯化鈉和硝酸銀反應生成氯化銀和硝酸鈉,氨氣、二氧化碳、水和氯化鈉發生反應生成碳酸氫鈉和氯化銨。
(1)聯合法制堿是以氯化鈉、二氧化碳、氨和水為原料, 制取純堿,副產氯化銨的過程,故上述生產純堿的方法稱聯合制堿法,副產品是氯化銨,用途為作化肥。
(2)二氧化碳在水中的溶解度較小,氨氣極易溶于水,應該先通氨氣有利于吸收二氧化碳,故向沉淀池中通入兩種氣體,先通入的是NH3,沉淀池發生的反應是氨氣、二氧化碳、水和氯化鈉發生反應生成碳酸氫鈉和氯化銨,反應的化學反應方程式是![]() 。
。
(3)煅燒碳酸氫鈉時生成二氧化碳、二氧化碳能循環利用,故上述流程中X物質的化學式為![]() 。
。
(4)循環Ⅰ是將未反應的氯化鈉返回沉淀池中,氯化鈉最后剩余在母液中,故使原料氯化鈉的利用率從70%提高到90%以上,主要是設計了循環Ⅰ。過濾可以將固體和液體分離,故從沉淀池中取NaHCO3沉淀的操作是過濾。
(5)氯離子能和硝酸酸化的硝酸銀反應生成白色沉淀,為檢驗產品碳酸鈉中是否含有氯化鈉,可取少量試樣溶于水后,先滴加足量的稀硝酸,排除Na2CO3的干擾,再滴加硝酸銀溶液,有白色沉淀說明含有氯化鈉,否則,沒有氯化鈉。


 中考解讀考點精練系列答案
中考解讀考點精練系列答案科目:初中化學 來源: 題型:
【題目】下圖是甲、乙兩種固體物質的溶解度曲線,請回答:
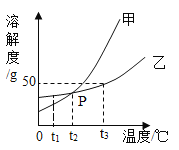
(1)甲、乙兩種物質溶解度受溫度影響較大的是_____________。
(2)t1℃時,甲的溶解度_________乙的溶解度(填“>”、“<”或“=”)。
(3)圖中P點的含義是_________。
(4)t3℃時,將30g甲物質加入到50g水中,所得溶液中溶質的量分數為________(保留到0.1%)。
(5)甲溶液中混有少量乙物質,可通過________ (填“蒸發結晶”或“降溫結晶”)提純甲物質。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】化學實驗過程經常會產生一定量的廢液,經過無害化處理可有效防止水體污染。在一次實驗課上,興趣小組的同學們完成了NaOH溶液和Na2CO3溶液的鑒別,并對廢液成分展開探究。
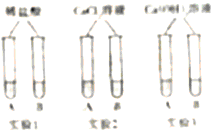
活動一
通過小組合作,同學們完成了右圖所示的三組小實驗。實驗中生成白色沉淀的化學方程式是____________________(寫一個)。
活動二
小雪將六支試管中的剩余物倒入一個潔凈的大燒杯中(如下圖), 充分攪拌、靜置。觀察到杯內上層是無色溶液,下層有白色沉淀。由此可以確定:上層溶液中一定不含有的離子是__________________、以及一定含有的離子。小組同學對上層溶液中還可能含有的離子進行了如下探究。![]()
(提出問題)上層溶液中還可能含有什么離子?
(猜想與假設)上層溶液中還可能含有OH-、CO32-、Ca2+中的一種或幾種。
(進行實驗)
實驗步驟 | 實驗現象 | 實驗結論 | |
方案一 | ①取少量溶液于試管中,滴加無色酚酞溶液②繼續滴加稀鹽酸 | ①溶液變紅 ②產生氣泡 | ①有OH- ②有CO32-、無Ca2+ |
方案二 | 取少量溶液于試管中,____________(指示劑除外) | ①____________ ②___________ | ①有CO32-、無Ca2+ ②有OH- |
(反思與評價)
(1)小明同學對方案一提出質疑, 他的理由是________________________。
(2)經過綜合分析,最終確定上層溶液中肯定存在的離子有______________________。
(3)將燒杯內物質過濾,濾渣回收,向濾液中加入適量_______________________進行處理后再排放。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室制取氣體所需的裝置如下圖所示。
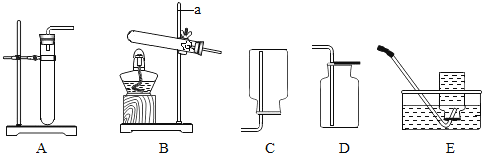
請回答以下問題。
(1)實驗儀器 a 的名稱是___________。
(2)用高錳酸鉀制取氧氣的化學方程式為__________,所選用的發生裝置為_________(填字母序號,下同),收集裝置為__________。
(3)用過氧化氫溶液和二氧化錳制取氧氣的化學方程式為____________。所選用的發生裝置也可做實驗室制備二氧化碳的發生裝置,該裝置是___________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】聯系已學的化學知識,回答下列問題。
(1)人體攝入_____元素不足或過量均會導致甲狀腺疾病。
(2)保險絲(鉛銻合金)比組成它的純金屬的熔點_____。
(3)用洗潔精除去油污,是由于洗潔精對油污有_____作用。
(4)牛奶是一種優質食品,除水外,牛奶中富含的營養素是_____。
(5)已知石蠟的著火點約為190℃,蠟燭的火焰由氣態石蠟燃燒形成,如圖所示,在溫度計示數為280℃以上時,快速推動活塞,會觀察蠟燭立即熄滅。蠟燭熄滅的主要原因是_____(填序號)。
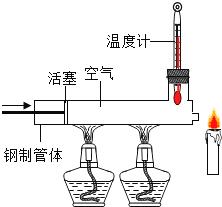
A 降低溫度至著火點以下
B 隔絕氧氣
C 移動可燃物
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列說法中正確的是![]()
A.根據質量守恒定律,1L氫氣和1L氧氣反應能生成2L水
B.只有固體、液體間的反應遵守質量守恒定律,如果氣體參加,就不遵守了
C.水結冰后質量沒有改變,由此說明化學變化符合質量守恒定律
D.鎂條在空氣中燃燒,生成物的總質量比原來鎂條的質量大
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】水是生命之源,沒有水就沒有生命。
(1)從物質的分類角度分析,水不屬于_____(填字母)
A 單質 B 氧化物 C 化合物 D 純凈物
(2)圖1為電解水的實驗,a試管中收集到的氣體為_____,此反應的化學方程式_____,此實驗可以說明水是由_____組成的;從能量轉化角度分析,電解水是將_____能轉化為_____能。
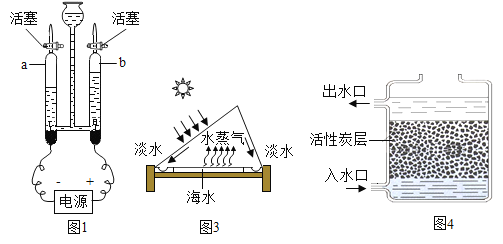
(3)自來水廠凈水過程的主要操作流程如圖2:
(資料:常用的絮凝劑有明礬![]() ,消毒劑有液氯。)
,消毒劑有液氯。)
回答下列問題:
①操作X的名稱是_____。
②明礬的作用是_____;其原理是明礬與水反應生成氫氧化鋁膠狀物。
③液氯(化學式Cl2)殺菌消毒屬于_____變化(填“物理”或“化學”),液氯也會與水中雜質反應生成一些對人體有害的物質。因此,水煮沸后,仍需要打開壺蓋繼續加熱一會兒。
④自來水廠的凈水過程_____(填“能”或“不能”)將硬水軟化成軟水,生活中將硬水軟化的方法是_____。
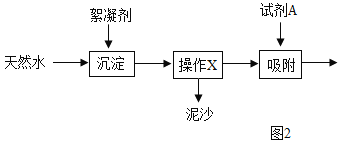
(4)海水淡化可緩解淡水資源匱乏的問題。圖3為太陽能海水淡化裝置圖。水變成水蒸氣的過程中,不發生變化的是_____(填字母序號)。
A 分子質量 B 分子運動 C 分子間隔 D 分子種類
這種方法與實驗室通過_____(填操作名稱)凈化水的方法原理相同。
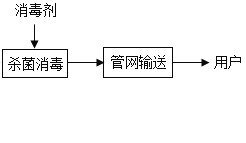
(5)圖4凈水器入水口在下方的優點是_____。
A 使水的化學性質發生改變
B 有助于除去懸浮性顆粒
C 不易堵塞活性炭孔
D 可以將硬水軟化
(6)保護水環境,珍愛水資源,是每個公民應盡的責任和義務。為了防止水的污染,下列做法有利于保護水資源的是(填序號)_____。
①抑制水中所有動、植物的生長;
②不任意排放工業廢水;
③大量使用化肥農藥;
④生活污水經過凈化處理后再排放。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】如圖是甲、乙固體的溶解度曲線。下列說法正確的是( )
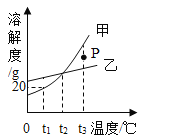
A.圖中P點所表示的溶液是t3℃時甲的飽和溶液
B.可用t1℃時20%的甲溶液配制10%的甲溶液
C.若甲中含有少量乙,可采用冷卻熱飽和溶液的方法提純甲
D.分別將t3℃等質量的甲、乙飽和溶液降溫至t2℃,所得溶液中溶質質量相等
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】請從A或B兩題中任選一個作答,若兩題均作答,按A計分。
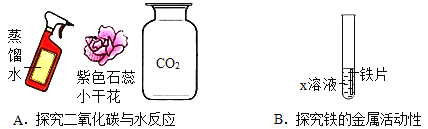
A | B |
(1)圖A探究二氧化碳與水反應的實驗操作為______________。 (2)二氧化碳與水反應的化學方程式為________。 | (1)圖 B 中,若X溶液為稀鹽酸,則觀察到的現象為____________。 (2)若 X 溶液為硫酸銅溶液,則反應的化學方程式為______________。 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com