
【題目】甲、乙兩個化學研究小組的同學對生活中的一些金屬材料進行了一系列的研究。
Ι.甲組同學收集了一些廢銅屑。他們欲用這些廢銅屑制取硫酸銅,設計了如下兩個方案:
方案1:Cu![]() CuO
CuO![]() CuSO4
CuSO4
方案2:Cu![]() CuSO4[已知Cu+2H2SO4(濃)
CuSO4[已知Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O]
CuSO4+SO2↑+2H2O]
從綠色化學的觀點出發,上述兩個方案中,你認為比較合理的是_____方案(填“1”或“2”)。
Ⅱ.乙組同學還利用單質銅制取氫氧化銅。設計方案如圖1:
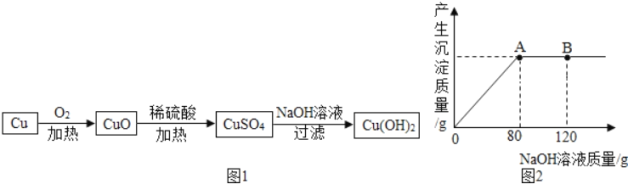
(1)銅加熱轉化為氧化銅的化學反應,屬于_____反應類型(填“化合”、“分解”、“置換”之一)。
(2)取一定量的氧化銅放入盛有一定量稀硫酸的燒杯中,恰好完全反應。向燒杯中逐滴加入 10%的NaOH溶液,產生沉淀的質量與所滴入NaOH溶液質量的關系曲線如圖2所示。
① 滴入上述NaOH溶液至 B 點時,溶液中溶質是_____。
② 當滴入上述NaOH溶液至 A 點時,試通過計算,所得氫氧化銅沉淀的質量_____。(計算結果精確至 0.1g)
【答案】1 化合 Na2SO4、NaOH 9.8g
【解析】
Ι.方案1:Cu![]() CuO
CuO![]() CuSO4,方案1沒有明顯的有毒性、污染性氣體產生,原料利用率高;
CuSO4,方案1沒有明顯的有毒性、污染性氣體產生,原料利用率高;
方案2:Cu![]() CuSO4[已知Cu+2H2SO4(濃)
CuSO4[已知Cu+2H2SO4(濃)![]() CuSO4+SO2↑+2H2O],根據給出的轉化關系可知生成二氧化硫,同時消耗的硫酸也多,所以從綠色化學的觀點出發,上述兩個方案中,比較合理的是方案1,故填1。
CuSO4+SO2↑+2H2O],根據給出的轉化關系可知生成二氧化硫,同時消耗的硫酸也多,所以從綠色化學的觀點出發,上述兩個方案中,比較合理的是方案1,故填1。
Ⅱ.(1)銅加熱轉化為氧化銅的化學反應,是兩種物質反應生成一種物質,符合化合反應的特征,屬于化合反應,故填化合。
(2)①由圖可知,滴入上述NaOH溶液至 A點沉淀達到最大量,此時硫酸銅與氫氧化鈉恰好完全反應,所以至B點時氫氧化鈉有剩余,此時的溶液中溶質是生成的Na2SO4和剩余的NaOH,故填Na2SO4和NaOH。
②解:參加反應的氫氧化鈉的質量為80g×10%=8g
設Cu(OH)2沉淀的質量為x
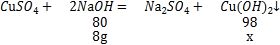
80:98=8g:x
x=9.8g
答:所得氫氧化銅沉淀的質量為9.8g。


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:
【題目】人類歷史發展的不同階段曾以不同金屬材料的使用作為標志。

(1)金、銀在自然界有單質形式存在,說明他們的化學性質都_____。
(2)在生產生活實踐中,人類逐漸掌握了多種金屬的冶煉技術。
①比較兩種鐵礦石磁鐵礦(主要成分Fe3O4)和菱鐵礦(主要成分FeCO3),從化學的角度分析“磁鐵礦作煉鐵原料更具優勢”,其原因是_____。
②近代工業上采用電解熔融氧化鋁(A12O3)的方法冶煉鋁,Al2O3分解后得到兩種單質,該反應的化學方程式為_____。
(3)鎂鋁合金被譽為“21世紀綠色金屬結構材料”。一種鎂鋁合金Mg17All2是特殊的儲氫材料,完全吸收氫氣后得到MgH2和Al,該反應的化學方程式為_____。
(4)鈦和鈦合金是21世紀的重要的金屬材料。鈦合金制品放在海水中數年,取出后仍光亮如新,是因為其_____(填字母序號)非常好。
A 可塑性 B 機械性能 C 抗腐蝕性能
(5)鐵在潮濕的空氣中反應生成疏松的鐵銹。已知:2FeCl3+Fe=3FeC12
①鐵銹的主要成分是_____(填化學式):將生銹的鐵制品放入一定量的稀鹽酸中充分反應,變化過程中最多涉及_____種化學反應基本類型。
②將10g表面生銹的鐵釘(雜質已忽略)浸泡在100g溶質質量分數為7.3%的稀鹽酸中充分反應,觀察到鐵銹已完全消失。反應停止后,取出光亮的鐵釘洗滌、干燥、稱量,質量為3.6g。則原銹鐵釘中鐵元素的質量分數為_____。
(6)利用“活潑金屬”可以制得H2,H2可用作汽車能源。若推廣應用于汽車產業,則需綜合考慮的因素有_____(填字母序號)。
A.金屬原料的成本 B.生成過程中的能耗和污染 C.金屬的回收利用
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】質量相等的四種物質①H2O2②KMnO4③KClO3④H2O,完全分解后所制得氧氣的質量由大到小的順序為_____(填序號,下同);四種金屬①Zn②Mg③Al④Fe分別投入質量相等且足量的稀硫酸中,充分反應后所得四種溶液的質量相等,則投入金屬的質量由小到大的順序為_____。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】某化學反應的微觀過程如圖,則下列說法中,不合理的是
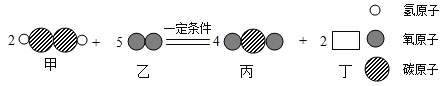
A. 該反應屬于氧化反應
B. 甲、乙兩物質參加反應的質量比為13:16
C. 物質丁的化學式是H2O
D. 反應前后氧元素的化合價發生了改變
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】小紅家從農貿市場買回一包化肥,化肥包裝上的標簽如圖所示,請回答下列問題。

(1)該化肥是由_____種元素組成的。
(2)該化肥中C、N兩種元素的質量比是_____。
(3)試通過計算說明此種尿素的純度____(是、否)為一級品?(國際一級品標準為尿素的質量分數98.5%),
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】A、B、C、D、E為初中化學常見的五種物質,它們之間存在如圖所示的關系(“→”表示物質經一步反應可轉化為另一種物質,“—”表示相連兩種物質能發生化學反應,部分反應物、生成物及反應條件已略去)。請回答下列問題:

(1)若A、B為組成元素相同的氣體,E為大理石的主要成分,寫出符合題意的D物質的一個化學式__。
(2)若A是能供給人類呼吸的氣體,B是一種最常用的溶劑,D常用于鉛蓄電池中,其濃溶液有脫水性。則D—E反應的化學方程式是_________。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】2019年6月5日是世界環境日,倡導“美麗中國,人人都是建設者”。關于如何建設我們美麗的家園,請回答下面問題:

(1)水是生命之源,請說出生活中一種節約用水的做法。
(2)如圖是由于空氣污染所造成的酸雨問題,請提出一條防治酸雨的有效措施。
(3)用布袋代替塑料袋的好處是什么?(答一點)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】煙臺有漫長的海岸線,蘊藏著豐富的海洋資源。
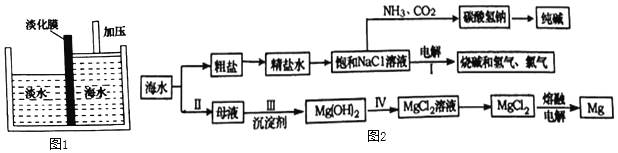
(1)海水淡化。可以采用如圖1所示的膜分離法淡化海水,水分子可以通過淡化膜(海水中體積較大的鹽的離子和其他分子不能通過)進入左側的淡水池,從而得到淡水。下列說法中正確的是________(填字母序號)。
A 膜分離法的原理與濾紙過濾原理類似
B 膜分離法還可以濃縮海水中的鹽類物質
C 膜分離法也是一種分離混合物的方法
D 該膜分離法的目的是除去海水中的不溶物
(2)粗鹽提純。除去難溶性雜質后的食鹽水中還含有Ca2+、Mg2+、SO42-等雜質離子,為得到較純的氯化鈉,進行如下的實驗操怍①加入過量的Na2CO3溶液;②加入過量的BaCl2溶液③加入過量的NaOH溶液;④加入適量的鹽酸調節溶液的pH等于7;⑤過濾;⑥蒸發。下列操作順序正確的是________(填字母序號),其中操作④加入適量的鹽酸調節溶液的pH等于7的目的是________。
A ①③②④⑤⑥
B ③②①④⑤⑥
C ③①②⑤④⑥
D ②③①⑤④⑥
(3)海水資源綜合利用的部分途徑如圖2。
①氨堿工業生產過程中,在加壓并不斷向飽和的氨鹽水中通入二氧化碳的條件下,使碳酸氫鈉結晶析出,該反應的化學方程式是________。
②寫出步驟Ⅰ電解飽和NaCl溶液的化學方程式是________。
③海水制鎂。實際生產中,步驟Ⅲ常選用________作為沉淀劑,從海水中提取MgCl2歷經步驟Ⅱ、Ⅲ、Ⅳ三步轉換的主要目的是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com