
【題目】化合物G是一種藥物合成中間體,其合成路線如下:
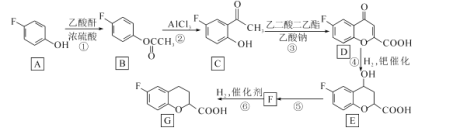
已知:乙酸酐的結構簡式為![]() 。請回答下列問題:
。請回答下列問題:
(1)G中含氧官能團的名稱是______________
(2)反應①的化學方程式為__________________
(3)反應⑤所需的試劑和條件是____,該反應類型是______________
(4)寫出滿足下列條件的C的同分異構體的結構簡式________________________。
I.苯環上只有兩種取代基;Ⅱ,核磁共振氫譜圖中只有4組吸收峰;Ⅲ.能與NaHCO3溶液反應生成CO2。
(5)碳原子上連有4個不同的原子或基團時,該碳稱為手性碳。則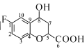 中的手性碳是____(填碳原子的數字標號)。
中的手性碳是____(填碳原子的數字標號)。
(6)設計以![]() 為原料制備
為原料制備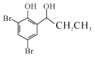 的合成路線(無機試劑任選)。
的合成路線(無機試劑任選)。
_____________________________________
【答案】羧基、醚鍵  濃硫酸、加熱 消去反應
濃硫酸、加熱 消去反應 ![]() 、
、![]() 5、8
5、8 
【解析】
(1)根據G的結構簡式,分析含有的含氧官能團;
(2)對比A和B的結構簡式,反應①為取代反應,據此書寫方程式;
(3)E→F→G過程中,消除了E中的羥基,因此反應⑤為消去反應,據此分析判斷;
(4)C的同分異構體的核磁共振氫譜有4組峰,說明是對稱結構,能與NaHCO3反應,說明含有羧基,據此分析和判斷;
(5)利用手性碳原子的定義進行分析;
(6)對比原料和目標產物結構的異同,利用題給信息和所學知識設計合成路線。
(1)根據G的結構簡式,G中的含氧官能團是醚鍵、羧基;
(2)對比A和B的結構簡式,A中氧氫鍵斷裂,乙酸酐中 ,從虛線中斷裂,該反應為取代反應,反應方程式為
,從虛線中斷裂,該反應為取代反應,反應方程式為 ;
;
(3) F→G顯然發生加成反應,說明F中含有不飽和鍵,即E生成F發生消去反應,所需試劑和條件為濃硫酸、加熱;
(4)C的同分異構體的核磁共振氫譜有4組峰,說明是對稱結構,兩個取代基位置應是對位,能與NaHCO3溶液反應,說明含有羧基,即符合條件的同分異構體是![]() 、
、![]() ;
;
(5)根據手性碳原子的定義,屬于手性碳原子是5、8;
(6)對比原料和目標產物,模仿B→C,先讓![]() 在AlCl3發生反應生成
在AlCl3發生反應生成 ,然后羰基與H2在鈀作催化劑下,發生加成反應,由于酚羥基的影響,使得苯環上的鄰位和對位上的氫變得活潑,容易發生取代,最后與濃溴水發生取代反應,即合成路線為
,然后羰基與H2在鈀作催化劑下,發生加成反應,由于酚羥基的影響,使得苯環上的鄰位和對位上的氫變得活潑,容易發生取代,最后與濃溴水發生取代反應,即合成路線為 。
。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列有關Fe2(SO4)3溶液的敘述正確的是
A.該溶液中K+、Fe2+、SCN-、Br-可以大量共存
B.和KI溶液反應的離子方程式:Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反應的離子方程式:Fe3++SO42-+Ba2++3OH-==Fe(OH)3↓+BaSO4↓
D.1 L 0.1 mol·L-1該溶液和足量的Zn充分反應,生成11.2 g Fe
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物分子中,當某個碳原子連接著四個不同的原子或原子團時,這種碳原子稱為“手性碳原子”。例如,下列有機物分子中帶“*”碳原子就是手性碳原子。該有機物分別發生下列反應,生成的有機物分子中仍含有手性碳原子的是

A. 與銀氨溶液作用發生銀鏡反應B. 催化劑作用下與![]() 反應
反應
C. 與乙酸發生酯化反應D. 與NaOH溶液加熱條件下反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮化鎵( GaN)是制造SG芯片的材料,氮化鋁LED燈可發出紫外光。回答下列問題:
(1) Ga的價電子排布式為____,該基態原子占據最高能級的電子云輪廓圖形狀為________。
下列狀態的鋁中,電離最外層的一個電子所需能量最小的是____(填字母)。
![]()
(2)8 -羥基喹啉鋁常用于發光材料及電子傳輸材料,可由LiAlH4與 合成。LiAlH4中陰離子的空間構型為_____________,
合成。LiAlH4中陰離子的空間構型為_____________, 所含元素中電負性最大的是____(填元素符號),N的雜化方式為________________
所含元素中電負性最大的是____(填元素符號),N的雜化方式為________________
(3)金屬晶體Al、Ga的熔點分別為660℃、30℃,Al比Ga熔點高的原因是____________
(4)氮化鎵為六方晶胞,結構如右圖所示。該晶體密度為ρg/cm3,晶胞參數a=b≠c(單位:pm),a、b夾角為120°,阿伏加德羅常數的值為NA,則晶胞參數c=____pm(用含a、ρ、NA的代數式表示)。

(5)在立方晶胞中,與晶胞體對角線垂直的面在晶體學中稱為(1,1,1)晶面。如右圖,該立方晶胞中(1,1,1)晶面共有____個。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把500![]() 有
有![]() 和
和![]() 的混合溶液分成5等份,取一份加入含
的混合溶液分成5等份,取一份加入含![]()
![]() 硫酸鈉的溶液,恰好使鋇離子完全沉淀;另取一份加入含
硫酸鈉的溶液,恰好使鋇離子完全沉淀;另取一份加入含![]()
![]() 硝酸銀的溶液,恰好使氯離子完全沉淀。則該混合溶液中鉀離子濃度為
硝酸銀的溶液,恰好使氯離子完全沉淀。則該混合溶液中鉀離子濃度為
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,反應N2(g)+3H2(g)2NH3(g),在1L密閉容器中進行,5min內氨的物質的量增加了0.2mol,則反應速率為( )
A. v(H2)=0.015mol/(L·min)B. v(N2)=0.02mol/(L·min)
C. v(NH3)=0.17mol/(L·min)D. v(NH3)=0.01mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于NaHCO3和Na2CO3的性質判斷正確的是( )
A.相同溫度下的溶解度:NaHCO3>Na2CO3
B.常溫下,相同物質的最濃度溶液的pH:NaHCO3<Na2CO3
C.熱穩定性:NaHCO3<Na2CO3
D.等物質的量濃度的兩種鹽溶液與同濃度、同體積的鹽酸反應生成氣體的快慢:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為Zn-Cu原電池的示意圖,請回答:

(1)鋅片為原電池的_____極,銅片為原電池的____極(填“正”或“負”)
(2)鋅電極反應式是_______,屬于______反應(填“氧化”或“還原”);銅電極反應式是______,屬于______反應(同上)。
(3)______(填“電子”或“電流”)從鋅片通過導線流向銅片,溶液中H+在______(填“鋅片”或“銅片”)獲得電子。
(4)若鋅片減輕0.1mol,則另一極放出氣體的物質的量為_____mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F六種物質有如下轉化關系,E為淡黃色粉末,通常用在呼吸面具中作為氧氣的來源。

(1)A、C、E、F的化學式:
A______,C______,E______,F______。
(2)向飽和的C的溶液中通入足量CO2,會出現的現象是_____,有關反應的化學方程式為____。
(3)鑒別C與F溶液應選用的試劑是_____,有關反應的離子方程式為_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com