
【題目】(1)2 mol O3和3 mol O2的質量之比為___,同溫同壓下的密度之比為____,含氧原子數之比為____。
(2)在標準狀況下,由CO和CO2組成的混合氣體6.72 L,質量為12 g.此混合物中CO和CO2分子數目之比是________,混合氣體的平均摩爾質量是________,對氫氣的相對密度是________.
(3)下列幾種均屬烴的含氧衍生物,請按要求作答:
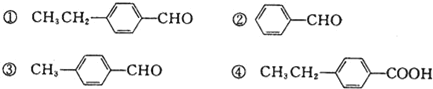
一定條件下①可轉化為④,下列試劑中能實現該轉化的是_________(填字母).
A.高錳酸鉀溶液 B.H2
C.銀氨溶液/H+ D.氫氧化鈉溶液
(4)已知 :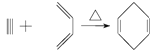 如果要合成
如果要合成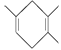 ,所用的起始原料的系統名稱為_________________。
,所用的起始原料的系統名稱為_________________。
【答案】1:1 3:2 1:1 1:3 40 20 C 2,3-二甲基-l,3-丁二烯和丙炔或2-甲基-l,3-丁二烯和2-丁炔
【解析】
(1)根據m=nM、N=nNA、ρ=![]() 、結合每個分子中含有的原子個數來分析解答;
、結合每個分子中含有的原子個數來分析解答;
(2)根據體積結合n=![]() =
=![]() 可列方程式組解計算其物質的量之比,再根據M=
可列方程式組解計算其物質的量之比,再根據M=![]() 、相同條件下氣體的密度之比等于其摩爾質量之比分析。
、相同條件下氣體的密度之比等于其摩爾質量之比分析。
(3)一定條件下①可轉化為④,僅是醛基被氧化,可用氫氧化銅懸濁液或銀氨溶液等弱氧化劑氧化;
(4)根據1,3-丁二烯與乙炔反應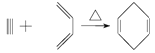 知,1,3-丁二烯中的兩個碳碳雙鍵斷裂,中間形成一個碳碳雙鍵,邊上兩個半鍵與乙炔中的兩個半鍵相連構成環狀,類比1,3-丁二烯與乙炔的加成反應,采用逆合成分析法可知,要合成
知,1,3-丁二烯中的兩個碳碳雙鍵斷裂,中間形成一個碳碳雙鍵,邊上兩個半鍵與乙炔中的兩個半鍵相連構成環狀,類比1,3-丁二烯與乙炔的加成反應,采用逆合成分析法可知,要合成![]() ,逆向推斷
,逆向推斷![]() 或者是
或者是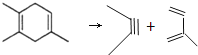 。
。
(1)臭氧的摩爾質量為48g/mol,氧氣的摩爾質量為32g/mol,根據m=nM知,其質量之比=(48g/mol×2):(32g/mol×3)=1:1;相同條件下,氣體摩爾體積相等,根據ρ=![]() 知,其密度之比等于其摩爾質量之比=48g/mol:32g/mol=3:2;一個臭氧分子中含有3個氧原子,一個氧氣分子中含有2個氧原子,其分子數之比為2:3,結合每個分子中含有的氧原子個數知,其原子個數之比為1:1;
知,其密度之比等于其摩爾質量之比=48g/mol:32g/mol=3:2;一個臭氧分子中含有3個氧原子,一個氧氣分子中含有2個氧原子,其分子數之比為2:3,結合每個分子中含有的氧原子個數知,其原子個數之比為1:1;
(2)設CO為xmol,CO2為ymol,則:x+y=![]() 、28x+44y=12,解得:x=0.075,y=0.225;此混合物中CO和CO2的分子數目比是0.075mol:0.225mol=1:3;混合氣體的平衡摩爾質量為
、28x+44y=12,解得:x=0.075,y=0.225;此混合物中CO和CO2的分子數目比是0.075mol:0.225mol=1:3;混合氣體的平衡摩爾質量為 ==40g/mol;相同條件下氣體的密度之比等于其摩爾質量之比,所以該混合氣體的密度相對氫氣的密度是20。
==40g/mol;相同條件下氣體的密度之比等于其摩爾質量之比,所以該混合氣體的密度相對氫氣的密度是20。
(3)一定條件下①可轉化為④,僅是醛基被氧化,可用氫氧化銅懸濁液或銀氨溶液等弱氧化劑氧化,題中高錳酸鉀具有強氧化性,還可氧化烴基,則只有C符合,故答案為C;
(4)根據1,3-丁二烯與乙炔反應![]() 知,1,3-丁二烯中的兩個碳碳雙鍵斷裂,中間形成一個碳碳雙鍵,邊上兩個半鍵與乙炔中的兩個半鍵相連構成環狀,類比1,3-丁二烯與乙炔的加成反應,采用逆合成分析法可知,要合成
知,1,3-丁二烯中的兩個碳碳雙鍵斷裂,中間形成一個碳碳雙鍵,邊上兩個半鍵與乙炔中的兩個半鍵相連構成環狀,類比1,3-丁二烯與乙炔的加成反應,采用逆合成分析法可知,要合成![]() ,逆向推斷
,逆向推斷![]() 或者是
或者是 ,若為
,若為![]() ,根據有機物的命名原則這兩種原料分別是2,3-二甲基-l,3-丁二烯和丙炔,若為
,根據有機物的命名原則這兩種原料分別是2,3-二甲基-l,3-丁二烯和丙炔,若為 根據有機物的命名原則這兩種原料分別是2-甲基-l,3-丁二烯和2-丁炔。
根據有機物的命名原則這兩種原料分別是2-甲基-l,3-丁二烯和2-丁炔。


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:
【題目】近期科學家報告了一種直接電化學合成H2O2的方法,裝置如圖。下列敘述不正確的是( )
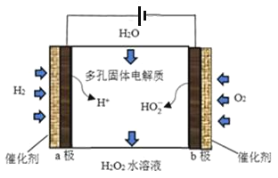
A.該裝置的工作原理是將化學能轉化成電能
B.b極發生的電極反應為O2+H2O+2e-=HO2-+OH-
C.電池工作時,內部發生反應:HO2-+OH-+2H+=H2O2+H2O
D.電路中通過2mol電子,消耗氧氣22.4L(標準狀況)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下表信息(部分短周期元素的原子半徑及主要化合價)可知,下列敘述正確的是
元素代號 | A | B | C | D | E |
原子半徑/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
主要化合價 | +1 | +3 | +2 | +6、-2 | -2 |
A.離子半徑大小:![]()
B.![]() 與
與![]() 的核外電子數不可能相等
的核外電子數不可能相等
C.最高價氧化物對應水化物的堿性:A<C
D.氫化物的穩定性:D>E
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】臭氧層是地球生命的保護神,臭氧比氧氣具有更強的氧化性.實驗室可將氧氣通過高壓放電管來制取臭氧:3O2![]() 2O3
2O3
(1)若在上述反應中有30%的氧氣轉化為臭氧,所得混合氣的平均摩爾質量為_________ (保留一位小數);
(2)將8L氧氣通過放電管后,恢復到原狀況,得到氣體6.5L,其中臭氧為__________L;
(3)實驗室將氧氣和臭氧的混合氣體0.896L(標準狀況)通入盛有20.0g銅粉的反應器中,充分加熱后,粉末的質量變為21.6g.則原混合氣中臭氧的體積分數為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】茚地那韋被用于新型冠狀病毒肺炎的治療,其結構簡式如圖所示(未畫出其空間結構)。

下列說法正確的是( )
A.茚地那韋屬于芳香族化合物,易溶于水
B.虛線框內的所有碳、氧原子均處于同一平面
C.茚地那韋可與氯化鐵溶液發生顯色反應
D.茚地那韋在堿性條件下完全水解,最終可生成三種有機物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列編號代表元素周期表中的一部分元素,用化學式回答下列問題:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ⑥ | ⑦ | ⑧ | |||||
三 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
四 | ② | ④ |
(1)①、③、⑤的最高價氧化物的水化物堿性由強到弱順序為___________(填化學式,下同)。
(2)②、③、④形成的簡單陽離子半徑由大到小的順序是______________。
(3)⑨和⑩的最高價氧化物對應的水化物化學式為_______和_________。①在氧氣中點燃生成淡黃色的固體,該固體的電子式為_______________,①能夠與水劇烈反應,請寫出該反應的化學方程式_______________,將元素⑩的單質通入NaBr溶液中,反應的離子方程式為_______________。
(4)⑥、⑦、⑧三種元素形成的氣態氫化物的穩定性排序是____________(填化學式,下同),三種元素非金屬性由強到弱的順序為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海水中含有的氯化鎂是鎂的重要來源之一。從海水中制取鎂有多種生產方法,可按如下步驟進行:
①把貝殼制成石灰乳
②在引入的海水中加石灰乳,沉降、過濾、洗滌沉淀物
③將沉淀物與鹽酸反應,結晶、過濾、干燥產物
④將得到的產物熔融后電解
關于從海水中提取鎂的下列說法不正確的是( )
A. 此法的優點之一是原料來源豐富
B. 進行①②③步驟的目的是從海水中提取氯化鎂
C. 以上制取鎂的過程中涉及的反應有分解反應、化合反應和置換反應
D. 第④步電解制鎂是由于鎂是很活潑的金屬
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物結構簡式為 ,下列敘述不正確的是( )
,下列敘述不正確的是( )
A. 1mol該有機物在加熱和催化劑作用下,最多能和4 molH2反應
B. 該有機物能使溴水褪色也能使酸性KMnO4溶液褪色
C. 該分子中最多有9個碳原子共平面
D. 該有機物在一定條件下,能發生消去反應或取代反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎授予美國科學家約翰古迪納夫、斯坦利惠廷厄姆和日本科學家吉野彰,以表彰他們在鋰離子電池研發領域作出的貢獻。近日,有化學家描繪出了一種使用DMSO(二甲亞砜)作為電解液,并用多孔的黃金作為電極的鋰—空氣電池的實驗模型,該電池放電時在多孔的黃金上氧分子與鋰離子反應,形成過氧化鋰,其裝置圖如圖所示。下列有關敘述正確的是( )

A.DMSO電解液能傳遞Li+和電子,不能換成水溶液
B.該電池放電時每消耗2molO2,轉移4mol電子
C.給該鋰—空氣電池充電時,金屬鋰接電源的正極
D.多孔的黃金為電池正極,電極反應式可能為O2+4e-=2O2-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com