
【題目】化學電池在通訊、交通及日常生活中有著廣泛的應用。
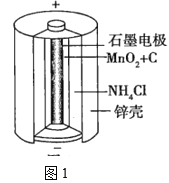
(1)鋅錳干電池是應用最普遍的電池之一,圖1為鋅錳干電池的構造示意圖,鋅錳干電池的負極材料是___(填物質名稱),負極發生的電極反應為___。若反應消耗32.5g負極材料,則電池中轉移電子的數目為___。
(2)目前常用的鎳-鎘(Ni—Cd)可充電電池的總反應式可表示為Cd+2NiO(OH)+2H2O![]() 2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均難溶于水,但能溶于酸,以下說法正確的是___(填序號)。
2Ni(OH)2+Cd(OH)2,已知Ni(OH)2和Cd(OH)2均難溶于水,但能溶于酸,以下說法正確的是___(填序號)。
①該電池可以在酸性條件下進行充、放電。
②該電池放電時,負極的電極反應式為Cd+2OH--2e-=Cd(OH)2
③該電池放電時,Cd極的質量減少
④該電池放電時,化學能轉變為電能。
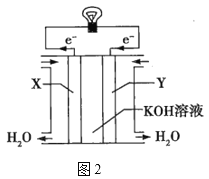
(3)圖2為氫氧燃料電池的構造示意圖,電解質溶液是KOH溶液。則X極為電池的__(填“正”或“負”)極,X極的電極反應式為___。
【答案】鋅 Zn-2e-=Zn2+ 6.02×1023 ②④ 負 H2-2e-+2OH-=2H2O
【解析】
鋅錳干電池是應用最普遍的電池之一,鋅為負極,發生氧化反應;鎳-鎘(Ni—Cd)可充電電池,放電為原電池,充電為電解池,氫氧燃料電池屬于新型電池,氫氣做負極,發生氧化反應,氧氣在正極發生還原反應,在分析和書寫極反應時,要注意電解質溶液的性質。
(1)負極發生氧化反應,鋅失去電子被氧化,所以負極材料為鋅,電極反應式為Zn-2e-=Zn2+,32.5g鋅的物質的量為0.5mol,1mol鋅參與反應失去2mol電子,所以32.5g鋅參與反應時轉移電子的物質的量為1mol,數目為6.021023。
答案為:鋅;Zn-2e-=Zn2+;6.021023。
(2)①Ni(OH)2與Cd(OH)2可以與酸反應,則該電池不能在酸性條件下進行充、放電,①錯誤;
②電池放電時,負極的電極反應式為Cd+2OH--2e-=Cd(OH)2,②正確;
③電池放電時,Cd為負極,發生氧化反應生成Cd(OH)2,Cd極的質量增加,③錯誤;
④該電池放電時為原電池,化學能轉化為電能,④正確。
答案選②④。
(3)電解質溶液為KOH溶液,X電極上失去電子,為負極,氫氣在負極失電子被氧化,電極反應式為:H2+2OH--2e-=2H2O。
答案為:H2+2OH--2e-=2H2O。


科目:高中化學 來源: 題型:
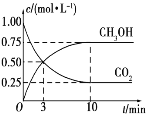
【題目】已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定條件下,向體積為1 L的密閉容器中充入1mol CO2和3mol H2,測得CO2和CH3OH(g)的濃度隨時間變化曲線如圖所示。下列敘述中,正確的是
A.升高溫度能使![]() 增大
增大
B.反應達到平衡狀態時,CO2的平衡轉化率為75%
C.3min時,用CO2的濃度表示的正反應速率等于用CH3OH的濃度表示的逆反應速率
D.從反應開始到平衡,H2的平均反應速率v(H2)=0.075mol·L-1·min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于如圖所示的原電池,下列說法正確的是( )
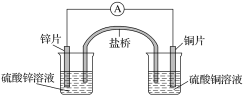
A. 電子從鋅電極通過電流表流向銅電極
B. 鹽橋中的陰離子向硫酸銅溶液中遷移
C. 鋅電極發生氧化反應;銅電極發生還原反應,其電極反應是2H++2e-===H2↑
D. 取出鹽橋后,電流表仍會偏轉,銅電極在反應前后質量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】燃料電池是目前電池研究的熱點之一。某課外小組自制的氫氧燃料電池如圖所示,a、b均為惰性電極下列敘述不正確的是( )
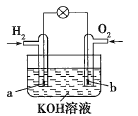
A.a極是負極,該電極上發生氧化反應
B.b極發生的電極反應是O2+4OH--4e-=2H2O
C.電池總反應方程式為2H2+O2=2H2O
D.氫氧燃料電池是一種具有應用前景的綠色電源
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有利于可持續發展的生態環境是全國文明城市評選的測評項目之一。
(1)已知反應 2NO(g)+2CO(g)![]() N2(g)+2CO2(g) v 正=k 正·c2(NO)·c2(CO),v 逆=k 逆·c(N2)·c2(CO2)(k正、k逆為速率常數,只與溫度有關)。一定條件下進行該反應,測得 CO 的平衡轉化率與溫度、起始投料比m=
N2(g)+2CO2(g) v 正=k 正·c2(NO)·c2(CO),v 逆=k 逆·c(N2)·c2(CO2)(k正、k逆為速率常數,只與溫度有關)。一定條件下進行該反應,測得 CO 的平衡轉化率與溫度、起始投料比m=![]() 的關系如圖 1 所示。
的關系如圖 1 所示。

①達到平衡后,僅升高溫度,k正增大的倍數________填“>”“<”或“=”)k逆增大的倍數。
②下列說法正確的是_______。
A 投料比:m1<m2<m3
B 汽車排氣管中的催化劑可提高 NO 的平衡轉化率
C 當投料比 m=2 時,NO 轉化率比 CO 轉化率小
D 當體系中 CO2 和 CO 物質的量濃度之比保持不變時,反應達到平衡狀態
③若在 1L 的密閉容器中充入 1 molCO 和 1 mol NO,在一定溫度下達到平衡時,CO 的轉化率為 40%, 則 k 正︰k 逆=_______(填寫分數即可,不用化簡)
(2)在 2L 密閉容器中充入 2mol CO 和 1mol NO2,發生反應 4CO(g)+2NO2(g)![]() N2(g)+4CO2(g) ΔH<0,如圖 2 為平衡時 CO2 的體積分數與溫度、 壓強的關系。
N2(g)+4CO2(g) ΔH<0,如圖 2 為平衡時 CO2 的體積分數與溫度、 壓強的關系。
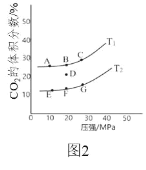
①該反應達到平衡后,為在提高反應速率同時提高 NO 的轉化率,可采 取的措施有______(填字母序號)
a 增加 CO 的濃度 b 縮小容器的體積 c 改用高效催化劑 d 升高溫度
②若在 D 點對反應容器降溫的同時縮小體積至體系壓強增大,達到的平衡狀態可能是圖中 A G 點中的______點。
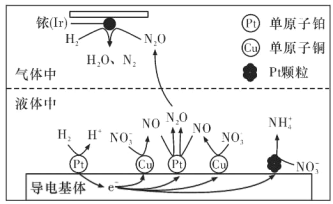
(3)近年來,地下水中的氮污染已成為一個世界性的環境問題。在金屬Pt、Cu和銥(Ir)的催化作用下,密閉容器中的 H2 可高效轉化酸性溶液中的硝態氮(NO3-),其工作原理如下圖所示。若導電基體上的 Pt 顆粒增多,造成的后果是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D1、D2均為有機化合物,請根據圖示回答問題.

(1)直鏈有機化合物A的結構簡式是______________;
(2)①的反應類型是____________________;.
(3)②的反應類型是__________________;
(4)③的反應類型是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據圖的能量圖,下列說法正確的是( )

A. A2(g)+B2(g)=2AB(g)是一個放熱反應
B. 2molAB(g)的總能量大于1mol A2(g)和1mol B2(g)的能量之和
C. 1mol A2(g)和1 mol B2(g)的能量之和為a kJmol﹣1
D. 2AB(g)═A2(g)+B2(g)△H=( a﹣b)kJmol﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以煤、天然氣和生物質為原料制取有機化合物日益受到重視。E是兩種含有碳碳雙鍵的酯的混合物。相關物質的轉化關系如下(含有相同官能團的有機物通常具有相似的化學性質):

請回答:
(1) A→B的反應類型________,C中含氧官能團的名稱________。
(2) C與D反應得到E的化學方程式________。
(3) 檢驗B中官能團的實驗方法________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】前四周期元素![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 的原子序數依次增大。
的原子序數依次增大。![]() 與
與![]() 同周期且相鄰的非金屬元素,
同周期且相鄰的非金屬元素,![]() 的基態原子的s電子數與p電子數相等,
的基態原子的s電子數與p電子數相等,![]() 是地殼中含量最多的金屬元素,
是地殼中含量最多的金屬元素,![]() 的原子核外價電子排布式為
的原子核外價電子排布式為![]() ,
,![]() 的基態原子的未成對電子數是同周期元素中最多的。下列說法錯誤的是
的基態原子的未成對電子數是同周期元素中最多的。下列說法錯誤的是
A.簡單氣態氫化物的穩定性:![]()
B.簡單離子的半徑:![]()
C.![]() 的最高價氧化物對應的水化物既能與強酸反應,又能與強堿反應
的最高價氧化物對應的水化物既能與強酸反應,又能與強堿反應
D.由![]() 、
、![]() 、
、![]() 三種元素形成的某種化合物可用于檢查司機是否酒后駕車
三種元素形成的某種化合物可用于檢查司機是否酒后駕車
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com