
【題目】


A. ①中陽極處能產生使濕潤淀粉KI試紙變藍的氣體
B. ②中待鍍鐵制品應與電源正極相連
C. ③中鋼閘門應與外接電源的正極相連,稱為犧牲陽極的陰極保護法
D. ④中的離子交換膜可以避免生成的Cl2與NaOH溶液反應
科目:高中化學 來源: 題型:
【題目】H3BO3可以通過電解NaB(OH)4溶液的方法制備,其工作原理如圖,下列敘述錯誤的是( )

A. M室發生的電極反應式為:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. b膜為陰膜,產品室發生反應的化學原理為強酸制弱酸
D. 理論上每生成1mol產品,陰極室可生成標準狀況下5.6L氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課外研究性學習小組用下圖所示裝置制備少量溴苯并驗證溴與苯的反應是取代反應。

實驗時,關閉F活塞,打開C活塞,在裝有少量苯的三口燒瓶中由A口加入少量液溴,再加入少量鐵屑,塞住A口。
回答下列問題:
(1) D試管內裝的是_________,其作用是__________________________。
(2) E試管內裝的是________________。
(3) 除去溴苯中混有的Br2雜質的試劑是____________,操作方法為:__________。
(4) 三口燒瓶中發生反應的化學方程式為:_______________________________。
(5) 根據什么現象可證明驗證溴與苯的反應是取代反應?__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物G是一種醫藥中間體,常用于制備抗凝血藥。可以通過下圖所示的路線合成:
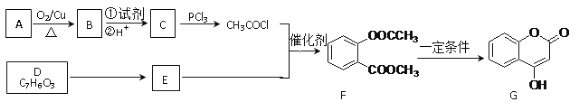
已知:RCOOH![]() RCOCl;D與FeCl3溶液能發生顯色。
RCOCl;D與FeCl3溶液能發生顯色。
請回答下列問題:
⑴B→C的轉化所加的試劑可能是__________,C+E→F的反應類型是_______。
⑵有關G的下列說法正確的是_________。
A.屬于芳香烴 B.能與FeCl3溶液發生顯色反應
C.可以發生水解、加成、氧化、酯化等反應 D.1mol G最多可以跟4mol H2反應
⑶E的結構簡式為_________。
⑷F與足量NaOH溶液充分反應的化學方程式為__________________________________。
⑸寫出同時滿足下列條件的E的同分異構體的結構簡式_______________。
①發生水解反應②與FeCl3溶液能發生顯色反應③苯環上有兩種不同化學環境的氫原子
⑹已知:酚羥基一般不易直接與羧酸酯化。而苯甲酸苯酚酯(![]() )是一種重要的有機合成中間體。試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用)。注:合成路線的書寫格式參照如下示例流程圖:_________________
)是一種重要的有機合成中間體。試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用)。注:合成路線的書寫格式參照如下示例流程圖:_________________
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學在能源開發與利用中起到十分關鍵的作用。甲烷是一種新型的綠色能源,又是一種重要的化工原料。甲烷燃料電池能量轉化率高,具有廣闊的發展前景,現用甲烷燃料電池進行如圖實驗(圖中所用電極均為惰性電極)

(1)電極b為______________極,溶液中OH-移向_____________極(填a或b);
(2)電極a處所發生的電極反應方程式為 ;
(3)乙裝置所發生的總反應方程式 ;
(4)如圖裝置中盛有100mL0.2molL-1AgNO3溶液,當氫氧燃料電池中消耗氧氣56mL(標準狀況下)時,則此時右圖裝置中溶液的pH=__________(溶液體積變化忽略不計),d極增重 g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(15分)為研究銅與濃硫酸的反應,某化學興趣小組進行如下實驗。
實驗I:反應產物的定性探究,按如圖裝置(固定裝置已略去)進行實驗:
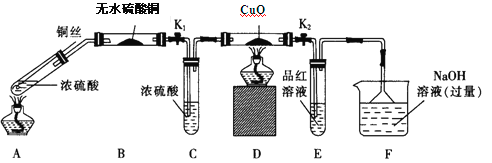
(1)F裝置的燒杯中發生反應的離子方程式是 ;B裝置中的現象是 。
(2)實驗過程中,能證明濃硫酸中硫元素的氧化性強于氫元素的現象是 。
(3)實驗結束時,撤去所有酒精燈之前必須完成的實驗操作是 。
(4)實驗結束后,證明A裝置試管中反應所得產物是否含有銅離子的操作方法是 。
實驗Ⅱ:反應產物的定量探究
(5)在銅與濃硫酸反應的過程中,發現有黑色物質出現,且黑色物質為Cu2S。產生Cu2S的反應為aCu+![]()
(6)為測定硫酸銅的產率,將該反應所得溶液中和后配制成250.00 mL溶液,取該溶液25.00 mL加入足量 KI溶液中振蕩,以淀粉溶液為指示劑,用O.36 mol·![]() 的Na2S2O3溶液滴定生成的I2,3次實驗平均消耗該Na2S2O3溶液25.00 mL。若反應消耗銅的質量為6.4 g,則硫酸銅的產率為 。
的Na2S2O3溶液滴定生成的I2,3次實驗平均消耗該Na2S2O3溶液25.00 mL。若反應消耗銅的質量為6.4 g,則硫酸銅的產率為 。
(已知![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 某溫度下,一元弱酸HA的Ka越小,則NaA的Kh(水解常數)越小
B. NaHCO3受熱易分解,可用于制胃酸中和劑
C. 反應活化能越高,該反應越易進行
D. 鍋爐水垢可先用Na2CO3處理,再用鹽酸去除
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】使18g焦炭發生不完全燃燒,所得氣體中CO占1/3體積,CO2占2/3體積,已知:C(s)+1/2O2(g)=CO(g) ΔH=-Q1kJ/mol;CO(g)+1/2O2(g)=CO2(g) ΔH=-Q2kJ/mol。與這些焦炭完全燃燒相比較,損失的熱量是( )
A. 1/3Q1kJ B. 1/3Q2kJ C. 1/3(Q1+Q2)kJ D. 1/2Q2kJ
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com