
【題目】制取物質、探究物質的性質是學習化學必備的素養之一。
回答下列問題。
(1)實驗室從含碘廢液(除水外含CCl4、I2、I-等)中回收碘,其實驗流程如下。

回答下列問題:
①物質X的名稱為________;
②操作Ⅰ選用的裝置為______(填標號);

③含碘廢液中加入稍過量的Na2SO3溶液將I2還原為I-,反應的離子方程式為___。
④氧化劑Y可用Cl2,也可以用H2O2。將同物質的量的I-轉化為I2,所需Cl2和H2O2的物質的量之比為________。
(2)某研究小組查閱資料知:氧化性的強弱順序為:Cl2>IO3->I2。用如圖裝置對Cl2與KI溶液的反應進行探究,發現通入Cl2一段時間后,KI溶液變為黃色,繼續通入Cl2,則溶液黃色變淺,最后變為無色。

①NaOH溶液的作用是______,反應的離子方程式為___________。
②溶液由黃色最后變為無色所發生反應的離子方程式為____________。
【答案】 四氯化碳 B SO32-+I2 +H2O=SO42-+2I-+2H+ 1:1 吸收尾氣Cl2 Cl2+2OH-=H2O+Cl-+ClO- 5Cl2+I2 +6H2O=2IO3-+10Cl-+12H+
【解析】(1)①亞硫酸鈉與單質碘發生氧化還原反應生成碘離子和硫酸根離子,四氯化碳不溶于水,分液即得到四氯化碳,因此物質X的名稱為四氯化碳;②操作Ⅰ是分液,需要利用分液漏斗,選用的裝置為B;③含碘廢液中加入稍過量的Na2SO3溶液將I2還原為I-,反應的離子方程式為SO32-+I2+H2O=SO42-+2I-+2H+。④1molCl2得到2mol電子,1molH2O2得到2mol電子,所以根據電子得失守恒可知將同物質的量的I-轉化為I2,所需Cl2和H2O2的物質的量之比為1:1。(2)①氯氣有毒,需要尾氣處理,則NaOH溶液的作用是吸收尾氣Cl2,反應的離子方程式為Cl2+2OH-=H2O+Cl-+ClO-。②通入Cl2一段時間后,KI溶液變為黃色,說明有單質碘生成,繼續通入Cl2,溶液黃色變淺,最后變為無色,根據氧化性強弱順序可判斷生成的單質碘繼續被氯氣氧化為碘酸,因此溶液由黃色最后變為無色所發生反應的離子方程式為5Cl2+I2+6H2O=2IO3-+10Cl-+12H+。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】在人類社會的發展進程中,金屬起著重要的作用。
(1)以下有關金屬單質的敘述正確的是_______。
A.金屬鈉非常活潑,在實驗室中保存在石蠟油或煤油中
B.用坩堝鉗夾住一小塊鋁箔,在酒精燈上加熱,可觀察到鋁箔熔化,并有熔融物滴下
C.鐵單質與水蒸氣反應的化學方程式為:2Fe+3H2O(g)![]() Fe2O3+3H2
Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三種固體組成的混合物溶于足量水后,產生1.16g白色沉淀,再向所得濁液中逐漸加入1.00mol/LHCl溶液,加入HCl溶液的體積與生成沉淀的關系如圖所示。
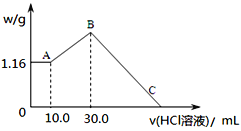
①A點的沉淀物的化學式為______________。
②寫出A點至B點發生反應的離子方程式:_________________。
③某溶液中溶有MgCl2和AlCl3兩種溶質,若把兩者分開,應選用的試劑為:NaOH溶液、_______和鹽酸。
④C點(此時沉淀恰好完全溶解)HCl溶液的體積為________mL。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組同學用如圖所示裝置設計實驗,檢驗碳與濃硫酸反應的產物。
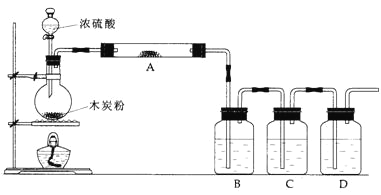
(1)寫出濃硫酸和木炭粉在加熱條件下發生反應的化學方程式:___________。
(2)儀器A中應加入的試劑是______,作用是____________。
(3)儀器B中應加入的試劑是_____,作用是________。
(4)該實驗小組在C中加入過量的酸性KMnO4溶液,D中加入澄清的石灰水,可根據__________現象判斷產物中存在CO2氣體。C中發生反應的離子方程式為:__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某原子的摩爾質量是M g/mol,則一個此原子的真實質量約為( )
A. M克 B. 1 / M克 C. M / ( 6.02×1023 )克 D. ( 6.02×1023 ) / M克
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的分類正確的是
酸 | 堿 | 鹽 | 酸性氧化物 | 堿性氧化物 | |
A | H2SO4 | Na2CO3 | Cu2(OH)2CO3 | SO3 | Fe2O3 |
B | HCl | NaOH | NaCl | CO2 | Na2O2 |
C | NaHSO4 | NaOH | CuSO4·5H2O | SO2 | MgO |
D | HNO3 | KOH | NaHCO3 | Mn2O7 | CaO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列各組離子在指定溶液中一定能大量共存的是
A.強酸性溶液:K+、HCO3、Br、Ba2+
B.滴加酚酞溶液顯紅色的溶液:Fe3+、NH4+、Cl、NO3
C.強酸性溶液:Cu2+、Na+、Mg2+、SO42
D.含有大量HCO3的溶液:Na+、NO3、Cl、OH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鹵代烴與金屬鎂在無水乙醚中反應,可得格氏試劑R﹣MgX,它可與醛、酮等羰基化合物加成: ![]() ,所得產物經水解可以得到醇,這是某些復雜醇的合成方法之一.現欲合成(CH3)3C﹣OH,下列所選用的鹵代烴和羰基化合物的組合正確的是( )
,所得產物經水解可以得到醇,這是某些復雜醇的合成方法之一.現欲合成(CH3)3C﹣OH,下列所選用的鹵代烴和羰基化合物的組合正確的是( )
A.乙醛和氯乙烷
B.甲醛和1﹣溴丙烷
C.甲醛和2﹣溴丙烷
D.丙酮和一氯甲烷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的轉化在給定條件下均能通過一步反應實現的是( )
A. NaAlO2(aq)![]() AlCl3
AlCl3![]() Al2O3 B. N2
Al2O3 B. N2![]() NO2
NO2![]() HNO3
HNO3
C. NaCl(飽和)![]() NaHCO3
NaHCO3![]() Na2CO3 D. FeS2
Na2CO3 D. FeS2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用可再生的物質制備乙酸乙酯的綠色合成路線之一如圖所示: 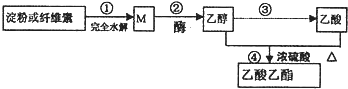
下列說法正確的是( )
A.常溫下,M能與銀氨溶液發生反應
B.④的反應類型屬于酯化反應,不屬于取代反應
C.用飽和碳酸鉀溶液能鑒別乙醇、乙酸和乙酸乙酯
D.淀粉和纖維素的化學式均為(C6H10O5)n , 二者互為同分異構體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com